13.下列说法中不正确的是( )
| A. | 在金属单质中,钠的熔点较低 | |
| B. | 钠在发生化学反应时化合价升高 | |
| C. | 钠在空气中燃烧生成氧化钠,并发生黄色火焰 | |
| D. | 钠原子最外层只有一个电子,容易失电子 |
12.下列物质之间的反应,一定不能生成盐的是( )
| A. | 酸性氧化物与碱反应 | B. | 碱性氧化物与酸反应 | ||
| C. | 单质与化合物的置换反应 | D. | 金属与氧气化合 |
11.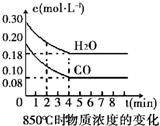 在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0.
在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0.
(1)CO和H2O浓度变化如右图,则在该温度下,该反应的平衡常数K=1.0~4min的平均反应速率v(CO)=0.03mol•L-1•min-1.若降低温度,该反应的K值将增大,该反应的化学反应速率将减小(填“增大”“减小”或“不变”).
(2)在相同容器中发生上述反应,当温度高于850℃时,容器内各物质的浓度变化如表.
①表中3min~4min之间反应处于平衡状态; c1数值大于0.08mol•L-1 (填大于、小于或等于).
②反应在4min~5min间,平衡向逆方向移动,可能的原因是d
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
(3)在相同温度下(850℃),若起始时c(CO)=1mol•L-1,c(H2O)=2mol•L-1,反应进行一段时间后,测得H2的浓度为0.5mol•L-1,则此时该反应是否达到平衡状态否(填“是”与“否”),此时v(正)大于v(逆)(填“大于”“小于”或“等于”),你判断的依据是浓度商Qc=$\frac{c(C{O}_{2})c({H}_{2})}{c(CO)c({H}_{2}O)}$=$\frac{0.5×0.5}{0.5×1.5}$=$\frac{1}{3}$<1,故平衡向正反应进行,此时v(正)>v(逆).
 在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0.
在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0.(1)CO和H2O浓度变化如右图,则在该温度下,该反应的平衡常数K=1.0~4min的平均反应速率v(CO)=0.03mol•L-1•min-1.若降低温度,该反应的K值将增大,该反应的化学反应速率将减小(填“增大”“减小”或“不变”).
(2)在相同容器中发生上述反应,当温度高于850℃时,容器内各物质的浓度变化如表.
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
②反应在4min~5min间,平衡向逆方向移动,可能的原因是d
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
(3)在相同温度下(850℃),若起始时c(CO)=1mol•L-1,c(H2O)=2mol•L-1,反应进行一段时间后,测得H2的浓度为0.5mol•L-1,则此时该反应是否达到平衡状态否(填“是”与“否”),此时v(正)大于v(逆)(填“大于”“小于”或“等于”),你判断的依据是浓度商Qc=$\frac{c(C{O}_{2})c({H}_{2})}{c(CO)c({H}_{2}O)}$=$\frac{0.5×0.5}{0.5×1.5}$=$\frac{1}{3}$<1,故平衡向正反应进行,此时v(正)>v(逆).
10. 常温下,向10mL0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH:溶液.有关微粒的物质的量变化如图(其中I代表、H2A,Ⅱ代表ⅡAⅢ代表A2-).根据图示判断,下列说法不正确的是( )
常温下,向10mL0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH:溶液.有关微粒的物质的量变化如图(其中I代表、H2A,Ⅱ代表ⅡAⅢ代表A2-).根据图示判断,下列说法不正确的是( )
 常温下,向10mL0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH:溶液.有关微粒的物质的量变化如图(其中I代表、H2A,Ⅱ代表ⅡAⅢ代表A2-).根据图示判断,下列说法不正确的是( )
常温下,向10mL0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH:溶液.有关微粒的物质的量变化如图(其中I代表、H2A,Ⅱ代表ⅡAⅢ代表A2-).根据图示判断,下列说法不正确的是( )| A. | 当V(NaOH)=10mL时,溶液中离子浓度的关系一有定:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| B. | 当V(NaOH)=15mL时,溶液中离子浓度的关系一定有:c(HA-)+2c(H+)+3c(H2A)=c(A2-)+2c(OH-) | |
| C. | 当V(NaOH)=15mL时,向溶液中滴加少量的盐酸或NaOH溶液,溶液的pH保持不变 | |
| D. | 当V(NaOH)=20mL时,向溶液中加水稀释,c(H+)减小,Kw不变 |
6.设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温下,32gO2含有2nA个氧原子 | |
| B. | 1mol Na2O2与足量水反应,转移2nA个电子 | |
| C. | 1L0.1mol•L-1Na2CO3溶液中含有0.1nA个CO${\;}_{3}^{2-}$ | |
| D. | 常温常压下,22.4LCH4中含有nA个CH4分子 |
5.下列关于反应KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O说法正确的是( )
| A. | 还原剂是KClO3 | B. | HCl被还原 | ||
| C. | 得到3molCl2转移6mol电子 | D. | 氧化产物、还原产物都是Cl2 |
4.能在水溶液中大量共存的一组离子是( )
0 171787 171795 171801 171805 171811 171813 171817 171823 171825 171831 171837 171841 171843 171847 171853 171855 171861 171865 171867 171871 171873 171877 171879 171881 171882 171883 171885 171886 171887 171889 171891 171895 171897 171901 171903 171907 171913 171915 171921 171925 171927 171931 171937 171943 171945 171951 171955 171957 171963 171967 171973 171981 203614
| A. | H+、Fe3+、I-、SO${\;}_{4}^{2-}$ | B. | Al3+、Mg2+、CO${\;}_{3}^{2-}$、Cl- | ||
| C. | K+、Fe2+、Ca2+、NO3- | D. | HCO3-、Na+、OH-、MnO4- |

 ,等物质的量的A、D完全燃烧生成水的质量之比为5:4;
,等物质的量的A、D完全燃烧生成水的质量之比为5:4; +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$ +NaCl+H2O;
+NaCl+H2O; .
.