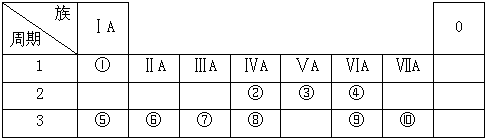
20.如图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为 .
.
(2)地壳中含量最多的金属元素是Al.写出元素⑥的氢化物的化学式CH4.
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(4)写出③.④.⑤对应离子氧化性由强到弱的是Al3+>Mg2+>Na+,②、⑦、⑩对应氢化物酸性由强到弱的是HBr>HCl>HF.
(5)写出⑪与氢氧化钠反应的化学方程式:Si+2NaOH+H2O=Na2SiO3+2H2↑.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ① | ② | |||||
| 三 | ③ | ④ | ⑤ | ⑪ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
 .
.(2)地壳中含量最多的金属元素是Al.写出元素⑥的氢化物的化学式CH4.
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(4)写出③.④.⑤对应离子氧化性由强到弱的是Al3+>Mg2+>Na+,②、⑦、⑩对应氢化物酸性由强到弱的是HBr>HCl>HF.
(5)写出⑪与氢氧化钠反应的化学方程式:Si+2NaOH+H2O=Na2SiO3+2H2↑.
19. 短周期元素A、B、C在周期表中的位置如图所示.已知B、C两元素所在族数之和是A元素族数的2倍,B、C两元素的原子序数之和是A元素的4倍,则A、B、C是( )
短周期元素A、B、C在周期表中的位置如图所示.已知B、C两元素所在族数之和是A元素族数的2倍,B、C两元素的原子序数之和是A元素的4倍,则A、B、C是( )
 短周期元素A、B、C在周期表中的位置如图所示.已知B、C两元素所在族数之和是A元素族数的2倍,B、C两元素的原子序数之和是A元素的4倍,则A、B、C是( )
短周期元素A、B、C在周期表中的位置如图所示.已知B、C两元素所在族数之和是A元素族数的2倍,B、C两元素的原子序数之和是A元素的4倍,则A、B、C是( )| A. | Be、Na、Al | B. | B、Mg、Si | C. | O、P、Cl | D. | C、Al、P |
17.下列电子式或结构式错误的是( )
| A. | OH-的电子式 | B. | NH4Br的电子式 | C. | Na2O的电子式: | D. | Na+的电子式:Na+ |
16.J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最高正化合价与最低负化合价的绝对值相等;M是地壳中含量仅次于氧元素的非金属元素;L的最简单气态氢化物甲能使湿润的红色石蕊试纸变蓝.
(1)M的原子结构示意图为 ; 元素T最高价氧化物对应水化物化学式是Cl2O7.
; 元素T最高价氧化物对应水化物化学式是Cl2O7.
(2)写出J和氧形成的一种酸性氧化物的电子式 ,含有共价键是极性键(填极性键或非极性键).
,含有共价键是极性键(填极性键或非极性键).
(3)写出能说明T非金属性比R强的反应的化学方程式Cl2+H2S=2HCl+S
(4)在微电子工业中,甲的水溶液可作刻蚀剂H2O2 的清除剂,所发生反应的产物不污染环境,其化学方程式为2NH3•H2O+3H2O2=N2↑+8H2O.
| J | |||
| R |
 ; 元素T最高价氧化物对应水化物化学式是Cl2O7.
; 元素T最高价氧化物对应水化物化学式是Cl2O7.(2)写出J和氧形成的一种酸性氧化物的电子式
 ,含有共价键是极性键(填极性键或非极性键).
,含有共价键是极性键(填极性键或非极性键).(3)写出能说明T非金属性比R强的反应的化学方程式Cl2+H2S=2HCl+S
(4)在微电子工业中,甲的水溶液可作刻蚀剂H2O2 的清除剂,所发生反应的产物不污染环境,其化学方程式为2NH3•H2O+3H2O2=N2↑+8H2O.
14.下列叙述正确的是( )


| A. | A的结构简式是CH3CH2COOH | B. | B代表的是苯的结构模型 | ||
| C. | D代表的是甲烷 | D. | C和D互为同系物 |
11.关于FeCl3溶液水解的错误说法是( )
0 171507 171515 171521 171525 171531 171533 171537 171543 171545 171551 171557 171561 171563 171567 171573 171575 171581 171585 171587 171591 171593 171597 171599 171601 171602 171603 171605 171606 171607 171609 171611 171615 171617 171621 171623 171627 171633 171635 171641 171645 171647 171651 171657 171663 171665 171671 171675 171677 171683 171687 171693 171701 203614
| A. | FeCl3水解使溶液呈酸性,并能起净水作用,使水中悬浮的杂质沉降 | |
| B. | 浓度为5mol•L-1和0.5mol•L-1的两种FeCl3溶液,其它条件相同时,Fe3+离子的水解程度前者比后者低 | |
| C. | 加热FeCl3溶液并蒸干,再灼烧,此时得到的固体是无水氯化铁 | |
| D. | 为了抑制Fe3+的水解,更好地保存FeCl3溶液,应向其中加入少量的盐酸 |
 .
.
 .
.