6.下列叙述正确的是( )
| A. | 某有机物分子中无支链,其名称为“乙×”,则该有机物的一个分子中一定含两个碳原子 | |
| B. | 放热反应的反应速率总是大于吸热反应的反应速率 | |
| C. | 应用盖斯定律,可以计算某些难于直接测量的反应的反应热 | |
| D. | △H小于零的反应是放热反应,这类反应的平衡常数K一般都大于1 |
5.加热下列溶液,其pH值不变的是( )(假设溶液的体积不变)
| A. | 稀H2SO4 | B. | 醋酸溶液 | C. | NaCl溶液 | D. | FeCl3溶液 |
4.升高温度,下列数据不一定增大的是( )
| A. | 某放热反应的正反应速率 | B. | 化学反应的平衡常数 | ||
| C. | 水的离子积 | D. | 吸热反应中反应物的转化率 |
3. 某密闭容器中发生如下反应:X(g)+3Y(g)?2Z(g)△H<0,如图表示该反应的速率随时间变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是( )
某密闭容器中发生如下反应:X(g)+3Y(g)?2Z(g)△H<0,如图表示该反应的速率随时间变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是( )
 某密闭容器中发生如下反应:X(g)+3Y(g)?2Z(g)△H<0,如图表示该反应的速率随时间变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是( )
某密闭容器中发生如下反应:X(g)+3Y(g)?2Z(g)△H<0,如图表示该反应的速率随时间变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是( )| A. | t2时升高了温度 | |
| B. | t3时降低了温度 | |
| C. | t5时增大了压强(缩小容器体积) | |
| D. | 平衡状态时,t6时刻Z的百分含量最低 |
2.下列平衡体系在体积不变时,加入所给物质,平衡可以发生移动的是( )
| A. | 在FeCl3(aq)+KSCN(aq)?Fe(SCN)3(aq)+3KCl(aq) 平衡体系中,加入KCl晶体 | |
| B. | 在N2(g)+3H2(g)?2NH3(g) 平衡体系中,通入HCl气体 | |
| C. | 在CaCO3(s)?Ca2+(aq)+CO32-(aq)平衡体系中,加入CaCO3固体 | |
| D. | 在2SO2(g)+O2(g)?2SO3(g) 平衡体系中,通入N2 |
1.已知下列热化学方程式:
C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1
现有0.2mol的炭粉和氢气组成的气、固混合物在氧气中完全燃烧,共放出63.53kJ热量,则炭粉与氢气的物质的量之比为( )
C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1
现有0.2mol的炭粉和氢气组成的气、固混合物在氧气中完全燃烧,共放出63.53kJ热量,则炭粉与氢气的物质的量之比为( )
| A. | 1:1 | B. | 1:2 | C. | 2:3 | D. | 3:2 |
20.已知溴酸银的溶解是吸热过程,在不同温度下溴酸银溶解平衡曲线如图所示,下列说法正确的是( )
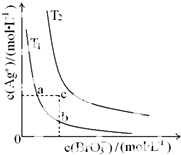

| A. | T1>T2 | |
| B. | 加入AgNO3固体,可使a点变到c点 | |
| C. | a点和b点的Ksp相等 | |
| D. | c点时,在T1、T2两个温度下均有固体析出 |
17.已知一种c(H+)=1×10-3mol•L-1的酸和一种c(OH-)=1×10-3mol•L-1的碱溶液等体积混合后,溶液呈酸性,其原因可能是( )
0 171433 171441 171447 171451 171457 171459 171463 171469 171471 171477 171483 171487 171489 171493 171499 171501 171507 171511 171513 171517 171519 171523 171525 171527 171528 171529 171531 171532 171533 171535 171537 171541 171543 171547 171549 171553 171559 171561 171567 171571 171573 171577 171583 171589 171591 171597 171601 171603 171609 171613 171619 171627 203614
| A. | 浓的强酸和稀的强碱溶液反应 | B. | 浓的弱酸和稀的强碱溶液反应 | ||
| C. | 等浓度的强酸和弱碱溶液反应 | D. | 生成一种强酸弱碱盐 |