15.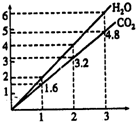 两种气态烃组成的混合气体,完全燃烧后得到C02和H2O的物质的量随着混合烃物质的量的变化如图所示.则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体,完全燃烧后得到C02和H2O的物质的量随着混合烃物质的量的变化如图所示.则下列对混合烃的判断正确的是( )
 两种气态烃组成的混合气体,完全燃烧后得到C02和H2O的物质的量随着混合烃物质的量的变化如图所示.则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体,完全燃烧后得到C02和H2O的物质的量随着混合烃物质的量的变化如图所示.则下列对混合烃的判断正确的是( )| A. | 一定含有CH4 | B. | 一定含有C2H6 | C. | 一定含有C2H4 | D. | 一定不含有C3H4 |
14.设NA 为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 1mol羟基中电子数为10NA | |
| B. | 常温下,1L 0.1mol/L的NH4NO3的溶液中氮原子数为0.2NA | |
| C. | 在反应KIO3+6HI=KI+3 I2+3 H2O中,每生成3mol I2转移的电子数为6NA | |
| D. | 常温常压下,22.4L乙烯中C-H键数为4NA |
12.某饱和一元醇 8g 与足量金属钠反应产生氢气 2.8L(标准状况).该醇可能是( )
| A. | 甲醇 | B. | 乙醇 | C. | 丙醇 | D. | 丁醇 |
11.有机物甲能发生银镜反应,甲催化加氢还原成有机物乙,1mol乙跟足量的金属钠反应放出标准状况下氢气22.4L,据此推断乙一定不是( )
| A. | HOCH2CH2OH | B. | HOCH2CH(OH)CH3 | C. | HOCH2CH2CH2OH | D. | CH3CH(OH)CH(OH)CH3 |
10.CH3COOH分别跟H-18O-C2H5和H-16O-C2H5起酯化反应后,两者生成水的质量( )
| A. | 前者大 | B. | 前者小 | C. | 相等 | D. | 不能确定 |
9. Ⅰ.甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究.向A中通入氯气至过量,观察A中,发现溶液先呈红色,然后变为黄色.
Ⅰ.甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究.向A中通入氯气至过量,观察A中,发现溶液先呈红色,然后变为黄色.
(1)B中反应的离子方程式是Cl2+2OH-═Cl-+ClO-+H2O;
(2)为了探究A中溶液由红色变为黄色的原因,甲同学进行如下实验.取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在Fe3+;
(3)资料显示:SCN -的电子式为 .甲同学猜想SCN-可能被Cl2氧化了,他进行了如下研究;
.甲同学猜想SCN-可能被Cl2氧化了,他进行了如下研究;
①取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明
SCN-中被氧化的元素是硫元素;
②甲同学通过实验证明了SCN-中氮元素转化为NO3-,已知SCN-中碳元素没有被氧化,若SCN-与Cl2反应生成1mol CO2,则转移电子的物质的量是16mol;
Ⅱ.8.12天津港特大爆炸事故现场有700吨左右氰化钠,氰化钠剧毒.有少量因爆炸冲击发生泄漏.这些泄露的氰化钠可通过喷洒氧化剂双氧水的方式来处理,以减轻污染.
(1)写出NaCN的电子式Na+ ,偏碱性条件下,氰化钠溶液的CN-被双氧水氧化为HCO3-,同时放出NH3,该反应的离子方程式:CN-+H2O2+H2O═NH3↑+HCO3-;
,偏碱性条件下,氰化钠溶液的CN-被双氧水氧化为HCO3-,同时放出NH3,该反应的离子方程式:CN-+H2O2+H2O═NH3↑+HCO3-;
(2)Cu2+可作为双氧水氧化CN-中的催化剂.某兴趣小组要探究Cu2+对双氧水氧化CN-是否起催化作用,请你完成下实验方案.填写实验步骤、实验现象和结论(己知:CN-浓度可用离子色谱仪测定)
 Ⅰ.甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究.向A中通入氯气至过量,观察A中,发现溶液先呈红色,然后变为黄色.
Ⅰ.甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究.向A中通入氯气至过量,观察A中,发现溶液先呈红色,然后变为黄色.(1)B中反应的离子方程式是Cl2+2OH-═Cl-+ClO-+H2O;
(2)为了探究A中溶液由红色变为黄色的原因,甲同学进行如下实验.取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在Fe3+;
(3)资料显示:SCN -的电子式为
 .甲同学猜想SCN-可能被Cl2氧化了,他进行了如下研究;
.甲同学猜想SCN-可能被Cl2氧化了,他进行了如下研究;①取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明
SCN-中被氧化的元素是硫元素;
②甲同学通过实验证明了SCN-中氮元素转化为NO3-,已知SCN-中碳元素没有被氧化,若SCN-与Cl2反应生成1mol CO2,则转移电子的物质的量是16mol;
Ⅱ.8.12天津港特大爆炸事故现场有700吨左右氰化钠,氰化钠剧毒.有少量因爆炸冲击发生泄漏.这些泄露的氰化钠可通过喷洒氧化剂双氧水的方式来处理,以减轻污染.
(1)写出NaCN的电子式Na+
 ,偏碱性条件下,氰化钠溶液的CN-被双氧水氧化为HCO3-,同时放出NH3,该反应的离子方程式:CN-+H2O2+H2O═NH3↑+HCO3-;
,偏碱性条件下,氰化钠溶液的CN-被双氧水氧化为HCO3-,同时放出NH3,该反应的离子方程式:CN-+H2O2+H2O═NH3↑+HCO3-;(2)Cu2+可作为双氧水氧化CN-中的催化剂.某兴趣小组要探究Cu2+对双氧水氧化CN-是否起催化作用,请你完成下实验方案.填写实验步骤、实验现象和结论(己知:CN-浓度可用离子色谱仪测定)
| 步骤:分别取等体积、等浓度的含氰废水于甲、乙两支试管中,再分别加入等体积、等浓度的双氧水溶液,只向甲试管中加入少量的无水硫酸铜粉末,用离子色谱仪测定相同反应时间内两支试管中的CN-浓度 | 现象与结论: 若甲试管中的CN-浓度小于乙试管中的CN-浓度,则Cu2+对双氧水破氰反应起催化作用 若两试管中的CN-浓度相同,则Cu2+对双氧水破氰反应不起催化作用 |
8.下列除杂所用试剂和操作不合理的是( )
| 选项 | 物质(括号中为杂质) | 除杂试剂 | 操作 |
| A | CO2(SO2) | 饱和NaHCO3溶液 | 洗气 |
| B | BaCO3(BaSO4) | 饱和Na2CO3溶液 | 搅拌、过滤 |
| C | 苯(苯酚) | 浓溴水 | 过滤 |
| D | Cl2(HCl) | 饱和食盐水 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
7.装置图所示,有关分析不正确的是( )


| A. | 该装置中Cu极为阳极 | |
| B. | 工作时,左池中K+移向a电极 | |
| C. | 工作一段时间,要使右池溶液复原可加入适量的CuO | |
| D. | b极的电极反应式:H2+2OH--2e-═2H2O |
6.下列说法正确的是( )
0 171421 171429 171435 171439 171445 171447 171451 171457 171459 171465 171471 171475 171477 171481 171487 171489 171495 171499 171501 171505 171507 171511 171513 171515 171516 171517 171519 171520 171521 171523 171525 171529 171531 171535 171537 171541 171547 171549 171555 171559 171561 171565 171571 171577 171579 171585 171589 171591 171597 171601 171607 171615 203614
| A. | 第ⅠA族元素是同周期中金属性最强的金属元素 | |
| B. | 两个非金属原子间不可能形成离子键 | |
| C. | HF、HCl、HBr和HI的热稳定性和还原性依次减弱 | |
| D. | 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 |
 ,则其单体的结构简式为CH≡CH.
,则其单体的结构简式为CH≡CH.