11.2007年诺贝尔化学奖得主Gerhard Ertl对金属Pt表面催化氧化CO反应的模型进行了深入研究.下列关于${\;}_{78}^{202}$Pt和${\;}_{78}^{198}$Pt的说法正确的是( )
| A. | ${\;}_{78}^{202}$Pt和${\;}_{78}^{198}$Pt的核外电子数相同,是同一种核素 | |
| B. | 于${\;}_{78}^{202}$Pt和${\;}_{78}^{198}$Pt的中子数相同,互称为同位素 | |
| C. | 于${\;}_{78}^{202}$Pt和${\;}_{78}^{198}$Pt的质子数相同,互称为同位素 | |
| D. | 于${\;}_{78}^{202}$Pt和${\;}_{78}^{198}$Pt的质量数相同,不能互称为同位素 |
6.某研究性学习小组探究FeSO4的化学性质和用途.回答下列问题:
(一)探究FeSO4溶液的酸碱性:
取少量FeSO4固体,利用石蕊试液测试FeSO4溶液的酸碱性,必须选用的仪器有胶头滴管、药匙和B.
A.玻璃棒 B.试管 C.天平 D.量筒
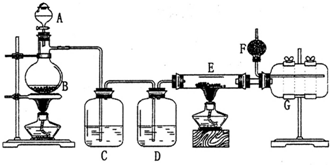
(二)利用下图装置探究FeSO4的稳定性

Ⅱ中有白色沉淀生成,小组成员结合理论分析,认为下列分解产物不可能的是A.
A.Fe2O3、SO3、H2O B.Fe2O3、SO2、SO3、H2O
C.FeO、Fe2O3、SO2、SO3、H2O
Ⅲ中溴水是用来检验是否有 SO2气体生成,若有SO2生成,溴水将褪色.实验中,观察到溴水褪色,据此推测FeSO4分解最有可能被氧化的元素是Fe.NaOH的作用是吸收SO2气体,请 写出最大量吸收SO2气体的反应化学方程式:2NaOH+SO2=Na2SO3+H2O.
(三)探究FeSO4中Fe2+还原性:
证明FeSO4有较强的还原性,完成下表.
(四)硫酸亚铁用途探究
缺铁性贫血往往口服硫酸亚铁,当用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,其作用是防止硫酸亚铁被氧化.
(一)探究FeSO4溶液的酸碱性:
取少量FeSO4固体,利用石蕊试液测试FeSO4溶液的酸碱性,必须选用的仪器有胶头滴管、药匙和B.
A.玻璃棒 B.试管 C.天平 D.量筒
(二)利用下图装置探究FeSO4的稳定性

Ⅱ中有白色沉淀生成,小组成员结合理论分析,认为下列分解产物不可能的是A.
A.Fe2O3、SO3、H2O B.Fe2O3、SO2、SO3、H2O
C.FeO、Fe2O3、SO2、SO3、H2O
Ⅲ中溴水是用来检验是否有 SO2气体生成,若有SO2生成,溴水将褪色.实验中,观察到溴水褪色,据此推测FeSO4分解最有可能被氧化的元素是Fe.NaOH的作用是吸收SO2气体,请 写出最大量吸收SO2气体的反应化学方程式:2NaOH+SO2=Na2SO3+H2O.
(三)探究FeSO4中Fe2+还原性:
证明FeSO4有较强的还原性,完成下表.
| 实验步骤 | 实验预期现象及结论 |
| 步骤一:取少量的FeSO4 固体于试管中,加入一定量水溶解 | |
| 步骤二: |
缺铁性贫血往往口服硫酸亚铁,当用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,其作用是防止硫酸亚铁被氧化.
4.将2molX 和2molY充入2L密闭容器中发生反应:X(g)+3Y(g)?2Z(g)+aQ(g).2min后达到平衡时生成0.8molZ,测得Q的浓度为0.6mol/L,下列叙述错误的是( )
0 171143 171151 171157 171161 171167 171169 171173 171179 171181 171187 171193 171197 171199 171203 171209 171211 171217 171221 171223 171227 171229 171233 171235 171237 171238 171239 171241 171242 171243 171245 171247 171251 171253 171257 171259 171263 171269 171271 171277 171281 171283 171287 171293 171299 171301 171307 171311 171313 171319 171323 171329 171337 203614
| A. | a的值为3 | B. | 平衡时X的浓度为0.8mol/L | ||
| C. | Y的转化率为60% | D. | 反应速率v(Y)=0.2mol/(L•min) |
 如图所示,钠、镁、铝、铁分别跟足量的氯气反应时,消耗金属的质量与反应的氯气的质量之间的关系,其中表示铝与氯气反应的是( )
如图所示,钠、镁、铝、铁分别跟足量的氯气反应时,消耗金属的质量与反应的氯气的质量之间的关系,其中表示铝与氯气反应的是( ) 碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下: