10. 将空气中久置的铁片投入盛有适量稀硫酸的烧杯中,反应产生氢气的速率与反应时间的关系可用如图曲线来表示.下列判断错误的是( )
将空气中久置的铁片投入盛有适量稀硫酸的烧杯中,反应产生氢气的速率与反应时间的关系可用如图曲线来表示.下列判断错误的是( )
 将空气中久置的铁片投入盛有适量稀硫酸的烧杯中,反应产生氢气的速率与反应时间的关系可用如图曲线来表示.下列判断错误的是( )
将空气中久置的铁片投入盛有适量稀硫酸的烧杯中,反应产生氢气的速率与反应时间的关系可用如图曲线来表示.下列判断错误的是( )| A. | 前a秒内,硫酸主要与氧化铁发生反应 | |
| B. | 铁与硫酸的反应为放热反应 | |
| C. | c秒后v(H2)减小是因为溶液c(H+)的减小 | |
| D. | 往烧杯中加入少量CuSO4,对v(H2)不影响 |
9.把一套以液化石油气(主要成分为C3H8和C4H10)为燃料的炉灶,现改用天然气(主要成分为CH4)为燃料,需要调整进入炉灶的燃料和空气的量.正确方法为( )
| A. | 只需调大燃料气的进气量 | B. | 只需调大空气的进气量 | ||
| C. | 同时调大燃料气和空气的量 | D. | 同时调小燃料气和空气的量 |
8.已知:合成氨反应(即N2+3H2═2NH3)为放热反应.反应过程中断裂1molN≡N消耗的能量为Q1kJ,断裂1molH-H消耗的能量为Q2kJ,断裂1molN-H消耗的能量为Q3kJ.下列关系式中正确的是( )
| A. | Q1+3Q2<6Q3 | B. | Q1+3Q2>2Q3 | C. | 3Q1+Q2>6Q3 | D. | Q1+3Q2<2Q3 |
7.若发现114号新元素X,下列有关X的相关推断合理的是( )
| A. | X是金属元素 | |
| B. | X的单质可作半导体材料 | |
| C. | X存在稳定的气态氢化物 | |
| D. | X最高价氧化物对应水化物的酸性较强 |
6.X、Y为周期表VIA族的两种元素,下列叙述能说明X得电子能力比Y强的是( )
| A. | X元素的电子层数比Y的电子层数多 | |
| B. | X的氢化物的沸点比Y的氢化物的沸点低 | |
| C. | X的气态氢化物比Y的气态氢化物稳定 | |
| D. | Y的单质能将X从H2X的溶液中置换出来 |
5.已知:M、N为短周期元素,M的原子序数小于N.M原子的最外层电子数是次外层电子数的3倍,N原子的次外导电子数是最外层电子数的2倍.下列说法中正确的是( )
| A. | 元素M、N属于同周期元素 | B. | 元素M、N属于同主族元素 | ||
| C. | 两元素组成的化合物为共价化合物 | D. | 两元素的原子半径大小:M>N |
4.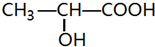 有机物甲的结构简式如图所示,利用该物质为原料制成的高分子材料乙具有生物兼容性.下列关于甲、乙的判断,错误的是( )
有机物甲的结构简式如图所示,利用该物质为原料制成的高分子材料乙具有生物兼容性.下列关于甲、乙的判断,错误的是( )
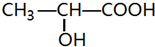 有机物甲的结构简式如图所示,利用该物质为原料制成的高分子材料乙具有生物兼容性.下列关于甲、乙的判断,错误的是( )
有机物甲的结构简式如图所示,利用该物质为原料制成的高分子材料乙具有生物兼容性.下列关于甲、乙的判断,错误的是( )| A. | 甲能与碳酸氢钠溶液发生反应 | |
| B. | 1mol甲能与2molNaOH反应 | |
| C. | 一定条件下,甲可发生酯化反应 | |
| D. | 由甲为原料制成高分子材料乙的反应不是加聚反应 |
3. 某由C、H、O组成的有机物分子结构模型如图(图中三种不同大小的球,分别表示三种不同的原子,数字“1”和“2”分别表示对应的化学键).下列有关说法正确的是( )
某由C、H、O组成的有机物分子结构模型如图(图中三种不同大小的球,分别表示三种不同的原子,数字“1”和“2”分别表示对应的化学键).下列有关说法正确的是( )
 某由C、H、O组成的有机物分子结构模型如图(图中三种不同大小的球,分别表示三种不同的原子,数字“1”和“2”分别表示对应的化学键).下列有关说法正确的是( )
某由C、H、O组成的有机物分子结构模型如图(图中三种不同大小的球,分别表示三种不同的原子,数字“1”和“2”分别表示对应的化学键).下列有关说法正确的是( )| A. | 该物质难溶于水,密度比水大 | |
| B. | 该物质不存在同分异构体 | |
| C. | 该物质与钠反应时,化学键“2”将断裂 | |
| D. | 该物质不可能发生取代反应 |
2.锂不仅在军事工业中占有举足轻重的地位,而且在民用工业也是一种重要的材料.已知,锂的核电荷数为3.下列说法错误的是( )
0 171029 171037 171043 171047 171053 171055 171059 171065 171067 171073 171079 171083 171085 171089 171095 171097 171103 171107 171109 171113 171115 171119 171121 171123 171124 171125 171127 171128 171129 171131 171133 171137 171139 171143 171145 171149 171155 171157 171163 171167 171169 171173 171179 171185 171187 171193 171197 171199 171205 171209 171215 171223 203614
| A. | 锂的原子半径比钠小 | B. | 锂原子核外有3个电子 | ||
| C. | 锂是第二周期IA族元素 | D. | LiOH的碱性比NaOH强 |
 已知:卤素的氢化物易溶于水.某同学采用如图所示装置研究氯气与甲烷反应.实验时,往U型管的左端装入甲烷和氯气(体积比为1:4)的混合气体,并将该装置放置在光亮处,让混合气体缓慢地反应一段时间.根据要求回答问题:
已知:卤素的氢化物易溶于水.某同学采用如图所示装置研究氯气与甲烷反应.实验时,往U型管的左端装入甲烷和氯气(体积比为1:4)的混合气体,并将该装置放置在光亮处,让混合气体缓慢地反应一段时间.根据要求回答问题: A.氢原子数为十二 B.一氯取代物只有一种结构.
A.氢原子数为十二 B.一氯取代物只有一种结构.