15.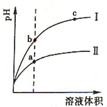 某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,溶液的pH随溶液体积变化的曲线如图所示.下列判断正确的是( )
某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,溶液的pH随溶液体积变化的曲线如图所示.下列判断正确的是( )
 某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,溶液的pH随溶液体积变化的曲线如图所示.下列判断正确的是( )
某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,溶液的pH随溶液体积变化的曲线如图所示.下列判断正确的是( )| A. | Ⅱ为盐酸稀释时的pH变化曲线 | |
| B. | a点Kw的数值比c点Kw的数值大 | |
| C. | b点酸的总浓度大于a点酸的总浓度 | |
| D. | b点溶液的导电性比c点溶液的导电性强 |
14.已知:在温度t1和t2下,X2(g)和H2反应生成HX的平衡常数如表.
随着卤素原子核电荷数的增加,仅依据K的变化,下列说法不正确的是( )
| 化学方程式 | K(t1) | K(t2) |
| F2+H2?2HF | 1.8×1036 | 1.9×1032 |
| Cl2+H2?2HCl | 9.7×1012 | 4.2×1011 |
| Br2+H2?2HBr | 5.6×107 | 9.3×106 |
| I2+H2?2HI | 42 | 34 |
| A. | 已知t2>t1,HX的生成反应是放热反应 | |
| B. | 在相同条件下,平衡时X2的转化率逐渐降低 | |
| C. | X2与H2反应的剧烈程度逐渐减弱 | |
| D. | HX的稳定性逐渐减弱 |
13.如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略).

(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
装置B中饱和食盐水的作用是除去Cl2中混有的HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗中液面上升,形成水柱.
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入d.
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱.当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为橙色,说明氯单质的氧化比溴单质强.
打开活塞,将装置D中少量溶液加入装置E中,振荡.观察到的现象液体分为两层,上层液体显紫红色.

(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
装置B中饱和食盐水的作用是除去Cl2中混有的HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗中液面上升,形成水柱.
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入d.
| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
打开活塞,将装置D中少量溶液加入装置E中,振荡.观察到的现象液体分为两层,上层液体显紫红色.
10.如图所示,电极a和b均为石墨棒,在电解过程中,下列说法正确的是( )


| A. | 电极a表面呈红色 | |
| B. | 电极b作阳极 | |
| C. | 电子由电源的正极沿导线流向电极a | |
| D. | 该装置能量转化形式为电能转化为化学能 |
8.对于如图所示装置的叙述正确的是( )
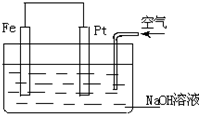

| A. | 这是一个原电池的装置 | |
| B. | 这是电解NaOH溶液的装置 | |
| C. | Pt为正极,其电极反应为:2H++2e-═H2↑ | |
| D. | Fe为负极,其电极反应为:4OH--4e-═2H2O+O2↑ |
7.下列固体物质溶于水,再将其溶液加热、蒸发结晶、再灼烧,能得到化学组成与原固体物质相同的是( )
①胆矾 ②氯化铝 ③硫酸铝 ④Na2CO3 ⑤NaHCO3 ⑥高锰酸钾.
①胆矾 ②氯化铝 ③硫酸铝 ④Na2CO3 ⑤NaHCO3 ⑥高锰酸钾.
| A. | ③④ | B. | ①③④ | C. | ①②③④⑤ | D. | 全部 |
6.下列说法中正确的是( )
0 170696 170704 170710 170714 170720 170722 170726 170732 170734 170740 170746 170750 170752 170756 170762 170764 170770 170774 170776 170780 170782 170786 170788 170790 170791 170792 170794 170795 170796 170798 170800 170804 170806 170810 170812 170816 170822 170824 170830 170834 170836 170840 170846 170852 170854 170860 170864 170866 170872 170876 170882 170890 203614
| A. | 在任何状况下,1 mol CO2和1 mol H2O所含的分子数和原子数都相等 | |
| B. | 只有在标准状况下,1 mol气体所占的体积才是22.4 L | |
| C. | 某物质含有阿伏加德罗常数个微粒,该物质在标准状况下体积为22.4 L | |
| D. | 22.4 L CO所含的分子数为6.02×1023个 |
