7.重金属是指相对原子质量大于55的金属,重金属离子具有毒性.实验室有甲、乙两种含重金属离子的废液,甲废液经化验呈碱性,主要有毒离子为Ba2+.如将甲、乙废液按一定比例混合,毒性明显降低.则乙废液中可能会有的离子是( )
| A. | Cu2+和SO42- | B. | K+和SO42- | C. | Cu2+和Cl- | D. | Ag+和NO3- |
3.A、B、C、D、E均为短周期元素,且原子序数依次增大,请根据表中信息回答下列问题:
(1)E在元素周期表中的位置第三周期第ⅥA族.
(2)B最简单气态氢化物的电子式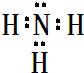 ,属于共价化合物(填“离子”或“共价”);D的最高价氧化物的水化物电子式
,属于共价化合物(填“离子”或“共价”);D的最高价氧化物的水化物电子式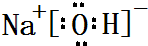 ,所含化学键类型:离子键、共价键.
,所含化学键类型:离子键、共价键.
(3)B、C、D、E简单离子半径由大到小顺序为:S2->N3->O2->Na+(填元素符号).
(4)用电子式表示E的氢化物的形成过程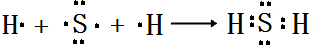 .
.
(5)由A、B、C与氢元素组成的一种常见酸式盐与过量D的最高价氧化物的水化物反应的离子方程式:NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O.
(6)19.2g金属铜与一定浓度的B的最高价氧化物的水化物反应,产生标准状况下NO、NO2(不考虑N2O4的存在)混合气6.72L,则参加反应的HNO3的物质的量为0.9mol.
| 元素 | 元素性质或结构 |
| A | 最外层电子数是其内层电子数的2倍 |
| B | B元素的单质在空气中含量最多 |
| C | C元素在地壳中含量最多 |
| D | D元素在同周期中金属性最强 |
| E | 常温常压下,E元素形成的单质是淡黄色固体,常在火山口附近沉积 |
(2)B最简单气态氢化物的电子式
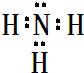 ,属于共价化合物(填“离子”或“共价”);D的最高价氧化物的水化物电子式
,属于共价化合物(填“离子”或“共价”);D的最高价氧化物的水化物电子式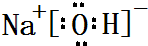 ,所含化学键类型:离子键、共价键.
,所含化学键类型:离子键、共价键.(3)B、C、D、E简单离子半径由大到小顺序为:S2->N3->O2->Na+(填元素符号).
(4)用电子式表示E的氢化物的形成过程
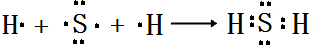 .
.(5)由A、B、C与氢元素组成的一种常见酸式盐与过量D的最高价氧化物的水化物反应的离子方程式:NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O.
(6)19.2g金属铜与一定浓度的B的最高价氧化物的水化物反应,产生标准状况下NO、NO2(不考虑N2O4的存在)混合气6.72L,则参加反应的HNO3的物质的量为0.9mol.
2.下述实验操作与预期实验目的或所得实验结论不一致的是( )
| 编号 | 实验操作 | 实验目的或结论 |
| A | 将SO2气体通入紫色石蕊试液中,观察溶液是否褪色 | 证明SO2有漂白性 |
| B | 向试管中加入等体积的0.005mol/L的FeCl3溶液和0.01mol/L的KSCN溶液,再滴加几滴饱和FeCl3溶液,观察颜色变化 | 探究增大反应物浓度时平衡移动的方向 |
| C | 将装有NO2和N2O4气体的联通球,一个置于冰水中,一个置于热水中,观察颜色变化 | 探究温度对化学平衡的影响 |
| D | 将CO2通入Na2SiO3水溶液观察是否有沉淀产生 | 探究碳和硅两元素非金属性强弱 |
| A. | A | B. | B | C. | C | D. | D |
1.23592U和23892U是铀的两种主要的同位素.U是制造原子弹和核反应堆的主要原料.下列有关说法正确的是( )
| A. | U原子核中含有92个中子 | B. | U原子核外有143个电子 | ||
| C. | 23592U和23892U互为同位素 | D. | 23592U和23892U互为同素异形体 |
19.下列叙述正确的是( )
0 170438 170446 170452 170456 170462 170464 170468 170474 170476 170482 170488 170492 170494 170498 170504 170506 170512 170516 170518 170522 170524 170528 170530 170532 170533 170534 170536 170537 170538 170540 170542 170546 170548 170552 170554 170558 170564 170566 170572 170576 170578 170582 170588 170594 170596 170602 170606 170608 170614 170618 170624 170632 203614
| A. | 预测PCl3的立体构型为平面三角形 | |
| B. | SO2和CO2都是含有极性键的非极性分子 | |
| C. | 在NH4+和[Cu(NH3)4]2+中都存在配位键 | |
| D. | 铝元素的原子核外共有5种不同运动状态的电子 |

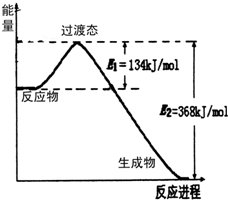 (1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1.
(1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1.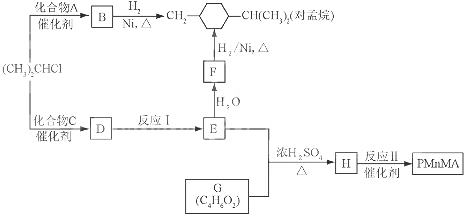

 ,
,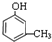
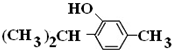 +3H2$→_{△}^{Ni}$
+3H2$→_{△}^{Ni}$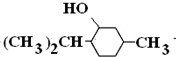
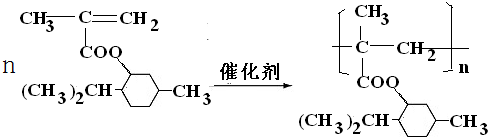 ;.
;.