0 16944 16952 16958 16962 16968 16970 16974 16980 16982 16988 16994 16998 17000 17004 17010 17012 17018 17022 17024 17028 17030 17034 17036 17038 17039 17040 17042 17043 17044 17046 17048 17052 17054 17058 17060 17064 17070 17072 17078 17082 17084 17088 17094 17100 17102 17108 17112 17114 17120 17124 17130 17138 203614
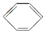
 (1)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示.
(1)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示.
 、④HCHO等,其中碳原子采取sp2杂化的分子有
、④HCHO等,其中碳原子采取sp2杂化的分子有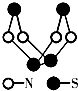 (2009?宜宾模拟)现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
(2009?宜宾模拟)现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )