8.反应NO2(g)+CO(g)=NO(g)+CO2(g)△H=+234kJ•mol-1的反应机理为:2NO2=NO3+NO(慢) NO2+CO=NO2+CO2(快)下列有关该反应的说法正确的是( )
| A. | 正反应的活化能比逆反应的活化能大234kJ•mol-1 | |
| B. | NO3是该反应的催化剂 | |
| C. | 化学反应速率v(NO2)=2v(CO) | |
| D. | 过程1和过程2均为放热反应 |
7.下列物质应用过程中,没有发生氧化还原反应的是( )
| A. | 铝热剂用于焊接钢轨 | B. | 过氧化钠用于呼吸面具供氧 | ||
| C. | 湿润红色石蕊试纸检验氨气 | D. | 湿润的淀粉碘化钾试纸检验氯气 |
5.在常温时,将V1mLc1mol•L-1CH3COOH溶液中滴加到V2mLc2mol•L-1NaOH溶液中,下列结论中,错误的是( )
| A. | 如果V1=V2,c1=c2,则混合溶液中c(CH3COO-)=c(Na+) | |
| B. | 如果混合溶液的pH=7,则混合溶液中c(CH3COO-)=c(Na+) | |
| C. | 如果混合溶液的pH>7,则不可能V1c1=V2c2 | |
| D. | 如果V1=V2,且混合溶液的pH<7,则c1>c2 |
4.X、Y、Z、W为四种短周期元素,它们在周期表中位于连续的四个主族,如图所示.Z元素原子最外层电子数是内层电子总数的$\frac{1}{5}$.下列说法中正确的是( )
| X | Y | ||
| Z | W |
| A. | 原子半径由小到大的顺序为X<Z<Y<W | |
| B. | Y元素最高价氧化物对应的水化物化学式为HYO3 | |
| C. | X、Z两种元素的氧化物中所含化学键类型相同 | |
| D. | Y最简单气态氢化物比Y相邻周期同主族元素气态氢化物沸点高 |
3.下列操作和现象与结论均正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 向盐酸酸化的Ba(NO3)2溶液中通入SO2 | 有白色沉淀生成 | BaSO3难溶于酸 |
| B | 向等浓度的KCl、Kl混合液中滴加AgNO3溶液 | 先出现白色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 溴乙烷与NaOH水溶液共热后,加HNO3酸化,滴加AgNO3溶液 | 出现淡黄色沉淀 | 溴乙烷含溴元素 |
| D | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
| A. | A | B. | B | C. | C | D. | D |
19.实验室进行:Cu+2H2SO4(浓)$\stackrel{△}{→}$CuSO4+SO2↑+2H2O,反应因硫酸浓度下降而停止.为测定反应残余液中硫酸的浓度,探究小组同学设计了4组实验方案(将残余液稀释至1L,每次均量取20mL稀释液进行实验),其中可行的是( )
0 167497 167505 167511 167515 167521 167523 167527 167533 167535 167541 167547 167551 167553 167557 167563 167565 167571 167575 167577 167581 167583 167587 167589 167591 167592 167593 167595 167596 167597 167599 167601 167605 167607 167611 167613 167617 167623 167625 167631 167635 167637 167641 167647 167653 167655 167661 167665 167667 167673 167677 167683 167691 203614
| A. | 加入足量BaCl2溶液反应,过滤、洗涤、干燥、恒重,称得固体质量为W1 g | |
| B. | 加入过量的W2 g Zn充分反应后,过滤、洗涤、干燥、恒重,称得固体质量为W3 g | |
| C. | 加入过量的W4 g CaCO3反应停止后,过滤、洗涤、干燥、恒重,称得固体质量为W5 g | |
| D. | 滴入适当指示剂,用已知浓度的NaOH溶液进行滴定,消耗NaOH溶液的体积为V mL |
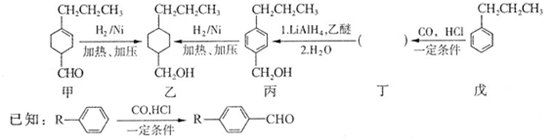
 和
和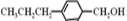 生成(写结构简式).
生成(写结构简式). .
. +H2O$→_{△}^{NaOH}$
+H2O$→_{△}^{NaOH}$ +HCl或
+HCl或
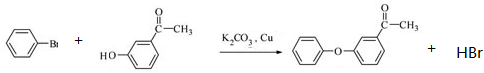 .
.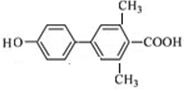 、
、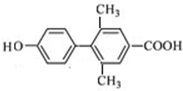 、
、 、
、 (其中一种).
(其中一种).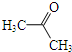 为原料制备
为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: →CH3-CHO+H2O
→CH3-CHO+H2O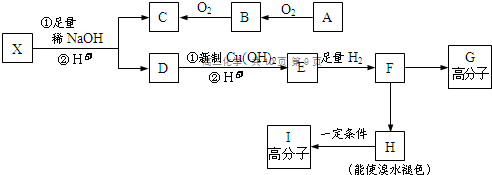
 ;F→H的反应类型是消去反应.
;F→H的反应类型是消去反应. .
. .
. .
.