0 16634 16642 16648 16652 16658 16660 16664 16670 16672 16678 16684 16688 16690 16694 16700 16702 16708 16712 16714 16718 16720 16724 16726 16728 16729 16730 16732 16733 16734 16736 16738 16742 16744 16748 16750 16754 16760 16762 16768 16772 16774 16778 16784 16790 16792 16798 16802 16804 16810 16814 16820 16828 203614

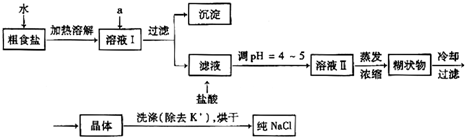
 (2008?海南)如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.
(2008?海南)如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.
 CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O