11.下列有关(NH4)2SO3溶液的叙述正确的是( )
| A. | 该溶液中,Na+、Fe3+、NO3-、Cl-可能大量共存 | |
| B. | 和溴水反应的离子方程式:Br2+SO32-+H2O=2H++2Br-+SO42- | |
| C. | 和Ba(OH)2溶液加热反应的离子方程式:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 1L0.1mol•L-1该溶液和足量的硝酸充分反应,生成2.24L(标准状况)SO2气体 |
10. 苯甲酸叶醇酯存在于麝香、百合和水仙花中,可用于高档香水的香精配方中,留香时间超过两周,其结构简式如图所示,下列关于苯甲酸叶醇酯的说法中错误的是( )
苯甲酸叶醇酯存在于麝香、百合和水仙花中,可用于高档香水的香精配方中,留香时间超过两周,其结构简式如图所示,下列关于苯甲酸叶醇酯的说法中错误的是( )
 苯甲酸叶醇酯存在于麝香、百合和水仙花中,可用于高档香水的香精配方中,留香时间超过两周,其结构简式如图所示,下列关于苯甲酸叶醇酯的说法中错误的是( )
苯甲酸叶醇酯存在于麝香、百合和水仙花中,可用于高档香水的香精配方中,留香时间超过两周,其结构简式如图所示,下列关于苯甲酸叶醇酯的说法中错误的是( )| A. | 苯甲酸叶醇酯能发生氧化反应 | |
| B. | 苯甲本叶醇酯能使溴的四氯化碳溶液褪色 | |
| C. | 1mol苯甲酸叶醇酯最多能与4molH2发生加成反应 | |
| D. | 1mol苯甲酸叶醇酯与NaOH溶液反应时,能消耗2molNaOH |
9.下列说法不正确的是( )
| A. | 二氯丙烷有三种同分异构体 | |
| B. | 碳酸氢钠可用作食品加工中的无铝发泡剂,快速发酵粉 | |
| C. | 二氧化碳制全降解塑料有助于控制温室效应和白色污染 | |
| D. | 某化合物的分子式为C8H10O,其中能与乙酸发生酯化反应的同分异构体有4种 |
8. 利用硫酸工业尾气中的二氧化硫可以制取氮肥硫酸铵.某探究小组设计实验对制得硫酸铵的品质进行鉴定.
利用硫酸工业尾气中的二氧化硫可以制取氮肥硫酸铵.某探究小组设计实验对制得硫酸铵的品质进行鉴定.
【查阅资料】硫酸铵化肥品质的束腰指标如表:
【观察外观】该硫酸铵化肥无可见机械杂质.
实验一:气体法测定含氮量.(实验装置如图1所示)
(1)烧瓶内发生反应的离子方程式为:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O;烧杯中盛放的试剂最好是稀硫酸(填“浓硫酸”、“稀硫酸”或“水”)
(2)甲同认为根据此实验测得的数据,计算硫酸铵化肥的含氮量可能偏高,因为实验装置中存在一个明显缺陷是:A、B装置间缺一个干燥装置.针对甲同学指出的缺陷,他们改进了实验装置,重新进行实验,准确测得氢气的质量.
实验二:甲醛法测定含氮量.
已知:①甲醛结构简式为HCHO,在空气中易被氧化成甲酸,甲酸酸性比乙醛强.
②甲醛法的反应原理为:4NH4++6HCHO→4H++6H2O+(CH2)6N4生成的酸再用NaOH标准溶液滴定,从而测定氮的含量.
(1)实验步骤:称取固体(NH4)2SO4样品0.600g于烧杯中,加入约30mL蒸馏水溶解,最终配成100mL溶液,用②(填图2中仪器编号)滴定管准确取出20.00mL的溶液与锥形瓶中,加入18%中性甲醛溶液5mL,放置5min后,加入1~2滴指示剂(已知滴定终点的pH约为8.8),用浓度为0.1000mol•L-1 NaOH标准溶液滴定,读数如表:
(2)探究结论,该化肥是(填“是”或“不是”)一等品.
(3)若滴定前待测也加甲醛后露置空气时间过长,则所测定的含氮量比实际值偏大(填“偏大”“偏小”或“无影响”).
实验三:测定碳酸氢铵中的含氮量
碳酸氢铵也是常用的氮肥,如果测定其含氮量,应选择的方法是气体法(填“气体法”或“甲醛法”),不选择另一种方法的理由是甲醛法用氢氧化钠标准溶液滴定时,溶液中HCO3-中的H+也会和氢氧化钠中和.
 利用硫酸工业尾气中的二氧化硫可以制取氮肥硫酸铵.某探究小组设计实验对制得硫酸铵的品质进行鉴定.
利用硫酸工业尾气中的二氧化硫可以制取氮肥硫酸铵.某探究小组设计实验对制得硫酸铵的品质进行鉴定.【查阅资料】硫酸铵化肥品质的束腰指标如表:
| 指标 项目 | 优等品 | 一等品 | 合格品 |
| 外观 | 白色结晶,无可见机械杂质 | 无可见机械杂质 | |
| 氮(N)含量 | ≥21.0% | ≥21.0% | ≥20.5% |
实验一:气体法测定含氮量.(实验装置如图1所示)
(1)烧瓶内发生反应的离子方程式为:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O;烧杯中盛放的试剂最好是稀硫酸(填“浓硫酸”、“稀硫酸”或“水”)
(2)甲同认为根据此实验测得的数据,计算硫酸铵化肥的含氮量可能偏高,因为实验装置中存在一个明显缺陷是:A、B装置间缺一个干燥装置.针对甲同学指出的缺陷,他们改进了实验装置,重新进行实验,准确测得氢气的质量.
实验二:甲醛法测定含氮量.
已知:①甲醛结构简式为HCHO,在空气中易被氧化成甲酸,甲酸酸性比乙醛强.
②甲醛法的反应原理为:4NH4++6HCHO→4H++6H2O+(CH2)6N4生成的酸再用NaOH标准溶液滴定,从而测定氮的含量.
(1)实验步骤:称取固体(NH4)2SO4样品0.600g于烧杯中,加入约30mL蒸馏水溶解,最终配成100mL溶液,用②(填图2中仪器编号)滴定管准确取出20.00mL的溶液与锥形瓶中,加入18%中性甲醛溶液5mL,放置5min后,加入1~2滴指示剂(已知滴定终点的pH约为8.8),用浓度为0.1000mol•L-1 NaOH标准溶液滴定,读数如表:
| 滴定次数 | 滴定前读数/mL | 滴定后读数/mL |
| 1 | 1.20 | 18.91 |
| 2 | 0.00 | 18.60 |
| 3 | 1.10 | 18.79 |
(3)若滴定前待测也加甲醛后露置空气时间过长,则所测定的含氮量比实际值偏大(填“偏大”“偏小”或“无影响”).
实验三:测定碳酸氢铵中的含氮量
碳酸氢铵也是常用的氮肥,如果测定其含氮量,应选择的方法是气体法(填“气体法”或“甲醛法”),不选择另一种方法的理由是甲醛法用氢氧化钠标准溶液滴定时,溶液中HCO3-中的H+也会和氢氧化钠中和.
6.25℃时,将Na2O2逐渐加入1L含有HCl、AlCl3、MgCl2的混合溶液中,产生沉淀和气体的量与加入Na2O2的量的关系如图所示(假设整个过程中溶液条件变化忽略不计).下列说法错误的是( )
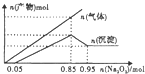

| A. | 混合溶液中m(Al3+)为5.4g | B. | 混合溶液中c(Mg2+)为0.5mol/L | ||
| C. | 混合溶液的pH=2 | D. | 混合溶液中c(Cl-)为1.7mol/L |
5.已知25℃时有关弱酸的电离平衡常数如下表:
下列关于Na2CO3溶液说法不正确的是( )
| 弱酸化学式 | HCN | H2CO3 |
| 电离平衡常数(25℃) | 4.9×10-10 | K1=4.3×10-7K2=5.6×10-11 |
| A. | Na2CO3溶液中滴入等体积、等浓度的盐酸后,溶液中一定存在:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(Cl-)+c(OH-) | |
| B. | Na2CO3溶液中通一定量的CO2气体后,溶液中一定存在:c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-) | |
| C. | Na2CO3溶液加水稀释后,c(H+)增大 | |
| D. | Na2CO3溶液中加入过量HCN,反应方程式为:Na2CO3+HCN=NaHCO3+NaCN |
4.下列说法或解释正确的是( )
| A. | 硅胶作干燥剂是利用其多孔、吸附水分的能力强 | |
| B. | 铝在空气中必须出良好的抗腐蚀性,说明铝极难与氧气反应 | |
| C. | 明矾可用于饮水的消毒杀菌 | |
| D. | 光导纤维比普通电缆有更强的传输信息能力,是因为其导电能力强 |
3.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1mol Na2O和Na2O2的混合物中,阴阳离子总数为3NA | |
| B. | 非标准状况下,NA个CO2分子所占的条件不可能为22.4L | |
| C. | 24.4gNa2O•SiO2中含有0.2NA个SiO2分子 | |
| D. | 56gFe投入1000mL3.5mol•L-1稀硝酸中,充分反应,转移电子总数为3NA |
2.下列离子或分子在溶液中能大量共存,且满足相应要求的是( )
0 167023 167031 167037 167041 167047 167049 167053 167059 167061 167067 167073 167077 167079 167083 167089 167091 167097 167101 167103 167107 167109 167113 167115 167117 167118 167119 167121 167122 167123 167125 167127 167131 167133 167137 167139 167143 167149 167151 167157 167161 167163 167167 167173 167179 167181 167187 167191 167193 167199 167203 167209 167217 203614
| 选项 | 离子或分子 | 要求 |
| A | Mg2+、SO42-、Cl-、NO3- | c(Mg2+)=c(SO42-) |
| B | Na+、Cu2+、I-、NH3•H2O | 在酸性高锰酸钾溶液中 |
| C | NH4+、Al3+、Cl-、NO3- | 滴加氨水有沉淀产生 |
| D | Cl-、Na+、Cr2O72-、C2H5OH | 溶液无色透明且遇甲基橙显红色 |
| A. | A | B. | B | C. | C | D. | D |
 周期表中有A、B、C三种原子序数依次增大的元素,A是地壳中含量最多的金属元素,B的价层电子排布为nsn-1npn+1,C是生活中的一种常用金属且其原子的外围电子排布为3d104s1.
周期表中有A、B、C三种原子序数依次增大的元素,A是地壳中含量最多的金属元素,B的价层电子排布为nsn-1npn+1,C是生活中的一种常用金属且其原子的外围电子排布为3d104s1.