15.X和Y属于短周期元素,X原子的最外层电子数是次外层电子数的一半,Y位于X的前一周期,且最外层只有一个电子,下列的说法正确的是( )
| A. | X可能是第二周期非金属元素 | B. | X可能是第三周期金属元素 | ||
| C. | Y可能与X同主族 | D. | Y可能是金属元素 |
14.类推的思维方式在化学学习与研究中经常采用,但类推出的结论是否正确要经过实验的验证,以下类推的结论正确的是( )
| A. | 由“Cl2+H2O═HCl+HClO”可推出“Br2+H2O═HBr+HBrO”也能发生 | |
| B. | Na与水反应生成NaOH和H2,故所有碱金属与水反应都能生成对应的碱和H2 | |
| C. | HCl的水溶液是强酸,推出HF的水溶液也是强酸 | |
| D. | 由“2Fe+3Cl2═2FeCl3”反应可推出“2Fe+3I2═2FeI3”反应也能发生 |
13.下表是部分短周期元素的原子半径及主要化合价,根据表中信息判断正确的是以下叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的沸点为H2T<H2R | |
| B. | M和T形成的化合物既能与强酸反应又能与强碱反应 | |
| C. | 单质与等浓度的稀盐酸反应的剧烈程度为Q>L | |
| D. | L2+与R2-的核外电子数相等 |
12.下列实验中,不能观察到明显变化的是( )
| A. | 把Cl2通入FeCl2溶液中 | |
| B. | 把一段打磨过的镁带放入少量冷水中 | |
| C. | 把绿豆大的钾投入少量水中 | |
| D. | 把溴水滴加到淀粉KI溶液中 |
11.下列判断错误的是( )
| A. | 沸点:HI>HBr>HCl>HF | |
| B. | 稳定性:NH3>PH3>AsH3(As与N位于同一主族) | |
| C. | 酸性:HClO4>H2SO4>H3PO4 | |
| D. | 碱性:NaOH>Mg(OH)2>Be(OH)2 |
10.用NA表示阿伏加德罗常数的值,下列有关物质结构中的说法正确的是( )
| A. | 78g Na2O2固体中所含阴阳离子个数均为2NA | |
| B. | 1.5g CH3+中含有的电子数为0.9NA | |
| C. | 3.4g氨气中含0.6NA个N-H键 | |
| D. | PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构 |
9.下列说法中正确的是( )
| A. | HCl中存在离子键,属于离子化合物 | |
| B. | KOH中含有离子键也含有共价键,属于离子化合物 | |
| C. | 阴阳离子通过静电引力而形成的化学键称为离子键 | |
| D. | 非金属元素组成的化合物中只含共价键 |
8.根据化学反应的实质是旧键断裂、新键形成的观点,下列变化没有发生化学键断裂的是( )
| A. | 电解水 | B. | 干冰受热直接变成气体 | ||
| C. | HCl溶解于水 | D. | 打雷放电时,O2变成O3 |
7.下列各项中表达正确的是( )
| A. | NH3分子的电子式: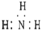 | B. | CH4分子的比例模型: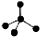 | ||
| C. | O原子的结构示意图: | D. | N2的结构式:N≡N |
6.下列有关原子结构的说法,正确的是( )
0 166988 166996 167002 167006 167012 167014 167018 167024 167026 167032 167038 167042 167044 167048 167054 167056 167062 167066 167068 167072 167074 167078 167080 167082 167083 167084 167086 167087 167088 167090 167092 167096 167098 167102 167104 167108 167114 167116 167122 167126 167128 167132 167138 167144 167146 167152 167156 167158 167164 167168 167174 167182 203614
| A. | 稀有气体元素原子的最外层电子数都是8 | |
| B. | 非金属元素的最外层电子数都大于3 | |
| C. | 金属元素的最外层电子数不都小于4 | |
| D. | 所有原子核都是由质子和中子构成的 |