8.化合物A、B是中学常见的物质,其阴阳离子可从下表中选择
(1)若A的水溶液为酸性,往B的水溶液加Al有气体产生,A、B的水溶液混合后,只产生不溶于稀硝酸的白色沉淀,①B的化学式为Ba(OH)2;
②A、B溶液混合后加热能产生气体的反应的离子方程式为H++SO42-+NH4++Ba2++2OH-$\frac{\underline{\;\;△\;\;}}{\;}$BaSO4↓+NH3↑+2H2O.
(2)若A的水溶液为浅绿色,B的焰色反应呈黄色.向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合后无明显变化.则
①A为FeI2;
②经分析上述过程中溶液变黄的原因可能有两种:
I仅有I-被氧化成I2使溶液呈黄色ⅡI-、Fe2+均被氧化使溶液呈黄色;
③请用一简易方法证明上述溶液变黄的原因取少量变黄溶液于试管中,滴加几滴KSCN溶液,若变红则Ⅱ合理,否则Ⅰ合理.
| 阳离子 | K+ Na+ NH+4 Fe2+ Ba2+ Cu2+ |
| 阴离子 | OH- I- NO3- AlO2- HCO3- HSO4- |
②A、B溶液混合后加热能产生气体的反应的离子方程式为H++SO42-+NH4++Ba2++2OH-$\frac{\underline{\;\;△\;\;}}{\;}$BaSO4↓+NH3↑+2H2O.
(2)若A的水溶液为浅绿色,B的焰色反应呈黄色.向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合后无明显变化.则
①A为FeI2;
②经分析上述过程中溶液变黄的原因可能有两种:
I仅有I-被氧化成I2使溶液呈黄色ⅡI-、Fe2+均被氧化使溶液呈黄色;
③请用一简易方法证明上述溶液变黄的原因取少量变黄溶液于试管中,滴加几滴KSCN溶液,若变红则Ⅱ合理,否则Ⅰ合理.
6.下列说法正确的是( )
| A. | 按系统命名法,有机物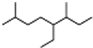 可命名为3,7-二甲基-4-乙基辛烷 可命名为3,7-二甲基-4-乙基辛烷 | |
| B. | 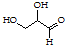 该有机物属于单糖,在一定条件下能发生取代、消去、加成、氧化、还原反应 该有机物属于单糖,在一定条件下能发生取代、消去、加成、氧化、还原反应 | |
| C. | 等质量的甲烷、乙烯、1,3-丁二烯分别充分燃烧,所耗用氧气的量依次增加 | |
| D. | 结构为…-CH=CH-CH=CH-CH=CH-CH=CH-…的高分子的单体是1,3-丁二烯 |
5.有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族; X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料.下列说法中,正确的是( )
| A. | X、M两种元素只能形成X2M型化合物 | |
| B. | 元素W和M的某些单质可作为水处理中的消毒剂 | |
| C. | 元素Y、Z、W的单质晶体属于同种类型的晶体 | |
| D. | 由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低 |
4.下列有关实验的操作与现象描述及相关结论正确的是( )
| A. | 向无水乙醇中加入浓H2SO4,加热至170°C产生的气体通入酸性KMnO4溶液,红色褪去,证明生成的气体全部是乙烯 | |
| B. | 润洗酸式滴定管时应从滴定管上口加入3~5mL所要盛装的酸溶液,倾斜着转动滴定管,使液体润湿其内壁,再从上口倒出,重复2~3次 | |
| C. | 某些强氧化剂如氯酸钾、硝酸钾等或其混合物不能研磨,否则可能引起爆炸 | |
| D. | 取5mL0.1mol•L-1KI溶液,滴加0.1mol•L-1FeCl3溶液5~6滴,继续加入2mLCCl4,充分振荡后静置,取上层溶液加KSCN溶液,无明显现象 |
3.下列说法不正确的是( )
| A. | 126C、136C、146C为碳元素的三种核素.元素周期表中碳的相对原子质量为12.01,说明自然界中的碳主要以126C的核素形式存在 | |
| B. | 汽车尾气催化转化装置可将尾气中的NO和CO等有害气体转化为N2和CO2,该装置中的催化剂可降低NO和CO反应的活化能,加快该反应的速率,却不能提高该反应的平衡转化率 | |
| C. | 人们通常用标准燃烧热或热值来衡量燃料燃烧放出热量的大小,某物质的热值越高则其标准燃烧热越大 | |
| D. | 绿色荧光蛋白在研究癌症发病机制的过程中应用突出,但其在酸性或碱性条件下可能会失去发光功能 |
1.某溶液中含有的离子是K+、NH4+、Fe2+、Fe3+、A13+、AlO2-、SO42-、CO32-、SiO32-、Cl-、NO3-中的某几种,已知各微粒的浓度均为0.1mol•L-1.现进行如下实验:
①取少量溶液加入足量的NaOH浓溶液,最终得到红褐色沉淀,并伴有气泡产生,过滤后的滤液中逐滴滴加稀硫酸至过量,过程中无沉淀产生.
②另取少量原溶液,加入稀硫酸溶液,有气体产生,并在空气中变为红色.
根据上述实验事实推断,有关该溶液的说法错误的是( )
①取少量溶液加入足量的NaOH浓溶液,最终得到红褐色沉淀,并伴有气泡产生,过滤后的滤液中逐滴滴加稀硫酸至过量,过程中无沉淀产生.
②另取少量原溶液,加入稀硫酸溶液,有气体产生,并在空气中变为红色.
根据上述实验事实推断,有关该溶液的说法错误的是( )
| A. | 至少含有4种离子 | |
| B. | 取少量原溶液先加入盐酸,后加入BaCl2溶液,肯定会产生白色沉淀 | |
| C. | 若原溶液中加入硝酸酸化的硝酸银溶液产生白色沉淀,则可推断溶液中含有K+ | |
| D. | 溶液中可能含有Fe3+、NH4+、SO42-、Cl-、NO3- |
20.下列说法正确的是( )
| A. | 氯化钴溶液中存在平衡,[Co(H2O)6]2+(粉红色)+4Cl-?[CoCl4]2-(蓝色)+6H2O△H=akJ•mol-1,将氯化钴溶液置于冰水浴,溶液变成粉红色,则可知:a<0 | |
| B. | 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 | |
| C. | 为了减小中和滴定的误差,锥形瓶必需洗净并烘干后才能使用 | |
| D. | 物质的分离提纯方法之一为“筛分”:如胶体-半透膜法分离提纯;悬浊液-过滤分离,本质上就是依据所分离粒子的直径大小选择具有合适孔径的“筛子” |
19.运用相关化学知识进行判断,下列结论正确的是( )
0 166913 166921 166927 166931 166937 166939 166943 166949 166951 166957 166963 166967 166969 166973 166979 166981 166987 166991 166993 166997 166999 167003 167005 167007 167008 167009 167011 167012 167013 167015 167017 167021 167023 167027 167029 167033 167039 167041 167047 167051 167053 167057 167063 167069 167071 167077 167081 167083 167089 167093 167099 167107 203614
| A. | PM2.5表示每立方米空气中直径小于或等于2.5μm的颗粒物的含量,PM2.5值越高,大气污染越严重,因此由PM2.5引起的雾霾一定属于胶体 | |
| B. | 分光光度计可用于分析溶液颜色与反应物(或生成物)浓度的关系,从而确定化学反应速率 | |
| C. | 对“地沟油”加工处理可以达到变废为宝的目的,比如对“地沟油”进行分馏可以制得汽油、煤油 | |
| D. | 次氯酸和臭氧都是强氧化剂,都能杀死水中的细菌.自来水常用氯气来杀菌消毒,是因为氯气杀菌消毒效果要比臭氧好,且不会残留有毒、有害物质 |
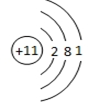 ,G在元素周期表中的位置为第三周期第ⅤⅡA族.
,G在元素周期表中的位置为第三周期第ⅤⅡA族. 写出B的化学式Fe2O3
写出B的化学式Fe2O3