12. 氯碱工业中离子交换膜电解槽示意图如下图,其中的离子交换膜为“阳离子交换膜”,它有一特殊的性质:只允许阳离子通过,而阻止阴离子和气体通过.下列说法正确的是( )
氯碱工业中离子交换膜电解槽示意图如下图,其中的离子交换膜为“阳离子交换膜”,它有一特殊的性质:只允许阳离子通过,而阻止阴离子和气体通过.下列说法正确的是( )
 氯碱工业中离子交换膜电解槽示意图如下图,其中的离子交换膜为“阳离子交换膜”,它有一特殊的性质:只允许阳离子通过,而阻止阴离子和气体通过.下列说法正确的是( )
氯碱工业中离子交换膜电解槽示意图如下图,其中的离子交换膜为“阳离子交换膜”,它有一特殊的性质:只允许阳离子通过,而阻止阴离子和气体通过.下列说法正确的是( )| A. | e口流入的是精制食盐水;f口流入的是蒸馏水 | |
| B. | a口流出的是稀食盐水,d口流出的是氢氧化钠溶液 | |
| C. | b为氯气,c为氧气 | |
| D. | b与a口流出的溶液可制得漂白液 |
10.下列有关溶液的叙述错误的是( )
| A. | pH相同的①CH3COONa、②NaHCO3、③NaAlO2溶液中c(Na+):③>②>① | |
| B. | 将0.2mol•L-1NaHCO3溶液与0.1mol•L-1KOH溶液等体积混合:3c(K+)+c(H+)═c(OH-)+c(HCO3-)+2c(CO32-) | |
| C. | 常温下,在pH=3的CH3COOH溶液和pH=11的NaOH溶液中,水的电离程度相同 | |
| D. | 向AgCl和AgBr的等体积饱和溶液中加入足量AgNO3溶液,则AgCl沉淀多于AgBr沉淀 |
9.如图是将SO2转化为重要的化工原料H2SO4的原理示意图,下列说法不正确的是( )

| A. | 该装置将化学能转化为电能 | |
| B. | 催化剂b表面O2发生还原反应,其附近酸性增强 | |
| C. | 催化剂a表面的反应是:SO2+2H2O-2e-═SO42-+4H+ | |
| D. | 若通入的H2O和SO2比例合适,得到的硫酸质量分数可能仍为49% |
8.工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.下列说法不正确的是( )
已知:放电顺序:Ni2+(高浓度)>H+>Ni2+(低浓度)

已知:放电顺序:Ni2+(高浓度)>H+>Ni2+(低浓度)
| A. | 碳棒上发生的电极反应:4OH--4e-═O2↑+2H2O | |
| B. | 为了提高Ni的产率,电解过程中需要控制废水pH | |
| C. | 电解过程中,B中NaCl溶液的物质的量浓度将不断增大 | |
| D. | 若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式不会发生改变 |
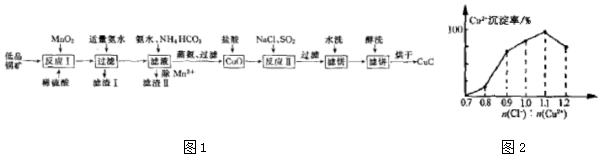
7.碳酸锶( SrCO3)可、作磁、材料、电子元件和焰火材料等.以天青石(主要成分为SrSO4,含有少量BaCO3.FeO.Fe2O3、Al2O3、SiO2等)为原料制备SrCO3的工艺流程如图1:

已知:
回答下列问题:
(I)写出一条能加快“浸取转化”反应速率的措施:升高温度增大纯碱浓度;滤液1的主要成分为Na2SO4(填化学式).
(2)加入HC1、HNO3混酸溶解后,所得溶液中阳离子共有5种;滤渣1的主要成分为SiO2(填化学式).
(3)“除钡”过程中硫酸过多会导致锶元素的损失.若除钡后所得溶液(M)中c(Ba2+)=1.0×10-5mol•L-1,要使锶元素不损失,则M中c(Sr2+)应不超过0.029mol•L-1(计算结果保留2位有效数字).
(4)“沉锶”生成SrCO3的离子方程式为Sr2++2HCO3-=SrCO3+H2O+CO2↑.“沉锶”过程中锶的转化率随温度变化如图2所示,60℃之前,锶的转化率随温度升高而变大的主要原因是升温有利于二氧化碳逸出有利于SrCO3生成.
(5)以SrCO3粉作原料经高温焙烧分解成SrO,再将SrO与铝粉充分混合并压制,真空环境下通过热还原反应可制得金属Sr,同时获得3SrO•Al2O3渣团.请写出热还原反应的化学方程式6SrO+2Al$\frac{\underline{\;高温\;}}{\;}$2Sr+3SrO•Al2O3.

已知:
| SrSO4 | BaSO4 | SrCO3 | |
| Ksp | 3.2×10-7 | 1.1×10-10 | 1.6×10-10 |
(I)写出一条能加快“浸取转化”反应速率的措施:升高温度增大纯碱浓度;滤液1的主要成分为Na2SO4(填化学式).
(2)加入HC1、HNO3混酸溶解后,所得溶液中阳离子共有5种;滤渣1的主要成分为SiO2(填化学式).
(3)“除钡”过程中硫酸过多会导致锶元素的损失.若除钡后所得溶液(M)中c(Ba2+)=1.0×10-5mol•L-1,要使锶元素不损失,则M中c(Sr2+)应不超过0.029mol•L-1(计算结果保留2位有效数字).
(4)“沉锶”生成SrCO3的离子方程式为Sr2++2HCO3-=SrCO3+H2O+CO2↑.“沉锶”过程中锶的转化率随温度变化如图2所示,60℃之前,锶的转化率随温度升高而变大的主要原因是升温有利于二氧化碳逸出有利于SrCO3生成.
(5)以SrCO3粉作原料经高温焙烧分解成SrO,再将SrO与铝粉充分混合并压制,真空环境下通过热还原反应可制得金属Sr,同时获得3SrO•Al2O3渣团.请写出热还原反应的化学方程式6SrO+2Al$\frac{\underline{\;高温\;}}{\;}$2Sr+3SrO•Al2O3.
6.湿法炼锌产生的铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质.一种由铜镉渣生产金属镉的流程如图:
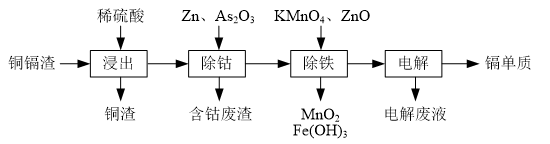
表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1mol•L-1计算):
(1)浸出过程中,不采用通入空气的方法进行搅拌,原因是防止将Cu氧化浸出,其离子方程式是2Cu+4H++O2=2Cu2++2H2O.
(2)除钴过程中,锌粉会与As2O3形成微电池产生AsH3.该微电池的正极反应式为As2O3+12H++12e-=2AsH3+3H2O.
(3)除铁时先加入适量KMnO4,再加入ZnO调节pH.
①除铁过程中,理论上参加反应的物质n(KMnO4):n(Fe2+)=1:3.
②除铁时加入ZnO控制反应液pH的范围为3.3~7.2.
(4)若上述流程中投入的KMnO4不足量,则待电解溶液中有Fe元素残余.请设计实验方案加以验证:取样,向其中滴加H2O2后再滴入KSCN溶液,若溶液变红(或向其中滴加K3[Fe(CN)6)]溶液,若产生蓝色沉淀),则待电解液中含有Fe元素.
(5)净化后的溶液用惰性电极电解可获得镉单质.电解废液中可循环利用的溶质是H2SO4.

表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1mol•L-1计算):
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.2 |
| 沉淀完全的pH | 3.3 | 9.9 | 9.5 |
(2)除钴过程中,锌粉会与As2O3形成微电池产生AsH3.该微电池的正极反应式为As2O3+12H++12e-=2AsH3+3H2O.
(3)除铁时先加入适量KMnO4,再加入ZnO调节pH.
①除铁过程中,理论上参加反应的物质n(KMnO4):n(Fe2+)=1:3.
②除铁时加入ZnO控制反应液pH的范围为3.3~7.2.
(4)若上述流程中投入的KMnO4不足量,则待电解溶液中有Fe元素残余.请设计实验方案加以验证:取样,向其中滴加H2O2后再滴入KSCN溶液,若溶液变红(或向其中滴加K3[Fe(CN)6)]溶液,若产生蓝色沉淀),则待电解液中含有Fe元素.
(5)净化后的溶液用惰性电极电解可获得镉单质.电解废液中可循环利用的溶质是H2SO4.
5.氯碱工业中电解饱和食盐水的原理示意图如图所示(电极均为石墨电极).下列说法正确的是( )

| A. | M为电子流出的一极 | |
| B. | 通电使氯化钠发生电离 | |
| C. | 电解一段时间后,阴极区pH降低 | |
| D. | 电解时用盐酸调节阳极区的pH在2~3,有利于气体逸出 |
4. 如图所示,a、b、c均为石墨电极,d为铁电极,通电进行电解.假设在电解过程中产生的气体全部逸出,下列说法正确的是( )
如图所示,a、b、c均为石墨电极,d为铁电极,通电进行电解.假设在电解过程中产生的气体全部逸出,下列说法正确的是( )
0 163843 163851 163857 163861 163867 163869 163873 163879 163881 163887 163893 163897 163899 163903 163909 163911 163917 163921 163923 163927 163929 163933 163935 163937 163938 163939 163941 163942 163943 163945 163947 163951 163953 163957 163959 163963 163969 163971 163977 163981 163983 163987 163993 163999 164001 164007 164011 164013 164019 164023 164029 164037 203614
 如图所示,a、b、c均为石墨电极,d为铁电极,通电进行电解.假设在电解过程中产生的气体全部逸出,下列说法正确的是( )
如图所示,a、b、c均为石墨电极,d为铁电极,通电进行电解.假设在电解过程中产生的气体全部逸出,下列说法正确的是( )| A. | 甲烧杯中溶液的pH降低 | |
| B. | 电解一段时间后,将甲、乙两溶液混合,一定会产生沉淀 | |
| C. | 当b极增重5.4g时,d极产生的气体为2.24L(标况) | |
| D. | 乙烧杯中的d电极反应式为Fe-2e-=Fe2+ |