12.下列金属氧化物的水化物碱性最强的是( )
| A. | CsOH | B. | Al(OH)3 | C. | NaOH | D. | Mg(OH)2 |
8.下表所列为五种短周期元素的相关信息:
回答下列问题:
(1)C元素在元素周期表中的位置为第二周期,第ⅤA族;
(2)B、D、E元素原子半径由大到小的顺序为Na>Al>Cl(填元素符号);
(3)A元素最高价氧化物的电子式为 ,含有的化学键类型为共价键;
,含有的化学键类型为共价键;
(4)工业上冶炼E的化学方程式为:2Al2O3$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑;
(5)下列说法正确的是AD(填选项字母).
A.简单氢化物稳定性:D>A B.最高价氧化物对应水化物的酸性:A>C
C.单质的还原性:E>B D.对应离子的氧化性:E>B.
| 元素 | 元素的相关信息 |
| A | A元素存在多种同素异形体,其中一种常用电极导电材料 |
| B | 短同期中金属性最强 |
| C | 单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
| E | 地壳中含量最多的金属 |
(1)C元素在元素周期表中的位置为第二周期,第ⅤA族;
(2)B、D、E元素原子半径由大到小的顺序为Na>Al>Cl(填元素符号);
(3)A元素最高价氧化物的电子式为
 ,含有的化学键类型为共价键;
,含有的化学键类型为共价键;(4)工业上冶炼E的化学方程式为:2Al2O3$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑;
(5)下列说法正确的是AD(填选项字母).
A.简单氢化物稳定性:D>A B.最高价氧化物对应水化物的酸性:A>C
C.单质的还原性:E>B D.对应离子的氧化性:E>B.
7.绿色化学提倡化工生产应提高原子利用率.原子利用率表示目标产物的质量与生成物总质量之比.下列制备乙醇的反应中,原子利用率最高的是( )
| A. | CH2═CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH | |
| B. | CH3CH2Br+NaOH$\stackrel{△}{→}$CH3CH2OH+NaBr | |
| C. | 2CO+4H2$\stackrel{一定条件}{?}$CH3CH2OH+H2O | |
| D. | CH3COOCH2CH3+NaOH$\stackrel{△}{→}$CH3CH2OH+CH3COONa |
6.用60g乙酸与92g乙醇的反应,实际得到乙酸乙酯的质量为52.8g,本实验的产率是( )
| A. | 30% | B. | 40% | C. | 60% | D. | 90% |
5.设NA表示阿伏加德罗常数,下列叙述不正确的是( )
| A. | 1mol羟基所含电子数为9NA | |
| B. | 常温、常压下,14g CO与N2的混合气含的原子数为NA | |
| C. | 标准状况下,22.4L CH3Cl所含原子数为5NA | |
| D. | 23gNa与足量H2O反应完全后可生成NA个H2分子 |
4.下列装置或操作能达到实验目的是( )


| A. | 图①所示实验能证明非金属性:S>C>Si | |
| B. | 图②装置可用于分离乙酸与乙醇的混合液 | |
| C. | 图③装置可以用来实验室制乙酸乙酯 | |
| D. | 图④装说可检验蔗糖是否水解 |
3.能通过化学反应使溴水褪色,又能使酸性髙锰酸钾褪色的是( )
0 163837 163845 163851 163855 163861 163863 163867 163873 163875 163881 163887 163891 163893 163897 163903 163905 163911 163915 163917 163921 163923 163927 163929 163931 163932 163933 163935 163936 163937 163939 163941 163945 163947 163951 163953 163957 163963 163965 163971 163975 163977 163981 163987 163993 163995 164001 164005 164007 164013 164017 164023 164031 203614
| A. | 苯 | B. | 乙烯 | C. | 乙醇 | D. | 乙酸 |

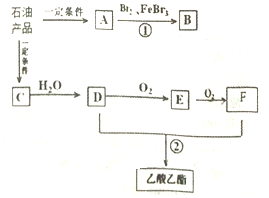 石油是一种重要的资源,其常压蒸馏的产品在一定条件下能转化为芳香烃.A-F均为有机化合物,C的产量可以用来衡量一个国家的石油化工发展水平.它们的转化关系如图所示(部分产物和反应条件已略去).
石油是一种重要的资源,其常压蒸馏的产品在一定条件下能转化为芳香烃.A-F均为有机化合物,C的产量可以用来衡量一个国家的石油化工发展水平.它们的转化关系如图所示(部分产物和反应条件已略去). ,反应类型为取代反应;
,反应类型为取代反应;