题目内容
4.下列装置或操作能达到实验目的是( )
| A. | 图①所示实验能证明非金属性:S>C>Si | |
| B. | 图②装置可用于分离乙酸与乙醇的混合液 | |
| C. | 图③装置可以用来实验室制乙酸乙酯 | |
| D. | 图④装说可检验蔗糖是否水解 |
分析 A.发生强酸制取弱酸的酸性,可知酸性为硫酸>碳酸>硅酸;
B.乙酸与乙醇互溶;
C.试管中导管在碳酸钠溶液的液面下,可发生倒吸;
D.检验葡萄糖应在碱性条件下.
解答 解:A.发生强酸制取弱酸的酸性,可知酸性为硫酸>碳酸>硅酸,则能证明非金属性:S>C>Si,故A正确;
B.乙酸与乙醇互溶,不能利用图中分液法分离,应选蒸馏法,故B错误;
C.试管中导管在碳酸钠溶液的液面下,可发生倒吸,为防止倒吸,导管口在液面上,故C错误;
D.检验葡萄糖应在碱性条件下,没有加碱至碱性,不能检验,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握非金属性比较、混合物分离提纯、有机物的制备和性质实验、实验装置的作用、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
14.在一定温度下向一个体积为2L固定容积的密闭容器中充入一定量的N2O4,进行如下化学反应:N2O4(g)?2NO2(g),请回答下列问题:
(1)下列说法能够判断该反应已经达到化学平衡状态的是BD.
A.容器内混合气体密度不变
B.混合气体的压强不变
C.0.5molN2O4分解的同时有1molNO2生成
D.混合气体的颜色不变
(2)每隔一段时间对该密闭容器内的物质进行分析,得到如下数据:
①b的值为0.16;
②达到化学平衡状态时,N2O4的平衡转化率为42.9%(或42.86%);
③20s~40s内用N2O4表示该反应的平均反应速率υ(N2O4)=0.01mol•L-1•s-1.
(1)下列说法能够判断该反应已经达到化学平衡状态的是BD.
A.容器内混合气体密度不变
B.混合气体的压强不变
C.0.5molN2O4分解的同时有1molNO2生成
D.混合气体的颜色不变
(2)每隔一段时间对该密闭容器内的物质进行分析,得到如下数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) (mol) | 2.80 | a | 2.00 | c | d | 1.60 |
| n(NO2) (mol) | 0 | 0.96 | b | 2.08 | 2.40 | 2.40 |
②达到化学平衡状态时,N2O4的平衡转化率为42.9%(或42.86%);
③20s~40s内用N2O4表示该反应的平均反应速率υ(N2O4)=0.01mol•L-1•s-1.
15.下列离子可以大量共存的是( )
| A. | Fe3+、Na+、I-、Cl- | B. | Al3+、NO3-、Cl-、K+ | ||
| C. | K+、H+、HCO3-、SO42- | D. | Cu2+、Na+、SO42-、Cl- |
12.某烃和溴水反应的产物为2,2,3,3-四溴丁烷,则该烃同分异构体为( )
| A. | 1-丁烯 | B. | 1-丁炔 | C. | 2-丁炔 | D. | 2-丁烯 |
19.下列叙述正确的是( )
| A. | 甲烷、乙烯中所有原子都在同一平面上 | |
| B. | 二氯甲烷只有一种结构 | |
| C. | C4H10的同分异构体有3种 | |
| D. | 淀粉和纤维素互为同分异构体 |
16.下列关于非金属元素的叙述正确的是( )
| A. | 非金属元素的原子最外层电子数都大于或等于4 | |
| B. | 非金属元素的原子都易得电子生成相应的阴离子 | |
| C. | 非金属单质都是气体 | |
| D. | 每一主族所包含的元素中不一定都有非金属元素 |
13.常温下,向100mL0.05mol/L氢硫酸中逐渐通入氯气.下列叙述正确的是( )
| A. | 溶液c(H+)先变大后变小 | |
| B. | 溶液导电能力逐渐增强 | |
| C. | 氢硫酸完全反应生成1.6g硫 | |
| D. | 反应的离子方程式为:S2-+Cl2→2Cl-+S↓ |
14.下列有机反应中,有一种反应类型与其他三种反应类型不同的是( )
| A. | CH3COOH+CH3CH2OH $\stackrel{催化剂}{?}$CH3COOCH2CH3+H2O | |
| B. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| C. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | |
| D. |  +Br2 $\stackrel{FeBr_{3}}{→}$ +Br2 $\stackrel{FeBr_{3}}{→}$ +HBr +HBr |
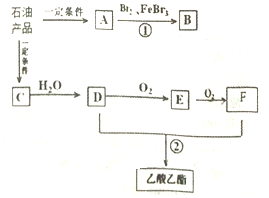 石油是一种重要的资源,其常压蒸馏的产品在一定条件下能转化为芳香烃.A-F均为有机化合物,C的产量可以用来衡量一个国家的石油化工发展水平.它们的转化关系如图所示(部分产物和反应条件已略去).
石油是一种重要的资源,其常压蒸馏的产品在一定条件下能转化为芳香烃.A-F均为有机化合物,C的产量可以用来衡量一个国家的石油化工发展水平.它们的转化关系如图所示(部分产物和反应条件已略去). ,反应类型为取代反应;
,反应类型为取代反应;