13.某有机物甲经氧化后最终得到乙(分子式为C2H3O2Cl);而甲经水解可得丙,1mol丙和2mol乙反应得一种含氯的酯(C6H8O4Cl2);由此推断甲的结构简式为( )
| A. | ClCH2CH2OH | B. | OHC-O-CH2Cl | C. | ClCH2CHO | D. | HOCH2CH2O |
10.(1)Al2(SO4)3溶液加热蒸干并灼烧最终得到物质是Al2(SO4)3(填化学式),将NaHCO3与Al2(SO4)3两者溶液混合后可做泡沫灭火剂,其原理是Al3++3HCO3-=Al(OH)3↓+3CO2↑(用离子方程式表示)
(2)实验室溶液中常用NaOH来进行洗气和提纯.当100mL 1mol•L-1的NaOH溶液吸收标准状况下2.24LSO2时,所得溶液中各离子浓度由大到小的顺序为c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-).
(3)25℃时,几种离子开始沉淀时的pH如下表:
当向含相同浓度Cu2+、Mg2+、Fe2+的溶液中滴加NaOH溶液时,Cu2+先沉淀(填离子符号),要使0.3mol•L-1硫酸铜溶液中Cu2+沉淀较为完全(当Cu2+浓度降至10-5 mol•L-1时),则应向溶液里加入氢氧化钠溶液使溶液pH为6.5(KspCu(OH)2=1×10-20)
(2)实验室溶液中常用NaOH来进行洗气和提纯.当100mL 1mol•L-1的NaOH溶液吸收标准状况下2.24LSO2时,所得溶液中各离子浓度由大到小的顺序为c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-).
(3)25℃时,几种离子开始沉淀时的pH如下表:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
8.向硝酸钠溶液中加入铜粉不发生反应,若加入某种盐,则铜粉可以逐渐溶解,符合此条件的盐是( )
| A. | Na2SO4 | B. | NaHCO3 | C. | NaHSO4 | D. | FeCl3 |
7.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 将0.5 mol NH4NO3溶于稀氨水中,溶液呈中性,溶液中NH4+的数目为0.5NA | |
| B. | 将0.2mol NH3充入密闭容器中,在一定条件下加热分解,生成N2的分子数为0.1NA | |
| C. | 足量的铜与50 mL 18 mol/L的浓硫酸在加热条件下反应时,转移的电子数为0.9NA | |
| D. | 标准状况下,8.96L平均相对分子质量为3.5g的H2与D2含有的中子数为0.3NA |
5.下列说法正确的是( )
0 163816 163824 163830 163834 163840 163842 163846 163852 163854 163860 163866 163870 163872 163876 163882 163884 163890 163894 163896 163900 163902 163906 163908 163910 163911 163912 163914 163915 163916 163918 163920 163924 163926 163930 163932 163936 163942 163944 163950 163954 163956 163960 163966 163972 163974 163980 163984 163986 163992 163996 164002 164010 203614
| A. | 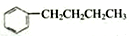 的与H2加成之后的产物中,其一氯代物有7种 的与H2加成之后的产物中,其一氯代物有7种 | |
| B. | CH3CH=CHCH3分子中的四个碳原子在同一直线上 | |
| C. | 按系统命名法,化合物 的名称是2,3,4-三甲基-2-乙基戊烷 的名称是2,3,4-三甲基-2-乙基戊烷 | |
| D. |  的一溴代物和 的一溴代物和  的一溴代物都有4种(不考虑立体异构) 的一溴代物都有4种(不考虑立体异构) |

 ; C2H4
; C2H4 .
. ③金刚石 ④35Cl ⑤
③金刚石 ④35Cl ⑤
 ⑦
⑦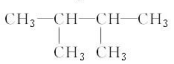 ⑧氯气 ⑨石墨 ⑩37Cl
⑧氯气 ⑨石墨 ⑩37Cl