20.从海带中提取碘单质,成熟的工艺流程如下,下列关于海水制碘的说法,不正确的是( )


| A. | 在碘水中加入 CCl4得到I2的CCl4溶液,该操作为“萃取” | |
| B. | 在含I-的滤液中加入稀硫酸和双氧水后,碘元素发生氧化反应 | |
| C. | 在碘水中加入几滴淀粉溶液,溶液变蓝色 | |
| D. | 实验室在蒸发皿中灼烧干海带,并且用玻璃棒搅拌 |
19. 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )| A. | 原子半径:r(W)>r(Z)>r(Y)>r(X) | |
| B. | Y元素的单质只能跟酸反应,不能跟碱反应 | |
| C. | 最简单气态氢化物的热稳定性:W>Z | |
| D. | W元素的各种氧化物对应的水化物均为强酸 |
18.氯气是一种重要的工业原料.工业上利用反应3Cl2+2NH3═N2+6HCl检查氯气管道是否漏气.下列说法错误的是( )
| A. | 若管道漏气遇氨就会产生白烟 | B. | 该反应利用了Cl2的强氧化性 | ||
| C. | 该反应属于置换反应 | D. | 生成1 mol N2有3 mol电子转移 |
17.230Th和232Th是钍的两种同位素,232Th可以转化成233U.下列有关Th的说法正确的是( )
| A. | 232Th和233U互为同素异形体 | B. | Th 元素的相对原子质量是231 | ||
| C. | 232Th 转换成233U是化学变化 | D. | 230Th和232Th的化学性质相同 |
16. 某温度下,向10mL0.1mol/LCuCl2溶液中滴加0.1mol/L的Na2S溶液,滴加过程中溶液中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,下列有关说法正确的是已知:lg2=0.3,Ksp(ZnS)=3×10-25mol2/L2.( )
某温度下,向10mL0.1mol/LCuCl2溶液中滴加0.1mol/L的Na2S溶液,滴加过程中溶液中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,下列有关说法正确的是已知:lg2=0.3,Ksp(ZnS)=3×10-25mol2/L2.( )
 某温度下,向10mL0.1mol/LCuCl2溶液中滴加0.1mol/L的Na2S溶液,滴加过程中溶液中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,下列有关说法正确的是已知:lg2=0.3,Ksp(ZnS)=3×10-25mol2/L2.( )
某温度下,向10mL0.1mol/LCuCl2溶液中滴加0.1mol/L的Na2S溶液,滴加过程中溶液中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,下列有关说法正确的是已知:lg2=0.3,Ksp(ZnS)=3×10-25mol2/L2.( )| A. | a、b、c三点中,水的电离程度最大的为b点 | |
| B. | Na2S溶液中:c(S2-)+c(HS-)+c(H2S)═2c(Na+) | |
| C. | 该温度下Ksp(CuS)=4×10-36 mol2/L2 | |
| D. | 向100 mLZn2+、Cu2+浓度均为10-5mol/L的混合溶液中逐滴加入10-4mol/L的Na2S溶液,Zn2+先沉淀 |
15. 有X、Y、Z、W、A、B六种元素.其相关信息如下:
有X、Y、Z、W、A、B六种元素.其相关信息如下:
请回答下列有关问题:
(1)根据信息分析元素Y是F(填元素符号),A在元素周期表中的位置是第四周期VIII.
(2)BX3分子的中心原子采取的杂化类型是sp3.
(3)光谱证实单质 Z与强碱溶液反应生成[Z(OH)4]-,该原子的空间构型是正四面体型,[Z(OH)4]-离子中存在的化学键有ACD (填字母)
A.极性共价键 B.非极性共价键 C.配位键 D.σ键 E.π键
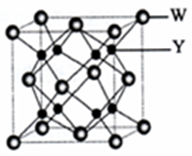
(4)Y与W可形成离子化合物,其晶胞结构如下图所示.W离子采取的堆枳方式是面心立方堆积,W离子的配位数为8,W离子的配位数为此空多余,Y离子占据空位四面体(填“四面体或八面体”).若该晶体的密度为dg•cm-3,则该晶胞中最近的Y离子与W离子间的距离是$\frac{\sqrt{3}}{4}$×$\root{3}{\frac{78×4}{{N}_{A}×d}}$cm,(设NA为阿佛加德罗常数的值,只需列出计算表达式)
 有X、Y、Z、W、A、B六种元素.其相关信息如下:
有X、Y、Z、W、A、B六种元素.其相关信息如下:请回答下列有关问题:
| 元素 | 相关信息 | ||||||||||||||
| X | X原子的1s轨道上只有1个电子 | ||||||||||||||
| Y | Y是周期表中电负性最大的元素 | ||||||||||||||
| Z | Z是第三周期主族元素,其电离能l1~l7如下表所示(单位:KJ/mol)
| ||||||||||||||
| W | W是主族元素且与A同周期,其最外电子层上有两个运动状态不同的电子 | ||||||||||||||
| A | A是过渡元素,其基态原子的外围电子排布图为: | ||||||||||||||
| B | B元素基态原子的2p轨道中有三个未成对的电子 |
(2)BX3分子的中心原子采取的杂化类型是sp3.
(3)光谱证实单质 Z与强碱溶液反应生成[Z(OH)4]-,该原子的空间构型是正四面体型,[Z(OH)4]-离子中存在的化学键有ACD (填字母)
A.极性共价键 B.非极性共价键 C.配位键 D.σ键 E.π键
(4)Y与W可形成离子化合物,其晶胞结构如下图所示.W离子采取的堆枳方式是面心立方堆积,W离子的配位数为8,W离子的配位数为此空多余,Y离子占据空位四面体(填“四面体或八面体”).若该晶体的密度为dg•cm-3,则该晶胞中最近的Y离子与W离子间的距离是$\frac{\sqrt{3}}{4}$×$\root{3}{\frac{78×4}{{N}_{A}×d}}$cm,(设NA为阿佛加德罗常数的值,只需列出计算表达式)
14. 非金属及其化合物在工农业生产、生活中有着重要应用,减少非金属的氧化物在大气中的排放是环境保护的重要内容之一.
非金属及其化合物在工农业生产、生活中有着重要应用,减少非金属的氧化物在大气中的排放是环境保护的重要内容之一.
(1)已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ•mol-1
C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-1
2C(s)+O2(g)=2CO(g)△H=-221kJ•mol-1
若某反应的平衡常数表达式为:K=$\frac{c({N}_{2})•{c}^{2}(C{O}_{2})}{c(NO)•{c}^{2}(CO)}$,请写出此反应的热化学方程式2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.5 kJ•mol-1.
(2)N2O5在一定条件下可发生分解:2N2O5(g)?4NO2(g)+O2(g).△H>0.某温度下测得恒容密闭容器中N2O5浓度随时间的变化如表:
反应开始时体系压强为P0,第3.00min时达到平衡体系压强为p1,则p1:p0=1.975;1.00min~3.00min内,O2的平均反应速率为0.09mol•L-1•min-1.从表中可知化学反应速率变化规律是随反应时间进行,反应物浓度降低,化学反应速率减少.
①该温度下反应的平衡常数Kp=$\frac{(1.3{P}_{0})^{4}×(0.325{P}_{0})}{(0.35{p}_{0})^{2}}$(用平衡分压代替平衡浓度计算,分压=总压×物质的量的分数,请列出用P0表示平衡常数表达式,不用计算).
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是a.
a.容器中压强不再变化 b.NO2和O2的体积比保持不变
c.2v正(NO2)=v逆(N2O5) d.混合气体的密度保持不变
(3)从N2O5可通过电解或臭氧氧化N2O4的方法制备.电解装置如图所示(隔膜用于阻止水分子通过),其阳极反应式为N2O4+2NO3--2e-=2N2O5.
 非金属及其化合物在工农业生产、生活中有着重要应用,减少非金属的氧化物在大气中的排放是环境保护的重要内容之一.
非金属及其化合物在工农业生产、生活中有着重要应用,减少非金属的氧化物在大气中的排放是环境保护的重要内容之一.(1)已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ•mol-1
C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-1
2C(s)+O2(g)=2CO(g)△H=-221kJ•mol-1
若某反应的平衡常数表达式为:K=$\frac{c({N}_{2})•{c}^{2}(C{O}_{2})}{c(NO)•{c}^{2}(CO)}$,请写出此反应的热化学方程式2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.5 kJ•mol-1.
(2)N2O5在一定条件下可发生分解:2N2O5(g)?4NO2(g)+O2(g).△H>0.某温度下测得恒容密闭容器中N2O5浓度随时间的变化如表:
| t/min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
| c(N2O5)/(mo•L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
①该温度下反应的平衡常数Kp=$\frac{(1.3{P}_{0})^{4}×(0.325{P}_{0})}{(0.35{p}_{0})^{2}}$(用平衡分压代替平衡浓度计算,分压=总压×物质的量的分数,请列出用P0表示平衡常数表达式,不用计算).
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是a.
a.容器中压强不再变化 b.NO2和O2的体积比保持不变
c.2v正(NO2)=v逆(N2O5) d.混合气体的密度保持不变
(3)从N2O5可通过电解或臭氧氧化N2O4的方法制备.电解装置如图所示(隔膜用于阻止水分子通过),其阳极反应式为N2O4+2NO3--2e-=2N2O5.
13. 25℃时,将0.0l mol•L-1 NaOH溶液滴入20mL0.01mol•L-1CH3COOH溶液的过程中,溶液中由水电离出的c(H+)与加入NaOH溶液体积的关系如图所示.下列说法正确的是( )
25℃时,将0.0l mol•L-1 NaOH溶液滴入20mL0.01mol•L-1CH3COOH溶液的过程中,溶液中由水电离出的c(H+)与加入NaOH溶液体积的关系如图所示.下列说法正确的是( )
 25℃时,将0.0l mol•L-1 NaOH溶液滴入20mL0.01mol•L-1CH3COOH溶液的过程中,溶液中由水电离出的c(H+)与加入NaOH溶液体积的关系如图所示.下列说法正确的是( )
25℃时,将0.0l mol•L-1 NaOH溶液滴入20mL0.01mol•L-1CH3COOH溶液的过程中,溶液中由水电离出的c(H+)与加入NaOH溶液体积的关系如图所示.下列说法正确的是( )| A. | x=20,a点的纵坐标为1.0×10-12 | |
| B. | b点和d点所示溶液的pH相等 | |
| C. | 滴定过程中,c(CH3COO-)与c(OH-)的比值逐渐增大 | |
| D. | e点所示溶液中,c(Na+)=2c(CH3COO-)+2c(CH3COOH) |
12.在微生物作用下电解有机废水(含CH3COOH ),可获得清洁能源H2.其原理如图所示.不正确的是( )

| A. | 通电后,H+通过质子交换膜向右移动,最终右侧溶液pH减小 | |
| B. | 电源B极为负极 | |
| C. | 与电源A极相连的惰性电极上发生的反应为CH3COOH-8e-+2H2O═2CO2↑+8H+ | |
| D. | 通电后,若有0.1molH2生成,则转移0.2 mol 电子 |
11.下列说法正确的是A( )
0 163672 163680 163686 163690 163696 163698 163702 163708 163710 163716 163722 163726 163728 163732 163738 163740 163746 163750 163752 163756 163758 163762 163764 163766 163767 163768 163770 163771 163772 163774 163776 163780 163782 163786 163788 163792 163798 163800 163806 163810 163812 163816 163822 163828 163830 163836 163840 163842 163848 163852 163858 163866 203614
| A. | 电解质与非电解质的本质区别,是在水溶液或熔化状态下能否电离 | |
| B. | SO2水溶液能导电性,SO2是电解质,BaSO4水溶液不导电是非电解质 | |
| C. | 酸、碱和盐类都属于电解质,其他化合物都是非电解质 | |
| D. | Cu能导电所以Cu是电解质 |