13.下列离子方程式书写正确的是( )
| A. | 烧碱溶液与小苏打溶液反应:OH-+HCO3-═H2O+CO2↑ | |
| B. | 铝粉与烧碱溶液反应:2Al+2OH-+H2O═2AlO2-+2H2↑ | |
| C. | 氢氧化铝与氢溴酸 Al(OH)3+3HBr═Al3++3H2O | |
| D. | 过量CO2通入漂白粉溶液中 CO2+H2O+ClO-═HCO3-+HClO |
12.据报道,摩托罗拉公司开发的一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可持续使用一个月.关于该电池的叙述正确的是( )
| A. | 放电时,正极反应为式:O2+4e-+4H+═2H2O | |
| B. | 放电时,负极反应为式:CH3OH-6e-+8OH-═CO32-+6H2O | |
| C. | 充电时,原电池的负极与电源的正极相连接 | |
| D. | 充电时,阴极反应式为:4OH--4e-═2H2O+O2↑ |
11.下列实验设计正确的是( )
| A. | 将SO2通入溴水中证明SO2具有漂白性 | |
| B. | 用向上排空气法收集铜粉与稀硝酸反应产生的NO | |
| C. | 将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 | |
| D. | 将乙烯通入KMnO4酸性溶液证明乙烯具有还原性 |
10.正确掌握化学用语是学好化学的基础,下列有关表述正确的是( )
| A. | H、D、T互为同素异形体 | B. | 质量数为31的磷原子:${\;}_{15}^{31}$P | ||
| C. | 次氯酸的电子式: | D. | 乙烯的结构简式是:CH2CH2 |
9. 近年来甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途径多种多样.现有实验室中模拟甲醇合成反应,在2L密闭容器内,400℃时反应:CO(g)+2H2(g)?CH3OH(g)△H<0,体系中n(CO)随时间的变化如表:
近年来甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途径多种多样.现有实验室中模拟甲醇合成反应,在2L密闭容器内,400℃时反应:CO(g)+2H2(g)?CH3OH(g)△H<0,体系中n(CO)随时间的变化如表:
(1)图1中表示CH3OH的变化的曲线是b.
(2)用H2表示从0~2s内该反应的平均速率v(H2)=0.006mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是b c.
a.v(CH3OH)=2v(H2) b.容器内压强保持不变
c.2v逆(CO)=v正(H2) d.容器内密度保持不变
(4)已知常温常压下1g液态甲醇燃烧生成CO2气体和液态水放出22.68kJ的热量,则该反应的热化学方程式为:CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-725.76kJ•mol-1.
(5)CH3OH与O2的反应可将化学能转化为电能,其工作原理如图2所示,图中CH3OH从A(填A或B)通入,b极的电极反应式是O2+4e-+2H2O=4OH-.
 近年来甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途径多种多样.现有实验室中模拟甲醇合成反应,在2L密闭容器内,400℃时反应:CO(g)+2H2(g)?CH3OH(g)△H<0,体系中n(CO)随时间的变化如表:
近年来甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途径多种多样.现有实验室中模拟甲醇合成反应,在2L密闭容器内,400℃时反应:CO(g)+2H2(g)?CH3OH(g)△H<0,体系中n(CO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 5 |
| n(CO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 |
(2)用H2表示从0~2s内该反应的平均速率v(H2)=0.006mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是b c.
a.v(CH3OH)=2v(H2) b.容器内压强保持不变
c.2v逆(CO)=v正(H2) d.容器内密度保持不变
(4)已知常温常压下1g液态甲醇燃烧生成CO2气体和液态水放出22.68kJ的热量,则该反应的热化学方程式为:CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-725.76kJ•mol-1.
(5)CH3OH与O2的反应可将化学能转化为电能,其工作原理如图2所示,图中CH3OH从A(填A或B)通入,b极的电极反应式是O2+4e-+2H2O=4OH-.
8. 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )
 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )| A. | 苛性钾溶液中KOH的质量是16.8 | |
| B. | 反应中转移电子0.21mol | |
| C. | 氯气被还原成0.06molClO-和0.03molClO3- | |
| D. | ClO3-的生成是由于温度升高引起的 |
7.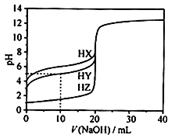 25℃时,用0.1000mol•L-1的NaOH溶液分别滴定20.00mL均为0.1000mol•L-1的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法错误的是( )
25℃时,用0.1000mol•L-1的NaOH溶液分别滴定20.00mL均为0.1000mol•L-1的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法错误的是( )
 25℃时,用0.1000mol•L-1的NaOH溶液分别滴定20.00mL均为0.1000mol•L-1的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法错误的是( )
25℃时,用0.1000mol•L-1的NaOH溶液分别滴定20.00mL均为0.1000mol•L-1的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法错误的是( )| A. | HZ是强酸,HX、HY是弱酸 | |
| B. | 根据滴定曲线,可得Ka(HY)≈10-5 | |
| C. | 将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+) | |
| D. | 将上述HY与HZ溶液等体积混合达到平衡时:C(H+)=c(OH-)=c(Z-)+c(Y-) |
6. 常温下,用0.05mol/LNaOH溶液分别滴定10.00mL浓度均为0.10mol/LCH3COOH( Ka=l×10-5)溶液HCN(Ka=5×10-10)溶液,所得滴定曲线如图.下列说法正确的是( )
常温下,用0.05mol/LNaOH溶液分别滴定10.00mL浓度均为0.10mol/LCH3COOH( Ka=l×10-5)溶液HCN(Ka=5×10-10)溶液,所得滴定曲线如图.下列说法正确的是( )
 常温下,用0.05mol/LNaOH溶液分别滴定10.00mL浓度均为0.10mol/LCH3COOH( Ka=l×10-5)溶液HCN(Ka=5×10-10)溶液,所得滴定曲线如图.下列说法正确的是( )
常温下,用0.05mol/LNaOH溶液分别滴定10.00mL浓度均为0.10mol/LCH3COOH( Ka=l×10-5)溶液HCN(Ka=5×10-10)溶液,所得滴定曲线如图.下列说法正确的是( )| A. | 对两种弱酸滴定均可选用甲基橙作指示剂 | |
| B. | ③处溶液有:c(Na+)=c(CH3COO-)<c(CH3COOH) | |
| C. | 溶液中水的电离程度:②>③>④ | |
| D. | 点①和点②溶液混合后:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH) |
5.常温时,将不同体积比的NH3和CO2的混合气体溶于水得到一系列混合溶液,溶液中部分微粒的分布分数f[f=$\frac{某含C(或N)微粒浓度}{所有含C(或N)微粒浓度总和}$]随pH的变化曲线如图所示:下列说法正确的是( )

0 163514 163522 163528 163532 163538 163540 163544 163550 163552 163558 163564 163568 163570 163574 163580 163582 163588 163592 163594 163598 163600 163604 163606 163608 163609 163610 163612 163613 163614 163616 163618 163622 163624 163628 163630 163634 163640 163642 163648 163652 163654 163658 163664 163670 163672 163678 163682 163684 163690 163694 163700 163708 203614

| A. | 当溶液pH=7时:c(NH4+)>c(H2CO3)+2c(CO32-) | |
| B. | 当溶液pH=9.5时:c(OH-)-c(H+)>c(NH4+)-3c(CO32-) | |
| C. | 若刚好是(NH4)2CO3溶液:c(OH-)+C(NH3•H2O)>c(H+)+c(H2CO3)+c(HCO3-) | |
| D. | 若刚好是NH4HCO3溶液,向其中加入等体积、等物质的量浓度的NaCl溶液,析出部分晶体,过滤所得的滤液中:c(Na+)=c(Cl-)>c(NH4+)>c(HCO3-)>c(CO32-) |
 NO、NO2 和CO均为大气污染物,对其治理备受关注.请回答下列问题:
NO、NO2 和CO均为大气污染物,对其治理备受关注.请回答下列问题: