1.Ⅰ、已知室温下,碳酸的电离常数K1=4.4×10-7,K2=4.7×10-11.NaHCO3水溶液显碱性,在NaHCO3溶液中继续逐渐通入二氧化碳,至溶液中n(HCO3-):n(H2CO3)=4.4时溶液可以达中性.
Ⅱ、工业上可通过CO和H2化合制得CH3OH:CO(g)+2H2(g) CH3OH(g)△H (CO结构式为C≡O).又知某些化学键的键能(断开 1mol化学键时所需要的最低能量)数值如下表:
则△H=-116kJ•mol-1.
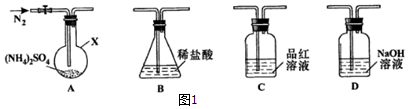
Ⅲ、电化学降解NO3-的原理如图1所示.
①电源 A 极为正极(填“正极”或“负极”),阴极反应式为2NO3-+10e-+12H+=6H2O+N2↑.
②若电解过程中转移了 1mol 电子,则膜左侧电解液的质量减少量为9g.
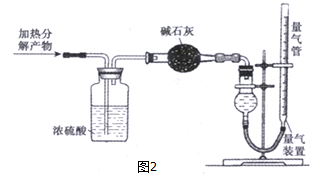
Ⅳ、已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一体积为 2L的恒温密闭玻璃容器中,10min反应达平衡.反应物浓度随时间变化关系如图2.
①图2中共有两条曲线X和Y,其中曲线X表示NO2浓度随时间的变化.下列不能说明该反应已达到平衡状态的是B.
A.容器内混合气体的压强不随时间变化而改变
B.容器内混合气体的密度不随时间变化而改变
C.容器内混合气体的颜色不随时间变化而改变
D.容器内混合气体的平均分子量不随时间变化而改变
②前 10min内化学反应的平衡常数K(b) 值为$\frac{10}{9}$
③反应 25min 时,若只改变了某一个条件,使曲线发生如图2所示的变化,该条件可能是增大NO2的浓度(用文字表达);其平衡常数 K(d)=K(b)(填“>”、“=”或“<”).
Ⅱ、工业上可通过CO和H2化合制得CH3OH:CO(g)+2H2(g) CH3OH(g)△H (CO结构式为C≡O).又知某些化学键的键能(断开 1mol化学键时所需要的最低能量)数值如下表:
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能 (kJ•mol-1) | 348 | 413 | 436 | 358 | 1072 | 463 |
Ⅲ、电化学降解NO3-的原理如图1所示.

①电源 A 极为正极(填“正极”或“负极”),阴极反应式为2NO3-+10e-+12H+=6H2O+N2↑.
②若电解过程中转移了 1mol 电子,则膜左侧电解液的质量减少量为9g.
Ⅳ、已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一体积为 2L的恒温密闭玻璃容器中,10min反应达平衡.反应物浓度随时间变化关系如图2.
①图2中共有两条曲线X和Y,其中曲线X表示NO2浓度随时间的变化.下列不能说明该反应已达到平衡状态的是B.
A.容器内混合气体的压强不随时间变化而改变
B.容器内混合气体的密度不随时间变化而改变
C.容器内混合气体的颜色不随时间变化而改变
D.容器内混合气体的平均分子量不随时间变化而改变
②前 10min内化学反应的平衡常数K(b) 值为$\frac{10}{9}$
③反应 25min 时,若只改变了某一个条件,使曲线发生如图2所示的变化,该条件可能是增大NO2的浓度(用文字表达);其平衡常数 K(d)=K(b)(填“>”、“=”或“<”).
20.分子式为C9H10O2,并能与饱和NaHCO3溶液反应放出气体的芳香族化合物有(不考虑立体异构)( )
0 163253 163261 163267 163271 163277 163279 163283 163289 163291 163297 163303 163307 163309 163313 163319 163321 163327 163331 163333 163337 163339 163343 163345 163347 163348 163349 163351 163352 163353 163355 163357 163361 163363 163367 163369 163373 163379 163381 163387 163391 163393 163397 163403 163409 163411 163417 163421 163423 163429 163433 163439 163447 203614
| A. | 6种 | B. | 14种 | C. | 16种 | D. | 18种 |



 $\stackrel{自动失水}{→}$
$\stackrel{自动失水}{→}$ +H2O
+H2O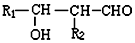
 ;G:(CH2OH)3CCHO.
;G:(CH2OH)3CCHO. .
. .
. (写一种).
(写一种).