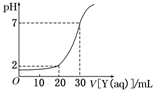
 如图为对15mL一定物质的量浓度的盐酸X用一定物质的量浓度的NaOH溶液Y滴定的图象,根据图象推出X(mol/L)和Y(mol/L)的物质的量浓度是下表内各组中的( ) 如图为对15mL一定物质的量浓度的盐酸X用一定物质的量浓度的NaOH溶液Y滴定的图象,根据图象推出X(mol/L)和Y(mol/L)的物质的量浓度是下表内各组中的( )
|
(2009?海南)在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
|
 如图为对15mL一定物质的量浓度的盐酸X用一定物质的量浓度的NaOH溶液Y滴定的图象,根据图象推出X(mol/L)和Y(mol/L)的物质的量浓度是下表内各组中的( ) 如图为对15mL一定物质的量浓度的盐酸X用一定物质的量浓度的NaOH溶液Y滴定的图象,根据图象推出X(mol/L)和Y(mol/L)的物质的量浓度是下表内各组中的( )
|
(2009?海南)在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
|