13.阿托酸甲酯(Y)能用于治疗肠道疾病,它可由阿托酸(X)经过下列反应合成:

下列说法正确的是( )

下列说法正确的是( )
| A. | X可用于合成高分子化合物,Y不能合成高分子化合物 | |
| B. | X在烧碱溶液中变质,而Y在烧碱溶液中不变质 | |
| C. | X分子中所有原子均可能共平面 | |
| D. | X和Y分别与浓硝酸反应都能生成5种二硝基取代物 |
12.化学与生产、生活密切相关,下列说法正确的是( )
| A. | 氢氟酸可蚀刻玻璃说明氢氟酸具有强酸性 | |
| B. | 油脂的氢化说明油脂分子中含有不饱和键 | |
| C. | 维生素C常用作抗氧化剂说明它具有氧化性 | |
| D. | 汽车尾气中含有氮氧化物说明汽油中含有氮元素 |
11. “天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将太阳能电池电解水技术与氢氧燃料电池技术相结合的可充电电池.下图为RFC工作原理示意图(隔膜为质子选择性透过膜),下列说法中正确的是( )
“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将太阳能电池电解水技术与氢氧燃料电池技术相结合的可充电电池.下图为RFC工作原理示意图(隔膜为质子选择性透过膜),下列说法中正确的是( )
 “天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将太阳能电池电解水技术与氢氧燃料电池技术相结合的可充电电池.下图为RFC工作原理示意图(隔膜为质子选择性透过膜),下列说法中正确的是( )
“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将太阳能电池电解水技术与氢氧燃料电池技术相结合的可充电电池.下图为RFC工作原理示意图(隔膜为质子选择性透过膜),下列说法中正确的是( )| A. | c极上发生的电极反应是:O2+4H++4e-═2H2O | |
| B. | 当有0.1mol电子转移时,b极产生1.12L 气体Y(标准状况下) | |
| C. | 装置I与装置II的电解质溶液中,氢离子运动方向相反 | |
| D. | RFC系统工作过程中只存在3种形式的能量转化 |
10.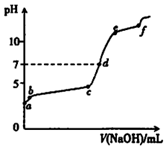 向0.1mol/L的Al2( SO4)3溶液中滴加1.0mol/L的NaOH溶液,滴加过程中溶液pH随NaOH溶液体积变化的曲线如图所示.下列分析不正确的是( )
向0.1mol/L的Al2( SO4)3溶液中滴加1.0mol/L的NaOH溶液,滴加过程中溶液pH随NaOH溶液体积变化的曲线如图所示.下列分析不正确的是( )
 向0.1mol/L的Al2( SO4)3溶液中滴加1.0mol/L的NaOH溶液,滴加过程中溶液pH随NaOH溶液体积变化的曲线如图所示.下列分析不正确的是( )
向0.1mol/L的Al2( SO4)3溶液中滴加1.0mol/L的NaOH溶液,滴加过程中溶液pH随NaOH溶液体积变化的曲线如图所示.下列分析不正确的是( )| A. | a点pH<7的原因:Al3++3H2O?Al(OH)3+3H+ | |
| B. | bc段发生的主要反应:Al3++3OH-═Al(OH)3 | |
| C. | ef段发生的主要反应:Al(OH)3+OH-═AlO2-+2H2O | |
| D. | d点,溶液中大量存在的离子是Na+、AlO2-和SO42- |
9.下列解释事实的方程式不正确的是( )
| A. | 电解饱和食盐水,产生黄绿色气体:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+H2+Cl2 | |
| B. | 用Na2CO3溶液将水垢中的CaSO4转化为CaCO3:CO32-+Ca2+=CaCO3 | |
| C. | 向H202溶液中滴加CuSO4溶液,产生气泡:2H2O2 $\frac{\underline{\;CuSO_{4}\;}}{\;}$2H2O+O2 T | |
| D. | 向苯酚浊液中滴加Na2CO3溶液,溶液变澄清: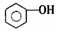 +CO32-→ +CO32-→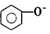 +HCO3- +HCO3- |
8.氯化亚铁具有独有的脱色能力,适用于染料、染料中间体、印染、造纸行业的污水处理.某课题小组设计如下方案制备氯化亚铁并探究氯化亚铁(Fe2+)的还原性.
某同学选择下列装置用氯化铁制备少量氯化亚铁(装置不可以重复使用).查阅资料知,氯化铁遇水剧烈水解,在加热条件下氢气还原氯化铁生成FeCl2.

(1)实验开始前应先检查装置的气密性,请叙述装置A气密性检验的方法:关闭活塞,向长颈漏斗内注水至形成一段水柱且液面高度不变,说明装置气密性良好
(2)气流从左至右,装置接口连接顺序是ab c e f d
(3)装置C中干燥管中所盛试剂的名称是:碱石灰或生石灰,作用是:除去HCl、并防止空气中水的进入
(4)装置D中发生的化学方程式是:2FeCl3+H2$\frac{\underline{\;\;△\;\;}}{\;}$2HCl+2FeCl2
(5)为了测定氯化亚铁的质量分数,某同学进行了如下实验:
称取实验制备的氯化亚铁样品5.435g,配成溶液,用1.00mol•L-1酸性KMnO4标准溶液滴定至终点.(已知还原性Fe2+>Cl-)滴定结果如表所示:
①写出滴定过程中所发生的2个离子方程式MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O,2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O
②样品中氯化亚铁的质量分数为70.1%.
某同学选择下列装置用氯化铁制备少量氯化亚铁(装置不可以重复使用).查阅资料知,氯化铁遇水剧烈水解,在加热条件下氢气还原氯化铁生成FeCl2.

(1)实验开始前应先检查装置的气密性,请叙述装置A气密性检验的方法:关闭活塞,向长颈漏斗内注水至形成一段水柱且液面高度不变,说明装置气密性良好
(2)气流从左至右,装置接口连接顺序是ab c e f d
(3)装置C中干燥管中所盛试剂的名称是:碱石灰或生石灰,作用是:除去HCl、并防止空气中水的进入
(4)装置D中发生的化学方程式是:2FeCl3+H2$\frac{\underline{\;\;△\;\;}}{\;}$2HCl+2FeCl2
(5)为了测定氯化亚铁的质量分数,某同学进行了如下实验:
称取实验制备的氯化亚铁样品5.435g,配成溶液,用1.00mol•L-1酸性KMnO4标准溶液滴定至终点.(已知还原性Fe2+>Cl-)滴定结果如表所示:
| 滴定次数 | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | |
| 1 | 1.04 | 25.03 |
| 2 | 1.98 | 25.99 |
| 3 | 3.20 | 25.24 |
②样品中氯化亚铁的质量分数为70.1%.
7.下列关于原子结构、元素性质的说法正确的是( )
| A. | 非金属元素组成的化合物中只含共价键 | |
| B. | ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强 | |
| C. | 同种元素的原子均有相同的质子数和中子数 | |
| D. | IA族金属元素是同周期中金属性最强的元素 |
6.常温下,下列各组离子一定能在指定溶液中大量共存的是( )
| A. | pH=1的溶液中:Na+、Cu2+、Cl-、CO32- | |
| B. | 0.1 mol•L-1 AlCl3溶液中:Cu2+、Mg2+、SO42-、NO3- | |
| C. | 由水电离产生的c(H+)=10-12 mol•L-1的溶液中:NH4+、SO42-、HCO3-、Cl- | |
| D. | 1.0mol/LKNO3溶液中:Fe2+、H+、Cl-、SO42- |
5.下列叙述中,正确的是( )
| A. | 同系物的化学性质一定相似 | |
| B. | 卤代烃在氢氧化钠醇溶液中共热均能发生消去反应 | |
| C. | 1mol醛与银氨溶液反应只能还原出2molAg | |
| D. | 在催化剂作用下,丙醛、丙酮、丙酸均能与氢气发生加成反应 |
4.下列有关实验的设计可行的是( )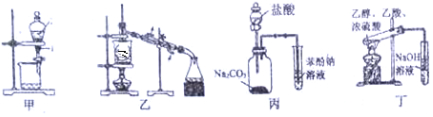
0 162710 162718 162724 162728 162734 162736 162740 162746 162748 162754 162760 162764 162766 162770 162776 162778 162784 162788 162790 162794 162796 162800 162802 162804 162805 162806 162808 162809 162810 162812 162814 162818 162820 162824 162826 162830 162836 162838 162844 162848 162850 162854 162860 162866 162868 162874 162878 162880 162886 162890 162896 162904 203614

| A. | 装置甲:用CCl4萃取碘水中的碘 | |
| B. | 装置乙:用于从酒精水溶液中制取无水乙醇 | |
| C. | 装置丙:验证盐酸、碳酸、苯酚溶液的酸性 | |
| D. | 装置丁:用乙酸、乙醇制取乙酸乙酯 |