题目内容
9.下列解释事实的方程式不正确的是( )| A. | 电解饱和食盐水,产生黄绿色气体:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+H2+Cl2 | |
| B. | 用Na2CO3溶液将水垢中的CaSO4转化为CaCO3:CO32-+Ca2+=CaCO3 | |
| C. | 向H202溶液中滴加CuSO4溶液,产生气泡:2H2O2 $\frac{\underline{\;CuSO_{4}\;}}{\;}$2H2O+O2 T | |
| D. | 向苯酚浊液中滴加Na2CO3溶液,溶液变澄清: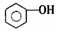 +CO32-→ +CO32-→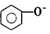 +HCO3- +HCO3- |
分析 A.电解饱和的食盐水生成氢氧化钠,氢气和氯气;
B.用Na2CO3溶液除水垢中的CaSO4生成碳酸钙和硫酸钠,CaSO4是一种微溶物书写离子方程式不拆;
C.向H202溶液中滴加CuSO4溶液生成水和氧气;
D.向苯酚浊液中滴加Na2CO3溶液生成苯酚钠和碳酸氢钠.
解答 解:A.电解饱和的食盐水生成氢氧化钠,氢气和氯气,故化学方程式为2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+H2+Cl2,故A正确;
B.用Na2CO3溶液除水垢中的CaSO4生成碳酸钙和硫酸钠,CaSO4是一种微溶物书写离子方程式不拆,故离子方程式为CO32-+CaSO4=CaCO3+SO42-,故B错误;
C.向H202溶液中滴加CuSO4溶液生成水和氧气,故化学方程式为2H2O2 $\frac{\underline{\;CuSO_{4}\;}}{\;}$2H2O+O2↑,故C正确;
D.向苯酚浊液中滴加Na2CO3溶液生成苯酚钠和碳酸氢钠,故离子方程式为 +CO32-→
+CO32-→ +HCO3-,故D正确,
+HCO3-,故D正确,
故选B.
点评 本题考查化学方程式的书写,为高频考点,把握发生的反应及反应生成物是什么,题目难度不大.

练习册系列答案
相关题目
19.下列叙述中,错误的是( )
| A. | 苯与浓硝酸、浓硫酸共热并保持50~60℃反应生成硝基苯 | |
| B. | 苯乙烯在合适条件下催化加氢可生成乙基环己烷 | |
| C. | 乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷 | |
| D. | 甲苯与氯气在光照下反应主要生成2,4-二氯甲苯 |
20.肼(N2H4)是一种高能燃料,在生产和研究中用途广泛.化学小组同学在实验室中用过量NH3和NaC1O溶液反应制取N2H4(液)并探究其性质.回答下列问题:
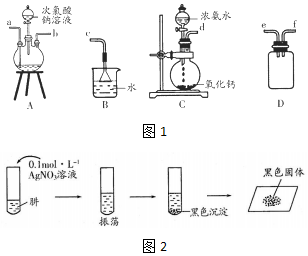
(1)肼的制备
①用图1装置制取肼,其连接顺序为defabc(按气流方向,用小写字母表示).
②装置A中发生反应的化学方程式为NaClO+2NH3=N2H4+NaCl+H2O,装置D的作用是防止倒吸或安全瓶.
(2)探究:N2H4和AgNO3溶液的反应将制得的肼分离提纯后,进行如下实验如图2:
证明黑色沉淀已洗涤干净的操作是取最后一次洗涤液少许于试管中,滴加NaCl溶液,无白色沉淀生成说明沉淀已洗涤干净.
【查阅资料】N2H4水溶液的碱性弱于氨水;N2H4有强还原性.AgOH在溶液中不稳定易分解生成Ag2O;Ag2O和粉末状的Ag均为黑色;Ag2O可溶于氨水.
【提出假设】
假设1:黑色固体可能是Ag;
假设2:黑色固体可能是Ag2O;
假设3:黑色固体可能是Ag和Ag2O.
【实验验证】该同学基于上述假设,设计如下方案,进行实验,请完成下表中的空白部分.
根据实验现象,假设1成立,则N2H4与AgNO3溶液反应的离子方程式为N2H4+4Ag+=4Ag↓+N2↑+4H+.

(1)肼的制备
①用图1装置制取肼,其连接顺序为defabc(按气流方向,用小写字母表示).
②装置A中发生反应的化学方程式为NaClO+2NH3=N2H4+NaCl+H2O,装置D的作用是防止倒吸或安全瓶.
(2)探究:N2H4和AgNO3溶液的反应将制得的肼分离提纯后,进行如下实验如图2:
证明黑色沉淀已洗涤干净的操作是取最后一次洗涤液少许于试管中,滴加NaCl溶液,无白色沉淀生成说明沉淀已洗涤干净.
【查阅资料】N2H4水溶液的碱性弱于氨水;N2H4有强还原性.AgOH在溶液中不稳定易分解生成Ag2O;Ag2O和粉末状的Ag均为黑色;Ag2O可溶于氨水.
【提出假设】
假设1:黑色固体可能是Ag;
假设2:黑色固体可能是Ag2O;
假设3:黑色固体可能是Ag和Ag2O.
【实验验证】该同学基于上述假设,设计如下方案,进行实验,请完成下表中的空白部分.
| 实验编号 | 操作 | 现象 | 实验结论 |
| 1 | 取少量黑色固体于试管,加入足量氨水,振荡 | 黑色固体不溶解 | 假设1成立 |
| 2 | 操作同实验1 | 黑色固体完全溶解 | 假设2成立 |
| 3 | ①取少量黑色固体于试管中,加入适量氨水,振荡,静置,取上层清液于洁净试管中,加入几滴乙醛,水浴加热②取少量黑色固体于试管中,加入足量稀硝酸,振荡 | ①试管内壁有银镜生成 ②固态完全溶解,并有气体产生 | 假设3成立 |
17.下列关于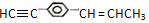 的说法正确的是( )
的说法正确的是( )
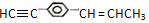 的说法正确的是( )
的说法正确的是( )| A. | 所有碳原子有可能都在同一平面上 | |
| B. | 最多只可能有9个碳原子在同一平面上 | |
| C. | 有7个碳原子可能在同一直线上 | |
| D. | 至少有6个碳原子在同一直线上 |
4.下列有关实验的设计可行的是( )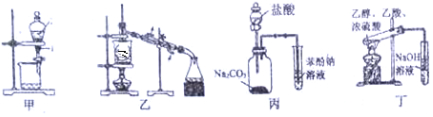

| A. | 装置甲:用CCl4萃取碘水中的碘 | |
| B. | 装置乙:用于从酒精水溶液中制取无水乙醇 | |
| C. | 装置丙:验证盐酸、碳酸、苯酚溶液的酸性 | |
| D. | 装置丁:用乙酸、乙醇制取乙酸乙酯 |
14.下列实验方案、现象与结论均正确的是( )
| 选项 | 实验方案 | 现象 | 结论 |
| A | 向SiO2固体中加入足量盐酸 | 固体不溶解 | SiO2不溶于任何酸 |
| B | 向Na2CO3溶液中通入足量CO2 | 产生晶体 | 溶解度:NaHCO3>Na2CO3 |
| C | 向75%的酒精中加入小粒钠 | 产生气泡 | 乙醇与钠反应产生H2 |
| D | 向KI 淀粉溶液中通入气体X | 溶液变蓝 | X的氧化性比I2的氧化性强 |
| A. | A | B. | B | C. | C | D. | D |
1. 钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,电池反应为:2Na+xS═Na2Sx,电池结构如图所示.下列说法不正确的是( )
钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,电池反应为:2Na+xS═Na2Sx,电池结构如图所示.下列说法不正确的是( )
 钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,电池反应为:2Na+xS═Na2Sx,电池结构如图所示.下列说法不正确的是( )
钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,电池反应为:2Na+xS═Na2Sx,电池结构如图所示.下列说法不正确的是( )| A. | 放电时,Na作负极,反应式为Na-e-=Na+ | |
| B. | 钠硫电池在常温下也能正常工作 | |
| C. | 放电时Na+向正极移动 | |
| D. | 当外电路通过0.25mol电子时消耗16g硫,则x=4 |
9.表为元素周期表的一部分.
请判断 X、Y、Z,并用相应的元素符号回答下列问题.
(1)X是Si,它的原子M层电子数是4.
(2)表中元素原子半径最大的是Si.
(3)Y在元素周期表中的位置是第二周期第ⅥA族,用电子式表示Y的最简单氢化物的形成过程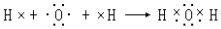 .
.
(4)氮气中氮原子之间的化学键属于共价键键,由氮气与氢气反应生成1mol氨气时转移电子的数目是3NA.
(5)硫与Z两种元素相比,非金属性强的是Cl,请用化学方程式说明这一结论H2S+Cl2=S↓+2HCl.
(6)碳、氮、Y三种元素的最简单气态氢化物的稳定性由强到弱的顺序是H2O>NH3>CH4.由最高价碳元素与最低价氮元素组成化合物的化学式是C3N4.
| 碳 | 氮 | Y | |
| X | 硫 | Z |
(1)X是Si,它的原子M层电子数是4.
(2)表中元素原子半径最大的是Si.
(3)Y在元素周期表中的位置是第二周期第ⅥA族,用电子式表示Y的最简单氢化物的形成过程
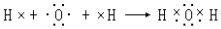 .
.(4)氮气中氮原子之间的化学键属于共价键键,由氮气与氢气反应生成1mol氨气时转移电子的数目是3NA.
(5)硫与Z两种元素相比,非金属性强的是Cl,请用化学方程式说明这一结论H2S+Cl2=S↓+2HCl.
(6)碳、氮、Y三种元素的最简单气态氢化物的稳定性由强到弱的顺序是H2O>NH3>CH4.由最高价碳元素与最低价氮元素组成化合物的化学式是C3N4.