12.某二元酸(H2A)在水中的电离方程式为H2A═H++HA-,HA-?H++A2-(25℃时Ka=1.0×10-2),下列说法正确的是( )
| A. | 在0.1mol•L-1的Na2A溶液中,c(A2-)+c(HA-)+2c(Na+)=0.5mol•L-1 | |
| B. | 在0.1mol•L-1的H2A溶液中,c(H+)>0.12mol•L-1 | |
| C. | 将同浓度(0.1mol•L-1)的NaHA和Na2A溶液等体积混合,混合溶液可能呈碱性 | |
| D. | 0.1mol•L-1的NaHA溶液中离子浓度为c(Na+)>c(H+)>c(A2-)>c(OH-) |
10.二氧化碳重整甲烷不仅可以获得合成气(CO和H2)还可减少温室气体排放.回答下列问题:
(1)已知断裂1mol化学键所需的能量如表:(CO的化学键近似表示为CO):
则反应CH4(g)+CO2(g)?2CO(g)+2H2(g)△H=+238KJ/molkJ•mol-1.
(2)在T℃时,向恒温4L的密闭容器中通入6mol CO2、6mol CH4,在催化剂作用下发生反应:CO2(g)+CH4(g)?2CO(g)+2H2(g).达平衡时H2的体积分数为0.4,若再向容器中同时充入2mol CO2、6molCH4、4molCO和8molH2,则上述平衡向逆反应(填“正反应”或“逆反应”)方向移动.
(3)CH4/CO2重整反应通过热力学计算可得到的图象之一如图1.实际生产中有C、H2O(g)等生成,生成碳的反应之一为CH4(g)?C(s)+2H2(g),600℃之后,C的物质的量减少,请用方程式表示C减少的原因C+CO2$\frac{\underline{\;\;△\;\;}}{\;}$2CO.
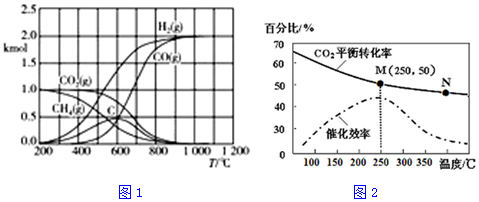
(4)不同温度对CO2的转化率及催化剂的效率影响如图2所示,下列有关说法不正确的是①②④(填序号).
①不同条件下反应,N点的速率最大
②温度低于250℃时,随温度升高乙烯的产率增大
③M点时平衡常数比N点时平衡常数大
④实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
(5)已知某温度下CO2(g)+CH4(g)?2CO(g)+2H2(g)的平衡常数为K1
H2O(g)+CH4(g)?CO(g)+3H2(g)的平衡常数为K2
C(s)+H2O(g)?2CO(g)+2H2(g)的平衡常数为K3
则反映C(g)+CO2(g)?2CO(g) 的平衡常数为K为$\frac{{K}_{3}{•K}_{1}}{{K}_{2}}$(用K1、K2、K3表示)
(1)已知断裂1mol化学键所需的能量如表:(CO的化学键近似表示为CO):
| 化学键 | C≡O | C=O | C-H | H-H |
| 能量/kJ•mol-1 | 1074 | 803 | 413 | 436 |
(2)在T℃时,向恒温4L的密闭容器中通入6mol CO2、6mol CH4,在催化剂作用下发生反应:CO2(g)+CH4(g)?2CO(g)+2H2(g).达平衡时H2的体积分数为0.4,若再向容器中同时充入2mol CO2、6molCH4、4molCO和8molH2,则上述平衡向逆反应(填“正反应”或“逆反应”)方向移动.
(3)CH4/CO2重整反应通过热力学计算可得到的图象之一如图1.实际生产中有C、H2O(g)等生成,生成碳的反应之一为CH4(g)?C(s)+2H2(g),600℃之后,C的物质的量减少,请用方程式表示C减少的原因C+CO2$\frac{\underline{\;\;△\;\;}}{\;}$2CO.

(4)不同温度对CO2的转化率及催化剂的效率影响如图2所示,下列有关说法不正确的是①②④(填序号).
①不同条件下反应,N点的速率最大
②温度低于250℃时,随温度升高乙烯的产率增大
③M点时平衡常数比N点时平衡常数大
④实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
(5)已知某温度下CO2(g)+CH4(g)?2CO(g)+2H2(g)的平衡常数为K1
H2O(g)+CH4(g)?CO(g)+3H2(g)的平衡常数为K2
C(s)+H2O(g)?2CO(g)+2H2(g)的平衡常数为K3
则反映C(g)+CO2(g)?2CO(g) 的平衡常数为K为$\frac{{K}_{3}{•K}_{1}}{{K}_{2}}$(用K1、K2、K3表示)
5. 2016年10月11日,神舟十一号飞船搭乘CZ-2F火箭成功发射.在重达495 吨的起飞重量中,95%的都是化学推进剂.
2016年10月11日,神舟十一号飞船搭乘CZ-2F火箭成功发射.在重达495 吨的起飞重量中,95%的都是化学推进剂.
(1)降冰片烯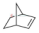 (C7H10)是一种重要的高密度液体燃料化学推进剂.已知:
(C7H10)是一种重要的高密度液体燃料化学推进剂.已知:
写出表示降冰片烯标准燃烧热的热化学方程式:C7H10(l)+9.5O2(g)=7CO2(g)+5H2O(l)△H=-3948kJ/mol.
(2)CH3OH和液氧是常用的液体火箭推进剂.
①已知:CO2(g)+3H2(g)?CH3OH(g)+H2O(l)△H1
2H2(g)+O2(l)═2H2O(l)△H2
CH3OH(g)═CH3OH(l)△H3
2CH3OH(l)+3O2(l)═2CO2(g)+4H2O(l)△H4
则△H4=3△H2-2△H1-2△H3(用△H1、△H2、△H3来表示).
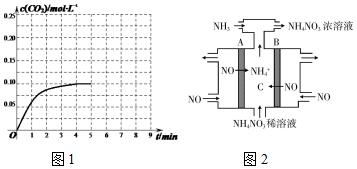
②某温度下,发生反应CO2(g)+3H2(g)?CH3OH (g)+H2O(g).在体积为2L的密闭容器中加入1mol CH3OH和1mol H2O,第4min达到平衡,容器内c(CO2)随时间的变化情况如图1所示,求此反应在该温度下的平衡常数59.26.保持其它条件不变,在第5min时向体系中再充入0.2mol CO2和0.4mol H2,第8min重新达到平衡,此时c(H2)=c(CH3OH).请在图中画出5到9min的c(CO2)变化曲线示意图.
(3)NH4NO3也是一种重要的固体推进剂,可通过电解NO制备NH4NO3,其工作原理如图2所示,A电极的名称为阴极,请写出在B电极上发生的电极反应式:NO-3e-+2H2O=NO3-+4H+.
 2016年10月11日,神舟十一号飞船搭乘CZ-2F火箭成功发射.在重达495 吨的起飞重量中,95%的都是化学推进剂.
2016年10月11日,神舟十一号飞船搭乘CZ-2F火箭成功发射.在重达495 吨的起飞重量中,95%的都是化学推进剂.(1)降冰片烯
 (C7H10)是一种重要的高密度液体燃料化学推进剂.已知:
(C7H10)是一种重要的高密度液体燃料化学推进剂.已知:| 燃料 | 密度(g•cm-3) | 体积热值(J•L-1) |
| 降冰片烯 | 1.0 | 4.2×107 |
(2)CH3OH和液氧是常用的液体火箭推进剂.
①已知:CO2(g)+3H2(g)?CH3OH(g)+H2O(l)△H1
2H2(g)+O2(l)═2H2O(l)△H2
CH3OH(g)═CH3OH(l)△H3
2CH3OH(l)+3O2(l)═2CO2(g)+4H2O(l)△H4
则△H4=3△H2-2△H1-2△H3(用△H1、△H2、△H3来表示).
②某温度下,发生反应CO2(g)+3H2(g)?CH3OH (g)+H2O(g).在体积为2L的密闭容器中加入1mol CH3OH和1mol H2O,第4min达到平衡,容器内c(CO2)随时间的变化情况如图1所示,求此反应在该温度下的平衡常数59.26.保持其它条件不变,在第5min时向体系中再充入0.2mol CO2和0.4mol H2,第8min重新达到平衡,此时c(H2)=c(CH3OH).请在图中画出5到9min的c(CO2)变化曲线示意图.
(3)NH4NO3也是一种重要的固体推进剂,可通过电解NO制备NH4NO3,其工作原理如图2所示,A电极的名称为阴极,请写出在B电极上发生的电极反应式:NO-3e-+2H2O=NO3-+4H+.
4.恒温恒容下,反应A(s)+2B(g)═2C(g)的平衡常数为4,现向该容器中投入lmol的C物质,平衡时,C的转化率为( )
0 162698 162706 162712 162716 162722 162724 162728 162734 162736 162742 162748 162752 162754 162758 162764 162766 162772 162776 162778 162782 162784 162788 162790 162792 162793 162794 162796 162797 162798 162800 162802 162806 162808 162812 162814 162818 162824 162826 162832 162836 162838 162842 162848 162854 162856 162862 162866 162868 162874 162878 162884 162892 203614
| A. | 20% | B. | 33% | C. | 50% | D. | 89% |
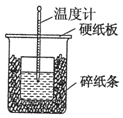 50mL 0.55mol•L-1盐酸与50mL 0.50mol•L-1NaOH溶液在如图的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
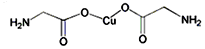
50mL 0.55mol•L-1盐酸与50mL 0.50mol•L-1NaOH溶液在如图的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: 磷化铜(Cu3P2)用于制造磷青铜、磷青铜是含少量锡、磷的铜合金,主要用作耐磨零件和弹性原件.
磷化铜(Cu3P2)用于制造磷青铜、磷青铜是含少量锡、磷的铜合金,主要用作耐磨零件和弹性原件.
 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示: ;
; ,该物质属于离子(离子、共价)化合物,该物质溶于水会破坏离子键(离子键、共价键).
,该物质属于离子(离子、共价)化合物,该物质溶于水会破坏离子键(离子键、共价键). ,该物质属于共价(离子、共价)化合物,该物质在受热气化时化学键没有(有、没有)遭到破坏.
,该物质属于共价(离子、共价)化合物,该物质在受热气化时化学键没有(有、没有)遭到破坏.