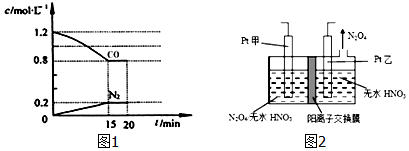
19.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 使甲基橙变红色的溶液:HCO3-、NO3-、Na+、NH4+ | |
| B. | pH=7溶液中:Fe3+、K+、SO42-、NO3- | |
| C. | 加入铝粉能产生H2的溶液:NH4+、K+、CO32-、NO3- | |
| D. | $\frac{{K}_{w}}{c({H}^{+})}$=0.1mol?L-1的溶液中:Na+、K+、SiO32-、AlO2- |
18.在给定条件下,下列选项所示的物质间转化均能实现的是( )
| A. | S$\stackrel{O_{2}、点燃}{→}$SO2$\stackrel{H_{2}O}{→}$H2SO4 | |
| B. | H2SO4$\stackrel{Cu}{→}$SO2$\stackrel{BaCl_{2}溶液}{→}$BaSO3 | |
| C. | Fe2O3$\stackrel{盐酸}{→}$FeCl3(aq)$\stackrel{蒸发}{→}$无水FeCl3 | |
| D. | SiO2$\stackrel{NaOH}{→}$Na2SiO3$\stackrel{HCl}{→}$H2SiO3 |
16.Mn、Fe均为第四周期过渡元素,两元素的部分电离能(I)数据列于表:
回答下列问题:
(1)Fe元素价电子层的电子排布式为3d64s2,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.对此,你的解释是由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态(或Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态).
(2)Fe原子或离子外围有较多能量相近的空轨道,能与一些分子或离子形成配合物,则与Fe原子或离子形成配合物的分子或离子应具备的条件是具有孤对电子.
(3)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂,据此判断三氯化铁晶体为分子晶体.
(4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示.面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为2:1,其中体心立方晶胞空间利用率为68%.
| 元素 | Mn | Fe | |
| 电离能(kJ/mol) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(1)Fe元素价电子层的电子排布式为3d64s2,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.对此,你的解释是由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态(或Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态).
(2)Fe原子或离子外围有较多能量相近的空轨道,能与一些分子或离子形成配合物,则与Fe原子或离子形成配合物的分子或离子应具备的条件是具有孤对电子.
(3)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂,据此判断三氯化铁晶体为分子晶体.
(4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示.面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为2:1,其中体心立方晶胞空间利用率为68%.
15.下列有关的说法不正确的是( )
| A. | 在一定条件下,苯与液溴、硝酸作用生成溴苯、硝基苯的反应都属于取代反应 | |
| B. | 戊烷有4种同分异构体,它们熔点、沸点各不相同 | |
| C. | 油脂发生皂化反应可以得到高级脂肪酸盐与甘油 | |
| D. | 淀粉和蛋白质都属于高分子化合物 |
14.下列指定反应的离子方程式正确的是( )
| A. | 用盐酸除铁锈:Fe2O3•xH2O+6H+═2Fe3++(3+x)H2O | |
| B. | Mg(HCO3)2溶液与足量的 NaOH 溶液反应:Mg2++HCO3-+OH-═MgCO3↓+H2O | |
| C. | 强碱性溶液中次氯酸钠溶液与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3=2FeO42-+3Cl-+H2O+4H+ | |
| D. | 用NaOH 溶液吸收 NO2:2NO2+2OH-═2NO3-+H2O |
12.在花瓶中插上一束美丽的鲜花,将会给你紧张而又忙碌的学习、生活带来轻松和愉悦的心情.可是过不了几天,花儿就会枯萎.如果在花瓶中加入“鲜花保鲜剂”,就会延长鲜花的寿命.表是1L“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是A(填字母).
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)“鲜花保鲜剂”中的K+的物质的量浓度约为(阿司匹林中不含K+)8.91×10-3mol/L
(3)配制上述1L“鲜花保鲜剂”所需的仪器有:量筒、烧杯、玻璃棒、托盘天平、药匙、胶头滴管,1000mL容量瓶.(填所缺仪器的名称).
(4)在溶液配制过程中,下列操作对配制结果没有影响的是BD(填字母).
A.定容用胶头滴管加水时,仰视观察溶液凹液面与容量瓶刻度线相切
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)实验室用固体加热制氨气的化学反应方程式为:2NH4Cl+Ca(OH)$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O
(6)若将收集到的氨气溶于水配成100mL的溶液,所得氨水中NH3物质量浓度(不考虑NH3与H2O的反应)为0.3mol•L-1,则需要氨气的体积为672mL(标准状况).
0 162517 162525 162531 162535 162541 162543 162547 162553 162555 162561 162567 162571 162573 162577 162583 162585 162591 162595 162597 162601 162603 162607 162609 162611 162612 162613 162615 162616 162617 162619 162621 162625 162627 162631 162633 162637 162643 162645 162651 162655 162657 162661 162667 162673 162675 162681 162685 162687 162693 162697 162703 162711 203614
| 成 分 | 质 量(g) | 摩尔质量(g/mol) |
| 蔗糖 | 50.00 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)“鲜花保鲜剂”中的K+的物质的量浓度约为(阿司匹林中不含K+)8.91×10-3mol/L
(3)配制上述1L“鲜花保鲜剂”所需的仪器有:量筒、烧杯、玻璃棒、托盘天平、药匙、胶头滴管,1000mL容量瓶.(填所缺仪器的名称).
(4)在溶液配制过程中,下列操作对配制结果没有影响的是BD(填字母).
A.定容用胶头滴管加水时,仰视观察溶液凹液面与容量瓶刻度线相切
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)实验室用固体加热制氨气的化学反应方程式为:2NH4Cl+Ca(OH)$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O
(6)若将收集到的氨气溶于水配成100mL的溶液,所得氨水中NH3物质量浓度(不考虑NH3与H2O的反应)为0.3mol•L-1,则需要氨气的体积为672mL(标准状况).
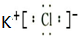 ;
;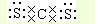 .
.