5.下列分散系不能发生丁达尔效应的是( )
| A. | 氢氧化铁浊液 | B. | 豆浆 | C. | 含尘埃的空气 | D. | 墨水 |
4.下列说法不正确的是( )
| A. | 明矾可作自来水的净水剂 | B. | 氢氧化铝可作胃酸的中和剂 | ||
| C. | 二氧化碳可用作钠着火的灭火剂 | D. | 小苏打可作面包的发泡剂 |
3.图象能直观地反映有关物理量的变化及规律,下列各图象与描述相符的是( )
| A. |  如图表示SO2氧化反应分别在有、无催化剂的情况下反应过程中的能量变化 | |
| B. |  如图表示0.1molMgCl2•6H2O在空气中充分加热时固体质量随时间的变化 | |
| C. |  如图表示分别稀释1mLpH=2的盐酸和醋酸时溶液pH的变化,图中b>100mL | |
| D. |  如图表示平衡2NO2(g)?N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化 |
2. 草酸(H2C2O4)是一种二元弱酸,部分性质如下:能溶于水,易溶于乙醇;大约在175℃升华(175℃以上分解生成H2O、CO2和CO);H2C2O4+Ca(OH)2=CaC2O4↓+2H2O.现用H2C2O4进行如下实验:
草酸(H2C2O4)是一种二元弱酸,部分性质如下:能溶于水,易溶于乙醇;大约在175℃升华(175℃以上分解生成H2O、CO2和CO);H2C2O4+Ca(OH)2=CaC2O4↓+2H2O.现用H2C2O4进行如下实验:
(一) 探究草酸的不稳定性
通过如图实验装置验证草酸受热分解产物中的CO2和CO,A、B、C中所加入的试剂分别是:

A、乙醇 B、Ca(OH)2或Ba(OH)2C、NaOH溶液.
(1)B中盛装的试剂Ca(OH)2或Ba(OH)2(填化学式)
(2)A中加入乙醇的目的是除去H2C2O4,避免对CO2的检验造成干扰.
(二) 探究草酸的酸性
将0.01mol草酸晶体(H2C2O4•2H2O)加入到100ml 0.2mol/L的NaOH溶液中充分反应,测得反应后溶液呈碱性,其原因是C2O42-+H2O?HC2O4-+OH-(用离子方程式表示).
(三) 用酸性KMnO4溶液与H2C2O4溶液反应来探究影响化学反应速率的因素
I、实验前先用酸性KMnO4标准溶液滴定未知浓度的草酸
反应原理:□MnO4-+□H2C2O4+□6H+=□Mn2++□CO2↑+□H2O
(1)配平上述离子方程式.
(2)滴定时KMnO4溶液应盛装于酸式(填“酸式”或“碱式”)滴定管中.
Ⅱ、探究影响化学反应速率的因素
如表列出了在“探究影响化学反应速率的因素”实验中得出的部分实验数据:
请回答:
(1)实验目的(a)是探究KMnO4溶液浓度对化学反应速率的影响;
(2)根据表中数据在右边坐标中画出反应褪色所需时间随KMnO4溶液浓度的变化关系图象;
(3)若要探究催化剂对该反应速率的影响应选择MnSO4而不选MnCl2作为催化剂,其原因是氯离子可与酸性高锰酸钾发生氧化还原反应.
 草酸(H2C2O4)是一种二元弱酸,部分性质如下:能溶于水,易溶于乙醇;大约在175℃升华(175℃以上分解生成H2O、CO2和CO);H2C2O4+Ca(OH)2=CaC2O4↓+2H2O.现用H2C2O4进行如下实验:
草酸(H2C2O4)是一种二元弱酸,部分性质如下:能溶于水,易溶于乙醇;大约在175℃升华(175℃以上分解生成H2O、CO2和CO);H2C2O4+Ca(OH)2=CaC2O4↓+2H2O.现用H2C2O4进行如下实验:(一) 探究草酸的不稳定性
通过如图实验装置验证草酸受热分解产物中的CO2和CO,A、B、C中所加入的试剂分别是:

A、乙醇 B、Ca(OH)2或Ba(OH)2C、NaOH溶液.
(1)B中盛装的试剂Ca(OH)2或Ba(OH)2(填化学式)
(2)A中加入乙醇的目的是除去H2C2O4,避免对CO2的检验造成干扰.
(二) 探究草酸的酸性
将0.01mol草酸晶体(H2C2O4•2H2O)加入到100ml 0.2mol/L的NaOH溶液中充分反应,测得反应后溶液呈碱性,其原因是C2O42-+H2O?HC2O4-+OH-(用离子方程式表示).
(三) 用酸性KMnO4溶液与H2C2O4溶液反应来探究影响化学反应速率的因素
I、实验前先用酸性KMnO4标准溶液滴定未知浓度的草酸
反应原理:□MnO4-+□H2C2O4+□6H+=□Mn2++□CO2↑+□H2O
(1)配平上述离子方程式.
(2)滴定时KMnO4溶液应盛装于酸式(填“酸式”或“碱式”)滴定管中.
Ⅱ、探究影响化学反应速率的因素
如表列出了在“探究影响化学反应速率的因素”实验中得出的部分实验数据:
| 实验组别 | c(H2C2O4) /(mol/L) | V(H2C2O4) /ml | c(KMnO4) /(mol/L) | V(KMnO4) /ml | c(H2SO4) /(mol/L) | 褪色所需时间 | 实验 目的 |
| 1 | 0.2 | 2 | 0.0025 | 4 | 0.12 | 6′55″ | (a)探究KMnO4溶液浓度对化学反应速率的影响 |
| 0.2 | 2 | 0.005 | 4 | 0.12 | 5′17″ | ||
| 0.2 | 2 | 0.01 | 4 | 0.12 | 3′20″ | ||
| 0.2 | 2 | 0.02 | 4 | 0.12 | 9′05″ | ||
| 0.2 | 2 | 0.03 | 4 | 0.12 | 11′33″ | ||
| 0.2 | 2 | 0.04 | 4 | 0.12 | 14′20″ |
(1)实验目的(a)是探究KMnO4溶液浓度对化学反应速率的影响;
(2)根据表中数据在右边坐标中画出反应褪色所需时间随KMnO4溶液浓度的变化关系图象;
(3)若要探究催化剂对该反应速率的影响应选择MnSO4而不选MnCl2作为催化剂,其原因是氯离子可与酸性高锰酸钾发生氧化还原反应.
9.根据下列实验操作与现象所得到的结论正确的是( )
| 选项 | 实验操作与现象 | 结论 |
| A | 向蛋白质溶液中滴加Pb(NO3)2溶液,产生白色沉淀,加水沉淀不消失 | 蛋白质发生了变性 |
| B | 测定浓度为 0.1mol•L-1CH3COONa与HCOONa 溶液的pH,CH3COONa溶液的pH较大 | 酸性:CH3COOH>HCOOH |
| C | 向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液,出现白色沉淀 | 溶液X中一定含有SO42- |
| D | 向浓度均为0.1mol•L-1NaCl和NaI混合溶液中滴加少量0.l mol•L-1AgNO3溶液,出现黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
| A. | A | B. | B | C. | C | D. | D |
8.室温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 含有大量Fe3+的溶液中:Na+、Fe2+、Br-、SO42- | |
| B. | 1.0 mol/L KMnO4的溶液中:H+、Na+、Cl-、SO42- | |
| C. | 能与铝反应放出H2的溶液中:K+、Mg2+、SO42-、NO3- | |
| D. | 水电离的c(H+)和C(OH-)之积为l×l0-20mol2•L-2的溶液中:Na+、K+、CO32-、Cl- |
7.合成可降解聚合物G的某流程的最后一步如图,下列有关说法不正确的是( )

| A. | 已知该步转化过程中的原子利用率为100%,则X为CO2 | |
| B. | 有机物F属于芳香族化合物,但不属于芳香烃 | |
| C. | (C9H8O3)n既是高分子G的化学式也是其链节的化学式 | |
| D. | 已知 经水解生成乙二醇,则F、G在一定条件下水解,可得相同的产物 经水解生成乙二醇,则F、G在一定条件下水解,可得相同的产物 |
6.下列图示与对应的叙述相符的是( )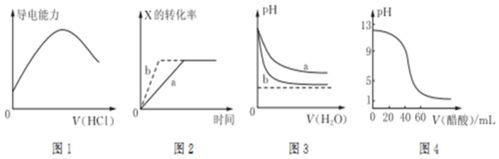
0 161936 161944 161950 161954 161960 161962 161966 161972 161974 161980 161986 161990 161992 161996 162002 162004 162010 162014 162016 162020 162022 162026 162028 162030 162031 162032 162034 162035 162036 162038 162040 162044 162046 162050 162052 162056 162062 162064 162070 162074 162076 162080 162086 162092 162094 162100 162104 162106 162112 162116 162122 162130 203614

| A. | 图1表示向氨水中通入HC1气体,溶液的导电能力变化 | |
| B. | 图2所示反应:X(g)+2Y(g)?3Z(g),b曲线表示的一定是增大压强 | |
| C. | 图3可表示pH相同的NaOH溶液与氨水稀释过程的pH变化,其中曲线a对应氨水 | |
| D. | 图4可表示用0.100 0 mol/L,醋酸滴定40.00 mL 0.100 0 mol/L NaOH溶液得到的滴定曲线 |