2.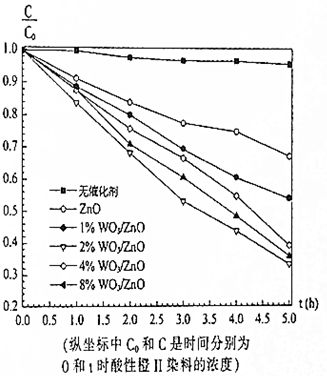 在紫外光照射下,利用WO3/ZnO光催化剂降解酸性橙Ⅱ染料废水的实验所得曲线如图.下列说法错误的是( )
在紫外光照射下,利用WO3/ZnO光催化剂降解酸性橙Ⅱ染料废水的实验所得曲线如图.下列说法错误的是( )
 在紫外光照射下,利用WO3/ZnO光催化剂降解酸性橙Ⅱ染料废水的实验所得曲线如图.下列说法错误的是( )
在紫外光照射下,利用WO3/ZnO光催化剂降解酸性橙Ⅱ染料废水的实验所得曲线如图.下列说法错误的是( )| A. | 不加催化剂时,紫外光照射降解酸性橙Ⅱ染料废水反应速率较慢 | |
| B. | 单一ZnO材料也是降解酸性橙Ⅱ染料废水的催化剂 | |
| C. | 2%WO3/ZnO的催化效果最好 | |
| D. | 由图中可以看出,光降解酸性橙Ⅱ染料是一个可逆反应 |
1.某兴趣小组利用以下实验装置模拟工业炼铁的主要过程:
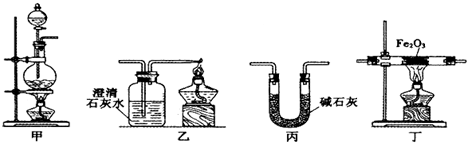
(1)装置甲中发生的反应为:HCOOH(甲酸)$→_{△}^{浓硫酸}$CO↑+H2O.已知甲酸是一种无色有刺激性气味的液体.制取一氧化碳时应该a(填字母).
a.将甲酸滴入浓硫酸 b.将浓硫酸滴入甲酸 c.将甲酸与浓硫酸混合后加入
(2)请按合适的顺序连接好以下装置:甲→丙→丁→乙
(3)丙装置中碱石灰的作用是除去一氧化碳中的甲酸和水蒸气.
(4)实验将近完成时,熄灭装置甲、乙、丁中酒精灯的先后顺序为丁甲乙.
(5)为了探究影响反应产物的外界因素,在Fe2O3与CO反应部位,该小组同学分别用酒精灯和酒精喷灯进行了两次实验,结果如下:
①甲同学猜想黑色产物中可能含有碳单质.乙同学排除了该可能,他提出的两种理由是:碳单质不会被磁铁吸引、从氧化还原角度分析不可能生成碳单质等.
②丙同学查找资料发现,Fe3O4也能被磁铁吸引,对黑色产物成分提出以下三种假设:i.全部为铁;ii.全部为四氧化三铁;iii.四氧化三铁和铁的混合物.

(1)装置甲中发生的反应为:HCOOH(甲酸)$→_{△}^{浓硫酸}$CO↑+H2O.已知甲酸是一种无色有刺激性气味的液体.制取一氧化碳时应该a(填字母).
a.将甲酸滴入浓硫酸 b.将浓硫酸滴入甲酸 c.将甲酸与浓硫酸混合后加入
(2)请按合适的顺序连接好以下装置:甲→丙→丁→乙
(3)丙装置中碱石灰的作用是除去一氧化碳中的甲酸和水蒸气.
(4)实验将近完成时,熄灭装置甲、乙、丁中酒精灯的先后顺序为丁甲乙.
(5)为了探究影响反应产物的外界因素,在Fe2O3与CO反应部位,该小组同学分别用酒精灯和酒精喷灯进行了两次实验,结果如下:
| 加热方式 | 通CO加热 时间/min | 澄清石灰水变 浑浊时间/min | 产物颜色 | 产物能否全部 被磁铁吸引 |
| 酒精灯 | 30 | 5 | 黑色 | 能 |
| 酒精喷灯 | 30 | 1 | 黑色 | 能 |
②丙同学查找资料发现,Fe3O4也能被磁铁吸引,对黑色产物成分提出以下三种假设:i.全部为铁;ii.全部为四氧化三铁;iii.四氧化三铁和铁的混合物.
13.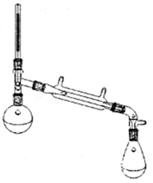 环乙烯是一种重要的化工原料,实验室常用下列反应制备环乙烯:
环乙烯是一种重要的化工原料,实验室常用下列反应制备环乙烯:
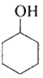 $→_{△}^{H_{2}SO_{4}}$
$→_{△}^{H_{2}SO_{4}}$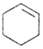 +H2O
+H2O
环己醇、环己烯的部分物理性质见表:
*括号中的数据表示该有机物与水形成的具有固定组成的混合物中有机物的质量分数
Ⅰ:制备环己烯粗品.实验中将环己醇与浓硫酸混合加入烧瓶中,按图所示装置,油浴加热,蒸馏约1h,收集馏分,得到主要含环己烯和水的混合物.
Ⅱ:环己烯的提纯.主要操作有abcde;
a.向馏出液中加入精盐至饱和;
b.加入3~4mL5%Na2CO3溶液;
c.静置,分液;
d.加入无水CaCl2固体;
e.蒸馏
回答下列问题:
(1)油浴加热过程中,温度控制在90℃以下,蒸馏稳定不宜过高的原因是减少未反应的环己醇蒸出.
(2)蒸馏不能彻底分离环己烯和水的原因是环己烯和水形成具有固定组成的混合物一起被蒸发.
(3)加入精盐至饱和的目的是增加水层的密度,有利于分层.
(4)加入3~4mL5%Na2CO3溶液的作用是中和产品中混有的微量的酸
(5)加入无水CaCl2固体的作用是除去有机物中少量的水
(6)利用核磁共振氢谱可以鉴定制备的产物是否为环己烯,环己烯分子中有 种不同环境的氢原子3.
 环乙烯是一种重要的化工原料,实验室常用下列反应制备环乙烯:
环乙烯是一种重要的化工原料,实验室常用下列反应制备环乙烯: $→_{△}^{H_{2}SO_{4}}$
$→_{△}^{H_{2}SO_{4}}$ +H2O
+H2O环己醇、环己烯的部分物理性质见表:
| 物质 | 沸点(℃) | 密度(g•cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8)* | 0.9624 | 能溶于水 |
| 环己烯 | 83(70.8)* | 0.8085 | 不溶于水 |
Ⅰ:制备环己烯粗品.实验中将环己醇与浓硫酸混合加入烧瓶中,按图所示装置,油浴加热,蒸馏约1h,收集馏分,得到主要含环己烯和水的混合物.
Ⅱ:环己烯的提纯.主要操作有abcde;
a.向馏出液中加入精盐至饱和;
b.加入3~4mL5%Na2CO3溶液;
c.静置,分液;
d.加入无水CaCl2固体;
e.蒸馏
回答下列问题:
(1)油浴加热过程中,温度控制在90℃以下,蒸馏稳定不宜过高的原因是减少未反应的环己醇蒸出.
(2)蒸馏不能彻底分离环己烯和水的原因是环己烯和水形成具有固定组成的混合物一起被蒸发.
(3)加入精盐至饱和的目的是增加水层的密度,有利于分层.
(4)加入3~4mL5%Na2CO3溶液的作用是中和产品中混有的微量的酸
(5)加入无水CaCl2固体的作用是除去有机物中少量的水
(6)利用核磁共振氢谱可以鉴定制备的产物是否为环己烯,环己烯分子中有 种不同环境的氢原子3.
10.下列物质的转化在给定条件下能实现的是( )
| A. | SiO2$\stackrel{H_{2}O}{→}$H2SiO3$\stackrel{NaOH(aq)}{→}$Na2SiO3 | |
| B. | 饱和食盐水$\stackrel{NH_{3}•CO_{2}}{→}$NaHCO3(s)$\stackrel{△}{→}$Na2CO3(s) | |
| C. | 海水$\stackrel{熟石灰}{→}$Mg(OH)2(s)$\stackrel{盐酸}{→}$MgCl2(aq)$\stackrel{电解}{→}$Mg(s) | |
| D. | NH3$→_{催化剂,△}^{O_{2}}$N2$\stackrel{O_{2},H_{2}O}{→}$HNO3 |
9.常温下,下列各组离子一定能在指定溶液中大量共存的是( )
| A. | pH=l 的溶液中:Ba2+、Fe3+、Cl-、SCN- | |
| B. | 能使酚酞变红的溶液:Ca2+、K+、HCO3-、CO32- | |
| C. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=10-12的溶液中:NH4+、Cu2+、NO3-、SO42- | |
| D. | 由水电离的c(H+)=10-12mol•L-1的溶液中:Na+、Al3+、Cl-、NO3- |
8.实验室采用下列装置制取氨气,正确的是( )
| A. |  生成NH3 | B. |  干燥NH3 | C. |  收集NH3并验满 | D. |  吸收多余NH3 |
7.下列反应的离子方程式正确的是( )
0 161917 161925 161931 161935 161941 161943 161947 161953 161955 161961 161967 161971 161973 161977 161983 161985 161991 161995 161997 162001 162003 162007 162009 162011 162012 162013 162015 162016 162017 162019 162021 162025 162027 162031 162033 162037 162043 162045 162051 162055 162057 162061 162067 162073 162075 162081 162085 162087 162093 162097 162103 162111 203614
| A. | 铜跟稀HNO3反应:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| B. | 向硫酸铝溶液中加入过量氨水:Al3++3OH-═AlO2-+2H2O | |
| C. | 向Ag(NH3)2NO3溶液中加入盐酸:Ag(NH3)2+2H+═Ag++2NH4+ | |
| D. | NaHSO4溶液和Ba(OH)2溶液混合后溶液呈中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O |