0 16084 16092 16098 16102 16108 16110 16114 16120 16122 16128 16134 16138 16140 16144 16150 16152 16158 16162 16164 16168 16170 16174 16176 16178 16179 16180 16182 16183 16184 16186 16188 16192 16194 16198 16200 16204 16210 16212 16218 16222 16224 16228 16234 16240 16242 16248 16252 16254 16260 16264 16270 16278 203614
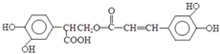 的合成线路如图所示:
的合成线路如图所示: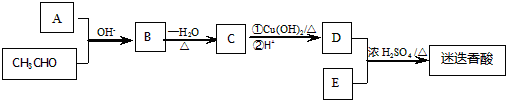
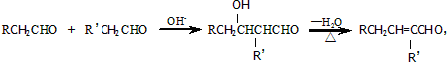 R、R’表示烃基或氢原子;
R、R’表示烃基或氢原子;
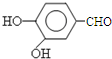
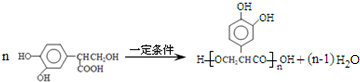
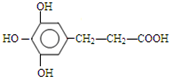
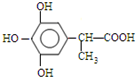
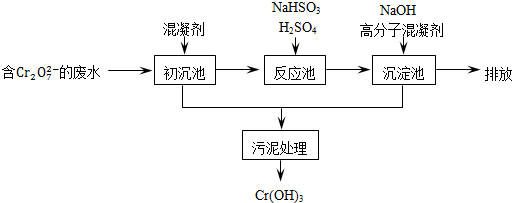




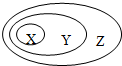 下表中所示物质或概念间的从属关系符合如图的是( )
下表中所示物质或概念间的从属关系符合如图的是( )