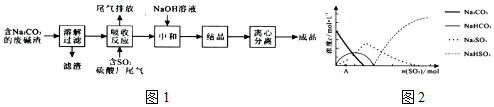
18.元素X、Y、Z位于不同短周期,原子序数依次增大.X、Z同主族,二者的原子序数之和是Y原子序数的两倍.主族元素W的原子最外层电子数比电子层数多4.下列说汰不正确的是( )
| A. | 简单离子半径:W>Z>X | |
| B. | X、Y、Z都能与W组成离子化合物 | |
| C. | X、Y组成的化合物可与W单质反应 | |
| D. | Q是Z、W组成的化合物,1molQ中约含有6.02×1023个阴离子 |
17.已知1~20号元素的离子,aW2+、bX+、cY2-、dZ-都具有相同的电子层结构,下列说法正确的是( )
| A. | 质子数:d>c>b>a | B. | 离子半径:W2+>X+>Y2->Z- | ||
| C. | 原子半径:Z<Y<W<X | D. | 最低负价:X<W<Z<Y |
16.aW、bX、cC、dZ、eR是五种短周期元素,e-d=d-c=c-b=b-a=4,其中一种是常见金属,下列有关说法不正确的是( )
| A. | Z为金属 | |
| B. | WY比WR稳定 | |
| C. | X的最高价氧化物对应的水化物为弱酸 | |
| D. | XR3是离子化合物 |
14.硼是第IIIA族元素,单质硼在加热条件下能与多种非金属反应.某同学欲利用氯气和单质硼反应制备三氯化硼.已知BC13的沸点为12.5℃,熔点为-107.3℃,遇水剧烈反应,生成硼酸和盐酸.
(1)该同学选用如图所示的部分装置(可以重复选用)进行实验,装置依次连接的合理顺序为A、B、D、C、E、D、F.
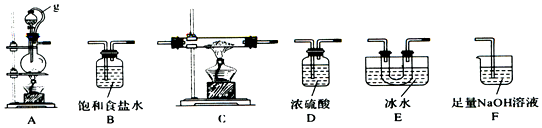
(2)A中反应的离子方程式为MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(3)图中g管的作用是保持气压平衡,便于分液漏斗中的液体流入蒸馏烧瓶,装置E 的作用是冷凝并收集BC13.
(4)停止实验,正确的操作是先熄灭C处酒精灯,再拔F处导管,后熄灭A处酒精灯.
(5)硼酸是一元弱酸,其钠盐化学式为Na[B(OH)4〕,则硼酸在水中的电离方程式是H3BO3+H2O═[B(OH)4]-+H+.
(6)实验完成后,某同学向F中(溶液含有0.05mol/LNaC10、0.05mol/LNaCl、0.1mol/LN a0H)滴加品红溶液,发现溶液褪色.现设计实验探究溶液褪色的原因,请在表中空格处填上数据,完成实验方案.
结论:NaClO使品红溶液褪色,溶液碱性越强褪色越慢.
(1)该同学选用如图所示的部分装置(可以重复选用)进行实验,装置依次连接的合理顺序为A、B、D、C、E、D、F.

(2)A中反应的离子方程式为MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(3)图中g管的作用是保持气压平衡,便于分液漏斗中的液体流入蒸馏烧瓶,装置E 的作用是冷凝并收集BC13.
(4)停止实验,正确的操作是先熄灭C处酒精灯,再拔F处导管,后熄灭A处酒精灯.
(5)硼酸是一元弱酸,其钠盐化学式为Na[B(OH)4〕,则硼酸在水中的电离方程式是H3BO3+H2O═[B(OH)4]-+H+.
(6)实验完成后,某同学向F中(溶液含有0.05mol/LNaC10、0.05mol/LNaCl、0.1mol/LN a0H)滴加品红溶液,发现溶液褪色.现设计实验探究溶液褪色的原因,请在表中空格处填上数据,完成实验方案.
| 实验序号 | 0.1mol/L NaClO溶液/mL | 0.1mol/L NaCl溶液/mL | 0.2mol/L NaOH溶液/mL | H2O/mL | 品红溶液 | 现象 |
| ① | 4.0 | 0 | 0 | 4.0 | 3滴 | 较快褪色 |
| ② | 0 | 4.0 | 4.0 | 0 | 3滴 | 不褪色 |
| ③ | 4.0 | 0 | 4.0 | 0 | 3滴 | 缓慢褪色 |
13.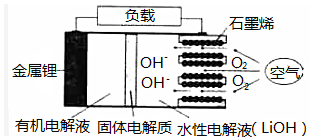 新型锂一空气电池具有能量密度高的优点,有望成为新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过.下列说法正确的是( )
新型锂一空气电池具有能量密度高的优点,有望成为新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过.下列说法正确的是( )
 新型锂一空气电池具有能量密度高的优点,有望成为新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过.下列说法正确的是( )
新型锂一空气电池具有能量密度高的优点,有望成为新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过.下列说法正确的是( )| A. | 放电时,负极反应式:Li-e-+OH-═LiOH | |
| B. | 放电时,当外电路中有1mole-转移时,水性电解液离子总数增加NA | |
| C. | 应用该电池电镀铜,阴极质量增加64g,理沦上将消耗11.2LO2 | |
| D. | 若把水性电解液换成固体氧化物电解质,则易引起正极材料碳孔堵塞 |
12.下列实验方案中,能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| ① | 检验淀粉是否水解生成葡萄糖 | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后新制Cu(OH)2浊液,加热,观察是否有红色沉淀生成 |
| ② | 比较H2CO3,HCN的酸性强弱 | 用pH计测定同温度同浓度的Na2CO3溶液和NaCN溶液的pH,比较pH大小 |
| ③ | 区别植物油和矿物油 | 向植物油和矿物油中分别加入烧碱溶液,加热,冷却后观察是否分层 |
| ④ | 验证CaCO3的溶解度小于CaSO4 | 将浓Na2CO3溶液滴加到CaSO4悬浊液中,充分振荡,过滤、洗涤,向所得固体中滴加盐酸,观察是否有气体生成 |
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①③ |
11.甲、乙、丙、丁四种物质在一定条件下有如图所示的转化关系.下列判断正确的是( )

| A. | 若图中均为非氧化还原反应,当丁为一元强碱时,甲可能是NaAlO2 | |
| B. | 若图中均为非氧化还原反应,当丁为一元强酸时,甲可能是NaOH | |
| C. | 若图中均为氧化还原反应,当丁为非金属单质时,丙可能是NH3 | |
| D. | 若图中均为氧化还原反应,当丁为金属单质时,丙可能是FeCl3 |
10.用NA表示阿佛加德罗常数的值,下列说法正确的是( )
0 161642 161650 161656 161660 161666 161668 161672 161678 161680 161686 161692 161696 161698 161702 161708 161710 161716 161720 161722 161726 161728 161732 161734 161736 161737 161738 161740 161741 161742 161744 161746 161750 161752 161756 161758 161762 161768 161770 161776 161780 161782 161786 161792 161798 161800 161806 161810 161812 161818 161822 161828 161836 203614
| A. | 在浓硫酸作用下,60g冰醋酸与足量无水乙醇反应生成乙酸乙酯的分子数为NA | |
| B. | 标准状况下,3.36LC2H4和C3H6的混合气体中含有碳碳双键的数目为0.15NA | |
| C. | 电解精炼铜,当外电路转移NA个电子时,阳极质量减少32g | |
| D. | 含0.01molFeCl3的浓溶液滴入沸水,制得的胶体粒子数目小于0.01NA |