20.下列对有机物的性质说法正确的是( )
| A. | 乙苯和邻二甲苯属于同分异构体 | |
| B. | 苯和苯乙烯属于同系物 | |
| C. | 糖类和蛋白质都属于天然高分子化合物 | |
| D. | 植物油和矿物油都属于油脂 |
19.化学与生活密切相关,下列一些物质的用途或对环境的影响解释错误的是( )
| 选项 | 对环境的影响(或用途) | 解释 |
| A | 酒精用于环境消毒 | 酒精能使蛋白质变性 |
| B | 热碳酸钠溶液清除炊具上残留的油污 | 碳酸钠溶液水解显碱性 |
| C | SO2和NO2溶于水形成酸雨 | SO2和NO2是酸性氧化物 |
| D | 浸泡过酸性KMnO4溶液的硅藻土保鲜水果 | 酸性KMnO4溶液氧化乙烯 |
| A. | A | B. | B | C. | C | D. | D |
18.利用如图所示装置进行下列实验,试管②中一定观察不到的现象是( )
| 选项 | a | b | c | 试管②中现象 | 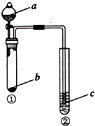 |
| A | NaOH溶液 | Al | 肥皂水 | 肥皂泡可点燃 | |
| B | 稀盐酸 | 碳酸钙 | NaAlO2溶液 | 生成白色絮状沉淀生成 | |
| C | 稀硫酸 | NaHCO3 | BaCl2溶液 | 溶液变浑浊 | |
| D | 水 | Na2O2 | 酸化的FeSO4溶液 | 溶液变黄 |
| A. | A | B. | B | C. | C | D. | D |
17.下列判断合理的是
①硫酸、烧碱、纯碱和生石灰分别属于酸、碱、盐和氧化物
②能电离出金属离子和酸根离子的化合物都是盐
③金属氧化物一定是碱性氧化物
④根据分散系是否具有丁达尔现象,将分散系分为溶液、胶体和浊液
⑤根据反应中是否有电子的转移,将化学反应分为氧化还原反应和非氧化还原反应
⑥稀释浓H2SO4时,将水慢慢倒入浓H2SO4中,并不断搅拌( )
①硫酸、烧碱、纯碱和生石灰分别属于酸、碱、盐和氧化物
②能电离出金属离子和酸根离子的化合物都是盐
③金属氧化物一定是碱性氧化物
④根据分散系是否具有丁达尔现象,将分散系分为溶液、胶体和浊液
⑤根据反应中是否有电子的转移,将化学反应分为氧化还原反应和非氧化还原反应
⑥稀释浓H2SO4时,将水慢慢倒入浓H2SO4中,并不断搅拌( )
| A. | 只有②④⑥ | B. | 只有③④⑥ | C. | 只有①③⑤ | D. | 只有①②⑤ |
16.下列有关实验的叙述正确的是( )
| A. | 蒸发时将蒸发皿放置在铁架台的铁圈上,并加垫石棉网加热 | |
| B. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| C. | 铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜的熔点高于铝 | |
| D. | 向某溶液中加入NaOH溶液得白色沉淀,又观察到沉淀颜色逐渐变为红褐色,说明该溶液中只含有Fe2+,不含有Mg2+ |
15.下列说法正确的是( )
| A. | 常温下,铁能被浓硝酸钝化,可用铁质容器贮运浓硝酸 | |
| B. | 包装食品里常有硅胶、石灰、还原铁粉三类小包,其作用相同 | |
| C. | 浓硫酸可用于干燥H2S和CO2 | |
| D. | 合金的物理性质一般与其各组分金属的物理性质相同 |
14. 某研究小组开发出一种人工仿生叶,据称该装置能“吃”进二氧化碳产出生物乙醇.这种装置能够利用太阳能电池板所提供的电力,而系统内的微生物以氢为食,能把空气中的二氧化碳转化为生物燃料.下列说法正确的是( )
某研究小组开发出一种人工仿生叶,据称该装置能“吃”进二氧化碳产出生物乙醇.这种装置能够利用太阳能电池板所提供的电力,而系统内的微生物以氢为食,能把空气中的二氧化碳转化为生物燃料.下列说法正确的是( )
 某研究小组开发出一种人工仿生叶,据称该装置能“吃”进二氧化碳产出生物乙醇.这种装置能够利用太阳能电池板所提供的电力,而系统内的微生物以氢为食,能把空气中的二氧化碳转化为生物燃料.下列说法正确的是( )
某研究小组开发出一种人工仿生叶,据称该装置能“吃”进二氧化碳产出生物乙醇.这种装置能够利用太阳能电池板所提供的电力,而系统内的微生物以氢为食,能把空气中的二氧化碳转化为生物燃料.下列说法正确的是( )| A. | 该电池为原电池装置 | |
| B. | a与外接电源正极相连 | |
| C. | a电极的电极反应式为2CO2+6H++12e-═C2H5OH+3H2O | |
| D. | 当a电极上生成1 mol C2H5OH时,b电极上产生标准状况下的气体体积为67.2 L |
13.关于容量瓶的使用,下列操作正确的是( )
0 161416 161424 161430 161434 161440 161442 161446 161452 161454 161460 161466 161470 161472 161476 161482 161484 161490 161494 161496 161500 161502 161506 161508 161510 161511 161512 161514 161515 161516 161518 161520 161524 161526 161530 161532 161536 161542 161544 161550 161554 161556 161560 161566 161572 161574 161580 161584 161586 161592 161596 161602 161610 203614
| A. | 使用前要先检查容量瓶是否漏液 | |
| B. | 用蒸馏水洗涤后必须要将容量瓶烘干 | |
| C. | 为了方便快捷,可以直接在容量瓶内进行固体溶解 | |
| D. | 定容结束后,为了使溶液均匀,手握瓶颈,左右振荡 |


