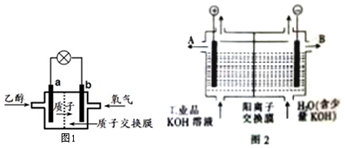
3.下列措施不能加快Zn与1mol/LH2SO4反应产生H2的速率的是( )
| A. | 升高温度 | B. | 用Zn粉代替Zn粒 | ||
| C. | 滴加少量的CuSO4溶液 | D. | 改用0.1mol/LH2SO4与Zn反应 |
2.下列离子在稳定人体血液的PH中起重要作用的是( )
| A. | HCO3- | B. | HSO3- | C. | Na+ | D. | Cl- |
20.一定条件下,用甲烷可以消除氧化物(NOx)的污染.已知:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1;
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ•mol-1.
则反应:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O的△H等于( )
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1;
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ•mol-1.
则反应:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O的△H等于( )
| A. | +867kJ•mol-1 | B. | -867kJ•mol-1 | C. | +1734kJ•mol-1 | D. | -1734kJ•mol-1 |
19.常温下,下列关于0.1mol•L-1的CH3COONa溶液的叙述中正确的是( )
| A. | 可由pH=1的CH3COOH溶液与pH=13的NaOH溶液等体积混合制得 | |
| B. | c(OH-)>c(H+) | |
| C. | c(Na+)>c(CH3COO-) | |
| D. | c(H+)+c(CH3COO-)=c(OH-) |
18.25℃时,三种浓度均为0.1mol•L-1的溶液pH如下表,下列说法正确的是( )
| 序号 | ① | ② | ③ |
| 溶液 | NaClO | NaHCO3 | Na2CO3 |
| pH | 10.3 | 8.3 | 11.6 |
| A. | 酸性:HClO>H2CO3 | |
| B. | 由水电离产生的c(OH-):①>② | |
| C. | 溶液①中的c(ClO-)大于溶液②中的c(HCO3-) | |
| D. | 溶液③中:c(HCO3-)+c(CO32-)=0.1 mol•L-1 |
17.下列溶液中导电性最强的是( )
| A. | 1L0.1mol•L-1醋酸 | B. | 1L0.1mol•L-1H2SO4溶液 | ||
| C. | 0.5L0.1mol•L-1盐酸 | D. | 2L0.1mol•L-1NaOH溶液 |
16.常温下,某溶液中由水电离出的c(H+)=1×10-30 mol•L-1,该溶液中溶质不可能是( )
| A. | KHSO4 | B. | Fe2(SO4)3 | C. | KOH | D. | HNO3 |
15.氮化硅是一种新型陶瓷材料,它可由石英与焦炭在氮气流中通过以下反应制得:3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)△H>0.根据化学平衡移动原理,理论上该反应的反应条件应为( )
| A. | 高温高压 | B. | 低温低压 | C. | 高温低压 | D. | 低温高压 |
14.下列过程或现象与盐类水解无关的是( )
0 161065 161073 161079 161083 161089 161091 161095 161101 161103 161109 161115 161119 161121 161125 161131 161133 161139 161143 161145 161149 161151 161155 161157 161159 161160 161161 161163 161164 161165 161167 161169 161173 161175 161179 161181 161185 161191 161193 161199 161203 161205 161209 161215 161221 161223 161229 161233 161235 161241 161245 161251 161259 203614
| A. | 使用热的纯碱溶液去油污 | B. | 浓氨水有刺激性气味 | ||
| C. | 明矾、氯化铁常用于净水 | D. | 硫化钠溶液有臭味 |