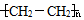6.含有Na+浓度为0.5mol•L-1某无色透明澄清溶液中,还可能含有表中的若干种离子.
已知:
①H2SiO3为不溶于水的胶状沉淀,加热时分解为两种氧化物;
②CaSiO3 BaSiO3不溶于水.
现取该溶液100mL进行如下实验:
回答下列问题.
(1)实验Ⅰ能确定一定不存在的离子是Ca2+、Ba2+
(2)实验Ⅰ中生成气体的离子方程式为CO32-+2H+=CO2↑+H2O
(3)据实验Ⅲ可知一定不存在的离子是SO42-
(4)某同学认为该溶液中一定存在K+,其理由是若无钾离子,阴离子带的电荷总数大于阳离子所带的电荷总数;据上述数据,c(K+)应不小于0.8mol/L.
| 阳离子 | K+ | Fe2+ | Ca2+ | Ba2+ |
| 阴离子 | NO3- | CO3-2 | SiO32- | SO42- |
①H2SiO3为不溶于水的胶状沉淀,加热时分解为两种氧化物;
②CaSiO3 BaSiO3不溶于水.
现取该溶液100mL进行如下实验:
| 序号 | 实验内容 | 实验结果 |
| Ⅰ | 向该溶液中加入足量稀盐酸 | 产生白色胶状沉淀并放出标准状况下0.56L气体 |
| Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4g |
| Ⅲ | 向Ⅱ的滤液中滴加BaCl2溶液 | 无明显现象 |
(1)实验Ⅰ能确定一定不存在的离子是Ca2+、Ba2+
(2)实验Ⅰ中生成气体的离子方程式为CO32-+2H+=CO2↑+H2O
(3)据实验Ⅲ可知一定不存在的离子是SO42-
(4)某同学认为该溶液中一定存在K+,其理由是若无钾离子,阴离子带的电荷总数大于阳离子所带的电荷总数;据上述数据,c(K+)应不小于0.8mol/L.
17.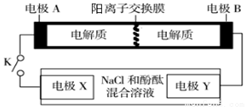 某二次电池充、放电的化学方程式为:2K2S2+KI3$?_{充电}^{放电}$ K2S4+3KI.与其它设备连接的电路如图所示.当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )
某二次电池充、放电的化学方程式为:2K2S2+KI3$?_{充电}^{放电}$ K2S4+3KI.与其它设备连接的电路如图所示.当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )
0 160762 160770 160776 160780 160786 160788 160792 160798 160800 160806 160812 160816 160818 160822 160828 160830 160836 160840 160842 160846 160848 160852 160854 160856 160857 160858 160860 160861 160862 160864 160866 160870 160872 160876 160878 160882 160888 160890 160896 160900 160902 160906 160912 160918 160920 160926 160930 160932 160938 160942 160948 160956 203614
 某二次电池充、放电的化学方程式为:2K2S2+KI3$?_{充电}^{放电}$ K2S4+3KI.与其它设备连接的电路如图所示.当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )
某二次电池充、放电的化学方程式为:2K2S2+KI3$?_{充电}^{放电}$ K2S4+3KI.与其它设备连接的电路如图所示.当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )| A. | 放电时,电极A发生还原反应 | |
| B. | A的电极反应式为:3I--2e-=I3- | |
| C. | 当有0.1 mol K+通过离子交换膜,X电极上产生气体1.12 L(标准状况下 | |
| D. | 电池充电时,B电极要与外电源的正极相连,电极上发生还原反应 |

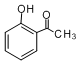 ;②
;②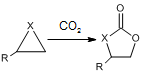 ( X=O,N,S;R为烃基); ③RCOOR+2R′OH→R′COOR′+2ROH
( X=O,N,S;R为烃基); ③RCOOR+2R′OH→R′COOR′+2ROH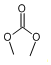 .
.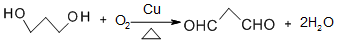 .
.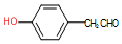 .
.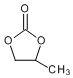 的合成路线.
的合成路线.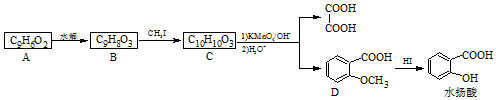

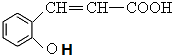 +CH3I→
+CH3I→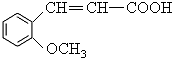 +HI,该反应类型为取代反应,该反应步骤的目的是保护酚羟基,使之不被氧化.
+HI,该反应类型为取代反应,该反应步骤的目的是保护酚羟基,使之不被氧化.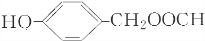 或
或 .
.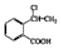 合成
合成 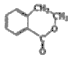 (用反应流程图表示,并注明反应条件).
(用反应流程图表示,并注明反应条件).