9.乙苯( )的二氯代物共有( )
)的二氯代物共有( )
 )的二氯代物共有( )
)的二氯代物共有( )| A. | 15种 | B. | 12种 | C. | 9种 | D. | 6种 |
7.下列说法正确的是( )
| A. | 检验NH4+时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验逸出的气体 | |
| B. | 碘易升华,可用加热升华法除去NH4Cl混有的I2 | |
| C. | 铁在硫蒸气中燃烧生成Fe2S3 | |
| D. | 在过氧化钠与水的反应,毎生成0.1mol氧气,转移电子的数目为0.2NA |
2.表为元素周期表的一部分.
回答下列问题
(1)表中元素原子半径最大的是(写元素符号)Si,Z原子核外电子能量最高的电子亚层是3p.
(2)下列事实能说明Y元素的非金属性比S元素的非金属性强的是ac
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(3)碳酸钠溶液中滴入酚酞,溶液显红色,请用离子方程式解释产生该现象的原因:CO32-+H2O?HCO3-+OH-;在上述红色的溶液中加入少许氯化钙固体,溶液颜色变浅,请用平衡理论解释产生该现象的原因Ca2++CO32-=CaCO3↓,导致溶液中碳酸根离子浓度减少,水解平衡向逆反应方向移动,氢氧根离子浓度减少,碱性减弱.
(4)硫酸工业生产中接触室内发生的反应方程式为2SO2+O2$?_{△}^{催化剂}$2SO3;在实际生产中,操作温度选定400-500℃、压强通常采用常压的原因分别是催化剂在400~500℃时,活性最大,在常压下及400~500℃时,二氧化硫的转化率已经很高,若加压会增加设备、投资和能量消耗.
0 160735 160743 160749 160753 160759 160761 160765 160771 160773 160779 160785 160789 160791 160795 160801 160803 160809 160813 160815 160819 160821 160825 160827 160829 160830 160831 160833 160834 160835 160837 160839 160843 160845 160849 160851 160855 160861 160863 160869 160873 160875 160879 160885 160891 160893 160899 160903 160905 160911 160915 160921 160929 203614
| 碳 | 氮 | Y | |
| X | 硫 | Z |
(1)表中元素原子半径最大的是(写元素符号)Si,Z原子核外电子能量最高的电子亚层是3p.
(2)下列事实能说明Y元素的非金属性比S元素的非金属性强的是ac
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(3)碳酸钠溶液中滴入酚酞,溶液显红色,请用离子方程式解释产生该现象的原因:CO32-+H2O?HCO3-+OH-;在上述红色的溶液中加入少许氯化钙固体,溶液颜色变浅,请用平衡理论解释产生该现象的原因Ca2++CO32-=CaCO3↓,导致溶液中碳酸根离子浓度减少,水解平衡向逆反应方向移动,氢氧根离子浓度减少,碱性减弱.
(4)硫酸工业生产中接触室内发生的反应方程式为2SO2+O2$?_{△}^{催化剂}$2SO3;在实际生产中,操作温度选定400-500℃、压强通常采用常压的原因分别是催化剂在400~500℃时,活性最大,在常压下及400~500℃时,二氧化硫的转化率已经很高,若加压会增加设备、投资和能量消耗.
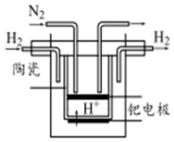 氮的固定对工农业及人类生存具有重大意义.
氮的固定对工农业及人类生存具有重大意义.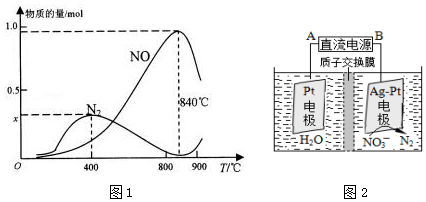
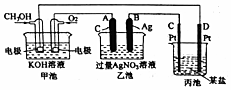

 .
. .
.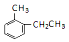 的名称是2-甲基乙苯.
的名称是2-甲基乙苯. +CH3COOH$?_{△}^{浓H_{2}SO_{4}}$
+CH3COOH$?_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O.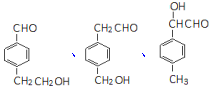 任一种.
任一种.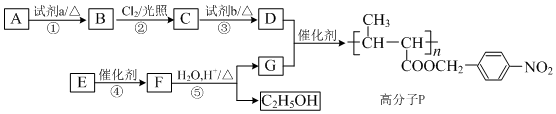
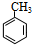 ,
,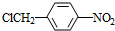 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$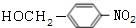 +NaCl.
+NaCl.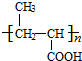 .
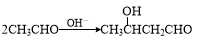
.
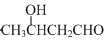 .
.