12.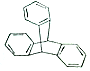 2016年诺贝尔化学奖由法国、美国及荷兰的三位化学家共同获得,以表彰他们在“分子马达”研究方面的成就.最初的“分子马达”的关键组件是三叠烯(如图),下列有关三叠烯的说法正确的是( )
2016年诺贝尔化学奖由法国、美国及荷兰的三位化学家共同获得,以表彰他们在“分子马达”研究方面的成就.最初的“分子马达”的关键组件是三叠烯(如图),下列有关三叠烯的说法正确的是( )
 2016年诺贝尔化学奖由法国、美国及荷兰的三位化学家共同获得,以表彰他们在“分子马达”研究方面的成就.最初的“分子马达”的关键组件是三叠烯(如图),下列有关三叠烯的说法正确的是( )
2016年诺贝尔化学奖由法国、美国及荷兰的三位化学家共同获得,以表彰他们在“分子马达”研究方面的成就.最初的“分子马达”的关键组件是三叠烯(如图),下列有关三叠烯的说法正确的是( )| A. | 分子式为C20H14 | B. | 属于苯的同系物 | ||
| C. | 能与溴水发生加成反应 | D. | 分子中所有原子可能在同一平面上 |
11.可用于判断溶液酸碱性的方法有很多,下列能够说明溶液一定呈碱性的是( )
| A. | 常温下能够使pH试纸显红色的溶液 | B. | 常温下能够使甲基橙显黄色的溶液 | ||
| C. | [OH-]>[H+]的溶液 | D. | 加入MgCl2生成白色沉淀的溶液 |
8.金矿中的单质金,可用电解法在空气中用NaCN溶液提取,试判断下列各项中是阳极反应的为( )
| A. | Au-e-═Au+ | B. | O2+2H2O+4e-═4OH- | ||
| C. | Au-e-+2CN-═Au(CN)2- | D. | 2H2O+2e-═2OH-+H2 |
7.锌和浓度不同的硝酸会发生不同的反应,其中被氧化的锌和被还原的硝酸的微粒个数之比为3:2的是( )
| A. | Zn+HNO3(浓)--Zn(NO3)2+NO2↑+H2O | B. | Zn+HNO3(浓)--Zn(NO3)2+NO↑+H2O | ||
| C. | Zn+HNO3(很稀)--Zn(NO3)2+NO2↑+H2O | D. | Zn+HNO3(很稀)--Zn(NO3)2+NH4NO3+H2O |
6.短周期主族元素Q、W、X、Y、Z原子序数依次增大,Q原子的最外层电子数是其内层电子总数的3倍,W是非金属性最强的元素,X的原子半径在短周期主族元素中为最大,Y是地壳中含量最多的金属元素,Z与Q同主族.下列叙述正确的是( )
| A. | 原子半径;r(Z)>r(W)>r(Q) | |
| B. | 气态氢化物的热稳定性:W>Q>Z | |
| C. | X与Z形成的化合物呈碱性的原因:Z2-+2H2O?H2Z+2OH- | |
| D. | Y与Z的二元化合物可以在溶液中通过复分解反应制得 |
4.在酸性溶液中,Fe2O42-易转化为Fe2+,其反应过程为Fe2O42-+H+-Fe2++H2O.现有KMnO4、Na2CO3、Cu2O、HNO3四种物质,其中一种物质能使上述反应发生,下列说法正确的是( )
| A. | 能使上述反应发生的物质是KMnO4 | |
| B. | 该氧化还原反应的离子方程式中水的计量数为5 | |
| C. | 该氧化还原反应中氧化剂是Fe2O42-,发生氧化反应 | |
| D. | 有1mol还原剂参与反应时,转移4NA个电子 |
3.某温度下,在体积一定的密闭容器中充入等物质的量的X和Y气体发生反应:X(g)+Y(g)?Z(g)+W(s)△H>0并达到平衡,若改变条件,下列叙述正确的是( )
0 160644 160652 160658 160662 160668 160670 160674 160680 160682 160688 160694 160698 160700 160704 160710 160712 160718 160722 160724 160728 160730 160734 160736 160738 160739 160740 160742 160743 160744 160746 160748 160752 160754 160758 160760 160764 160770 160772 160778 160782 160784 160788 160794 160800 160802 160808 160812 160814 160820 160824 160830 160838 203614
| A. | 加入少量W,逆反应速率增大,平衡左移 | |
| B. | 升高温度,混合气体的平均相对分子质量减小 | |
| C. | 加入Z,平衡左移,反应达到新的平衡时,体系中X的百分含量减小 | |
| D. | 反应达到平衡后再加入X,平衡右移,△H增大 |
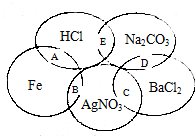 如图为一五元环图案,小明在图案上依次写了五种物质,图中相交的两种物质均可发生化学反应,A、B、C、D、E表示其相应的化学反应.请回答下列问题:
如图为一五元环图案,小明在图案上依次写了五种物质,图中相交的两种物质均可发生化学反应,A、B、C、D、E表示其相应的化学反应.请回答下列问题: