题目内容
9.取0.10mol•L-1的某一元弱酸(HA)50.0mL与20.0mL 0.10mol•L-1 KOH溶液混合将混合液稀释至100mL,测得此溶液的pH为5.25,问此一元弱酸(HA)的Ka值是多少?分析 该一元弱酸HA的Ka=$\frac{c({A}^{-})•c({H}^{+})}{c(HA)}$,分别计算出稀释溶液中c(HA)、c(A-)的浓度,然后带入表达式计算即可.
解答 解:混合溶液中c(HA)≈$\frac{0.10mol/L×0.05L-0.10mol/L×0.02L}{0.1L}$=0.03mol/L,c(A-)≈c(KA)=$\frac{0.10mol/L×0.02L}{0.1L}$=0.02mol/L,c(H+)=10-5.25mol/L,
则Ka=$\frac{c({A}^{-})•c({H}^{+})}{c(HA)}$=$\frac{0.02×1{0}^{-5.25}}{0.03}$≈3.75×10-6,
答:该一元弱酸(HA)的Ka值是3.75×10-6.
点评 本题考查酸碱混合的计算,题目难度中等,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握电离平衡常数的概念及表达式,试题培养了学生的化学计算能力.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
6.己知:100℃的溫度下,水的离子积Kw=1×10-12.下列说法正确的是( )
| A. | 0.05mol/L 的 H2SO4溶液 PH=1 | |
| B. | 0.001mol/L 的 NaOH溶液 PH=11 | |
| C. | 0.005mol/L的H2SO4溶液与0.0lmol/LNaOH溶液等体积浪合,混合液pH=6,溶液呈酸性 | |
| D. | 完全中和PH=3的H2SO4溶液50mL,需要pH=11的NaOH溶液50mL |
4.在酸性溶液中,Fe2O42-易转化为Fe2+,其反应过程为Fe2O42-+H+-Fe2++H2O.现有KMnO4、Na2CO3、Cu2O、HNO3四种物质,其中一种物质能使上述反应发生,下列说法正确的是( )
| A. | 能使上述反应发生的物质是KMnO4 | |
| B. | 该氧化还原反应的离子方程式中水的计量数为5 | |
| C. | 该氧化还原反应中氧化剂是Fe2O42-,发生氧化反应 | |
| D. | 有1mol还原剂参与反应时,转移4NA个电子 |
14.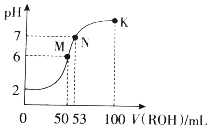 在常温下,向50mL0.01mol•L-1HCl溶液中逐滴加入0.01mol•L-1ROH溶液,如图所示的曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法不正确的是( )
在常温下,向50mL0.01mol•L-1HCl溶液中逐滴加入0.01mol•L-1ROH溶液,如图所示的曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法不正确的是( )
 在常温下,向50mL0.01mol•L-1HCl溶液中逐滴加入0.01mol•L-1ROH溶液,如图所示的曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法不正确的是( )
在常温下,向50mL0.01mol•L-1HCl溶液中逐滴加入0.01mol•L-1ROH溶液,如图所示的曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法不正确的是( )| A. | ROH为一元弱碱 | |
| B. | M点溶液呈酸性的原因是R++H2O?ROH+H+ | |
| C. | M、N、K三点水的电离程度逐渐减小 | |
| D. | K点溶液中离子浓度c(Cl-)>c(R+)>c(OH-)>c(H+) |
1.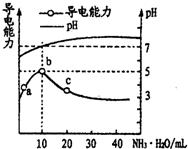 常温下,向10mL0.1mol/L的HR溶液中逐滴滴人0.1mol/L的NH3•H2O溶液,所得溶液pH及导电性变化如图.下列分析正确的是( )
常温下,向10mL0.1mol/L的HR溶液中逐滴滴人0.1mol/L的NH3•H2O溶液,所得溶液pH及导电性变化如图.下列分析正确的是( )
 常温下,向10mL0.1mol/L的HR溶液中逐滴滴人0.1mol/L的NH3•H2O溶液,所得溶液pH及导电性变化如图.下列分析正确的是( )
常温下,向10mL0.1mol/L的HR溶液中逐滴滴人0.1mol/L的NH3•H2O溶液,所得溶液pH及导电性变化如图.下列分析正确的是( )| A. | a→b点导电能力增强,说明HR为弱酸 | |
| B. | b点溶液的pH=5,此时酸碱恰好中和 | |
| C. | c点溶液存在c(OH-)>c(H+) | |
| D. | a、b、c三点NH3•H2O的电离常数均相等 |
18.下列各组离子在溶液中按括号内的物质的量之比混合,得到无色、澄清溶液的是( )
| A. | Fe3+、Na+、Cl-、S2-(1:2:3:1) | B. | NH4+、Ba2+、OH-、NO3-(1:1:1:2) | ||
| C. | K+、H+、I-、AlO2-(1:1:1:1) | D. | Na+、Al3+、Cl-、OH-(4:1:4:3) |
19.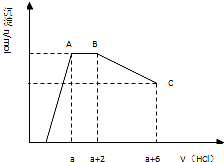 某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示(已知::AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-)),下列结论不正确的是( )
某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示(已知::AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-)),下列结论不正确的是( )
 某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示(已知::AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-)),下列结论不正确的是( )
某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示(已知::AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-)),下列结论不正确的是( )| A. | 溶液中一定不存在的离子:Fe3+,Mg2+,Al3+ | |
| B. | AB段可得到能使澄清的石灰水变浑浊的气体 | |
| C. | c(CO32-):c(AlO2-)=2:3 | |
| D. | BC段发生反应的离子方程式为Al(OH)3+3H+═Al3++3H2O |
