4.某同学拟用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取无水氯化铜,流程如图所示:
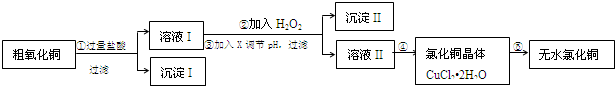
(1)步骤①中氧化铜与盐酸反应的离子方程式:CuO+2H+=Cu2++H2O.
(2)步骤②中加入H2O2的是为了将Fe2+氧化成Fe3+,Fe2+与H2O2在酸性溶液中反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)已知:
步骤③中调节pH的最佳范围为3.2-4.7,
步骤③中可以用于调节溶液pH的试剂X是bc:
a.NaOH b.CuO c. Cu(OH)2 d.NH3•H2O
(4)步骤⑤中要得到无水CuCl2,需要在干燥的HCl气流中加热CuCl2•2H2O,原因是在干燥的HCl气流中抑制Cu2+的水解,且带走CuCl2•xH2O受热产生的水气,故能得到无水氯化铜.

(1)步骤①中氧化铜与盐酸反应的离子方程式:CuO+2H+=Cu2++H2O.
(2)步骤②中加入H2O2的是为了将Fe2+氧化成Fe3+,Fe2+与H2O2在酸性溶液中反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)已知:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
| Fe2+ | 7.0 | 9.0 |
步骤③中可以用于调节溶液pH的试剂X是bc:
a.NaOH b.CuO c. Cu(OH)2 d.NH3•H2O
(4)步骤⑤中要得到无水CuCl2,需要在干燥的HCl气流中加热CuCl2•2H2O,原因是在干燥的HCl气流中抑制Cu2+的水解,且带走CuCl2•xH2O受热产生的水气,故能得到无水氯化铜.
3.孔雀石主要成分为Cu2(OH)2CO3,还含少量铁氧化物和硅氧化物.以下是实验室以孔雀石为原料制备CuSO4•5H2O晶体流程图:
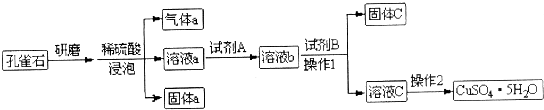
根据实验设计流程和实验目的,判断下列说法中错误的是( )
0 160479 160487 160493 160497 160503 160505 160509 160515 160517 160523 160529 160533 160535 160539 160545 160547 160553 160557 160559 160563 160565 160569 160571 160573 160574 160575 160577 160578 160579 160581 160583 160587 160589 160593 160595 160599 160605 160607 160613 160617 160619 160623 160629 160635 160637 160643 160647 160649 160655 160659 160665 160673 203614

根据实验设计流程和实验目的,判断下列说法中错误的是( )
| A. | 研磨孔雀石的目的是增大固体表面积,从而加快反应速率 | |
| B. | 试剂A目的是将溶液中Fe2+转化为Fe3+,可选用双氧水作氧化剂 | |
| C. | 试剂B目的是作pH调节剂,使Fe3+转化为沉淀 | |
| D. | 试剂B可以选择NaOH或氨水等碱性试剂 |
 甲醇作为基本的有机化工产品和环保动力燃料具有广阔的应用前景,二氧化碳加氢合成甲醇是合理利用二氧化碳的有效途径.由二氧化碳制备甲醇过程中可能涉及反应如下:
甲醇作为基本的有机化工产品和环保动力燃料具有广阔的应用前景,二氧化碳加氢合成甲醇是合理利用二氧化碳的有效途径.由二氧化碳制备甲醇过程中可能涉及反应如下: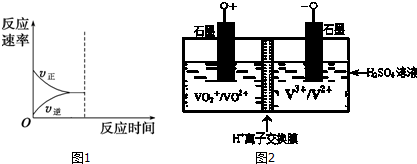


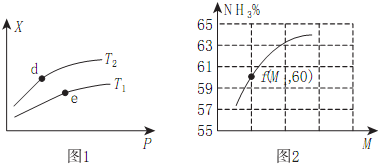 已知有关热化学方程式为:①4NH3(g)+5O2(g)4NO(g)+6H2O(g)△H=-905kJ/mol;②3H2(g)+N2(g)2NH3(g)△H=-92.4kJ/mol;③2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol;④N2(g)+O2(g)=2NO(g)△H=QkJ/mol;反应①中有关化学键的键能(kJ/mol)如下:H-O:463,H-N:391,O=O:497
已知有关热化学方程式为:①4NH3(g)+5O2(g)4NO(g)+6H2O(g)△H=-905kJ/mol;②3H2(g)+N2(g)2NH3(g)△H=-92.4kJ/mol;③2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol;④N2(g)+O2(g)=2NO(g)△H=QkJ/mol;反应①中有关化学键的键能(kJ/mol)如下:H-O:463,H-N:391,O=O:497 图示装置可用来制取和观察Fe(OH)2在空气中被氧化时的颜色变化.实验时必须使用的药品是铁屑和6mol•L-1的硫酸,其它试剂任选.
图示装置可用来制取和观察Fe(OH)2在空气中被氧化时的颜色变化.实验时必须使用的药品是铁屑和6mol•L-1的硫酸,其它试剂任选.