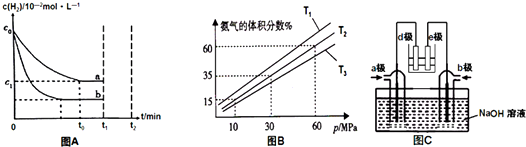
8.雾霾天气中SO2是造成空气污染的主要原因;在硫酸工业生产过程中2SO2(g)+O2(g)?2SO3(g)是关键步骤.该反应的过程在600℃时的平衡常数K=19,有关的能量变化,实验数据如图所示.
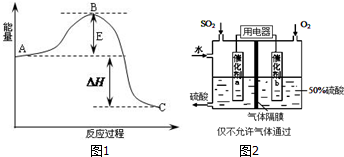
(1)已知1mol SO2(g)氧化为1mol SO3(g)时的△H=-99kJ/mol.则图中△H=198 kJ/mol; E代表的意义是正反应活化能.结合表中的数据解释该反应是放热反应的原因:压强一定时,温度升高,SO2转化率下降,说明升温有利于逆反应进行,所以正反应为放热反应;若600℃时,在一密闭容器中,将二氧化硫和氧气混合,当测得容器内c(SO2)=0.3mol/L,c(O2)=0.1mol/L,c(SO3)=0.4mol/L,在这种情况下,化学反应速率是v(正)> v(逆)(填“>”、“<”或“=”).
(2)硫酸工厂尾气处理时用NaOH溶液吸收SO2生成NaHSO3.已知在0.1mol/L的NaHSO3溶液中有关微粒浓度由大到小的顺序为c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3).该溶液中c(H+)>c(OH-)(填“>”、“<”或“=”),简述理由(用简单的文字和离子方程式说明):NaHSO3溶液中存在反应:HSO3-?H++SO32-、HSO3-+H2O?OH-+H2SO3,由于c(SO32-)>c(H2SO3),所以电离程度大于水解.
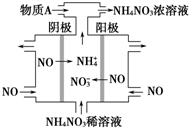
(3)有人设想用电化学原理生产硫酸(装置见图2),写出通入SO2的电极的电极反应式:SO2+2H2O-2e-=SO42-+4H+;为稳定持续生产,硫酸溶液的浓度应维持不变,则通入SO2和水的质量比为16:29.
0 160102 160110 160116 160120 160126 160128 160132 160138 160140 160146 160152 160156 160158 160162 160168 160170 160176 160180 160182 160186 160188 160192 160194 160196 160197 160198 160200 160201 160202 160204 160206 160210 160212 160216 160218 160222 160228 160230 160236 160240 160242 160246 160252 160258 160260 160266 160270 160272 160278 160282 160288 160296 203614

| 压强/Mpa 转化率/% 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
(2)硫酸工厂尾气处理时用NaOH溶液吸收SO2生成NaHSO3.已知在0.1mol/L的NaHSO3溶液中有关微粒浓度由大到小的顺序为c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3).该溶液中c(H+)>c(OH-)(填“>”、“<”或“=”),简述理由(用简单的文字和离子方程式说明):NaHSO3溶液中存在反应:HSO3-?H++SO32-、HSO3-+H2O?OH-+H2SO3,由于c(SO32-)>c(H2SO3),所以电离程度大于水解.
(3)有人设想用电化学原理生产硫酸(装置见图2),写出通入SO2的电极的电极反应式:SO2+2H2O-2e-=SO42-+4H+;为稳定持续生产,硫酸溶液的浓度应维持不变,则通入SO2和水的质量比为16:29.
 2015年3月,全国“两会”代表委员就我国“雾霾”治理积极建言献策.科学家研究表明氮氧化物与悬浮在大气中的盐粒子相互作用时能产生“二次雾霾”,涉及的反应有:
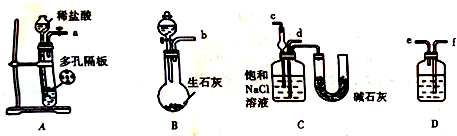
2015年3月,全国“两会”代表委员就我国“雾霾”治理积极建言献策.科学家研究表明氮氧化物与悬浮在大气中的盐粒子相互作用时能产生“二次雾霾”,涉及的反应有: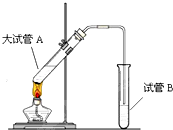 在实验室,可以用如图所示的装置制取乙酸乙酯.请回答下列问题:
在实验室,可以用如图所示的装置制取乙酸乙酯.请回答下列问题: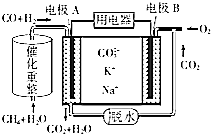 CH4和H2O(g)可发生催化重整反应:CH4(g)+H2O(g)?CO(g)+3H2(g).
CH4和H2O(g)可发生催化重整反应:CH4(g)+H2O(g)?CO(g)+3H2(g).

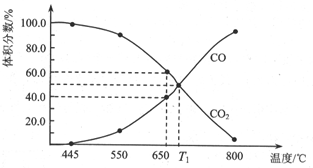 一定量的CO2与足量的C在恒容密闭容器中发生反应:C(s)+CO2(g)?2CO(g)△H.
一定量的CO2与足量的C在恒容密闭容器中发生反应:C(s)+CO2(g)?2CO(g)△H.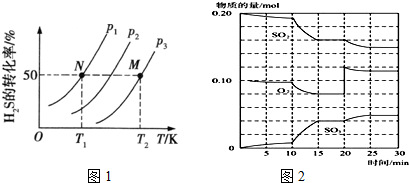
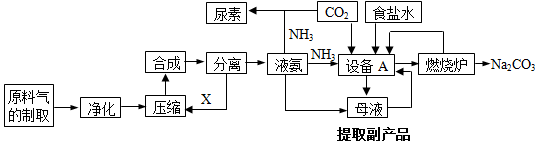
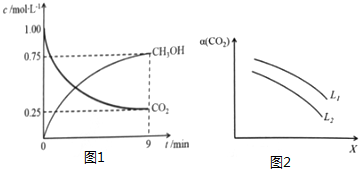 随着能源与环境问题越来越被人们关注,碳一化学(C1化学)成为研究的热点..“碳一化学”即以单质碳及CO、CO2、CH4、CH3OH等含一个碳原子的物质为原料合成工业产品的化学与工艺.(1)将CO2转化成有机物可有效实现碳循环.CO2转化成有机物的例子很多,如:
随着能源与环境问题越来越被人们关注,碳一化学(C1化学)成为研究的热点..“碳一化学”即以单质碳及CO、CO2、CH4、CH3OH等含一个碳原子的物质为原料合成工业产品的化学与工艺.(1)将CO2转化成有机物可有效实现碳循环.CO2转化成有机物的例子很多,如: