11.下述反应在密闭容器中已建立平衡:SO2(气)+NO2(气)?NO(气)+SO3(气)若向容器中通入一定量的氧气,此时会发生的变化是( )
| A. | 平衡向正反应方向移动 | |
| B. | 平衡向逆反应方向移动 | |
| C. | 平衡不移动,但容器内的压强将增大 | |
| D. | 平衡不移动,且容器内的压强不变 |
10.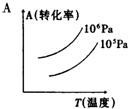 有一化学平衡mA(g)+nB(g)═PC(g)+qD(g),如图表示的转化率与压强、温度的关系.由此得出的正确结论是( )
有一化学平衡mA(g)+nB(g)═PC(g)+qD(g),如图表示的转化率与压强、温度的关系.由此得出的正确结论是( )
 有一化学平衡mA(g)+nB(g)═PC(g)+qD(g),如图表示的转化率与压强、温度的关系.由此得出的正确结论是( )
有一化学平衡mA(g)+nB(g)═PC(g)+qD(g),如图表示的转化率与压强、温度的关系.由此得出的正确结论是( )| A. | 正反应是吸热反应,(m+n)>(p+q) | B. | 正反应是吸热反应,(m+n)<(p+q) | ||
| C. | 正反应是放热反应,(m+n)>(p+q) | D. | 正反应是放热反应,(m+n)<(p+q) |
9.可逆反应aA(g)+bB(g)?cC(g)+dD(g)△H=Q,同时符合下列两图中各曲线的规律是( )
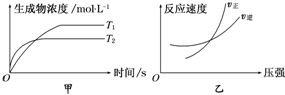

| A. | a+b>c+d T1>T2△H>0 | B. | a+b>c+d T1<T2 △H<0 | ||
| C. | a+b<c+d T1>T2△H>0 | D. | a+b>c+d T1>T2△H<0 |
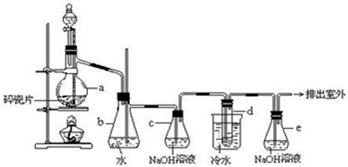
8. 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:
可能用到的有关数据如下:
合成反应:在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸.b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.
分离提纯:反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙.最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置a的名称是蒸馏烧瓶.
(2)加入碎瓷片的作用是;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加B.冷却后补加C.不需补加D.重新配料
(3)分液漏斗在使用前须清洗干净并;在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口放出”).
(4)分离提纯过程中加入无水氯化钙的目的是吸收水.
(5)在环己烯粗产物蒸馏过程中,可能用到的仪器有BE(填正确答案标号).
A圆底烧瓶 B温度计 C漏斗 D玻璃棒 E接收器
(6)本实验所得到的环己烯产率是61%.(保留两位有效数字)
(注:产率=实际产量/理论产量×100%)
 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:可能用到的有关数据如下:
| 相对分子质量 | 密度/(g•cm3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
分离提纯:反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙.最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置a的名称是蒸馏烧瓶.
(2)加入碎瓷片的作用是;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加B.冷却后补加C.不需补加D.重新配料
(3)分液漏斗在使用前须清洗干净并;在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口放出”).
(4)分离提纯过程中加入无水氯化钙的目的是吸收水.
(5)在环己烯粗产物蒸馏过程中,可能用到的仪器有BE(填正确答案标号).
A圆底烧瓶 B温度计 C漏斗 D玻璃棒 E接收器
(6)本实验所得到的环己烯产率是61%.(保留两位有效数字)
(注:产率=实际产量/理论产量×100%)
7.自然界地表层存在大量铁、铜的硫化物.现制得含氯化亚铁杂质的氯化铜水溶液,为制取纯净的CuCl2•2H2O,首先将其制成水溶液,然后按如图步骤进行提纯.
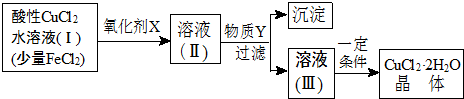
已知Cu2+、Fe3+和Fe2+的氢氧化物开始和完全沉淀时的pH,见表.请回答:
(1)加入氧化剂的目的是将Fe2+氧化为Fe3+,便于生成沉淀而与Cu2+分离.
(2)最适合作氧化剂X的是C(填序号).
A.K2Cr2O7 B.NaClO
C.H2O2 D.KMnO4
在酸性条件下,氧化剂X与Fe2+反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2 H2O.
(3)加入的物质Y以调节溶液pH,Y的化学式是CuO或Cu(OH)2或CuCO3或Cu2(OH)2CO3,pH的范围是调节溶液的pH至3.2~4.7.
(4)只能在HCl气流中加热浓缩才能得到CuCl2•2H2O晶体,HCl气流起的作用是:防止加热过程中CuCl2发生水解生成Cu (OH)2.
(5)已知Ksp(ZnS)>Ksp(CuS).地表层原生铜的硫化物经氧化、水浸作用后变成CuSO4溶液,再向地下深层渗透,遇到难溶的ZnS慢慢转变为铜蓝(CuS).用离子方程式解释ZnS能转变为CuS的原因Cu2+(aq)+ZnS(s)═Zn2+(aq)+CuS(s).

已知Cu2+、Fe3+和Fe2+的氢氧化物开始和完全沉淀时的pH,见表.请回答:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 9 | 6.7 |
(2)最适合作氧化剂X的是C(填序号).
A.K2Cr2O7 B.NaClO
C.H2O2 D.KMnO4
在酸性条件下,氧化剂X与Fe2+反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2 H2O.
(3)加入的物质Y以调节溶液pH,Y的化学式是CuO或Cu(OH)2或CuCO3或Cu2(OH)2CO3,pH的范围是调节溶液的pH至3.2~4.7.
(4)只能在HCl气流中加热浓缩才能得到CuCl2•2H2O晶体,HCl气流起的作用是:防止加热过程中CuCl2发生水解生成Cu (OH)2.
(5)已知Ksp(ZnS)>Ksp(CuS).地表层原生铜的硫化物经氧化、水浸作用后变成CuSO4溶液,再向地下深层渗透,遇到难溶的ZnS慢慢转变为铜蓝(CuS).用离子方程式解释ZnS能转变为CuS的原因Cu2+(aq)+ZnS(s)═Zn2+(aq)+CuS(s).
3.一氯甲烷(CH3C1)是一种重要的化工原料,常温下它是无色有毒气体,微溶于水,易溶于乙醇、CCl4等.(1)甲组同学在实验室用图1所示装置模拟催化法制备和收集一氯甲烷.
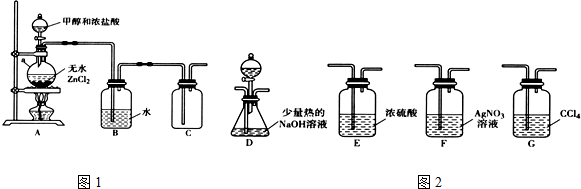
①无水ZnCl2为催化剂,a瓶中发生反应的化学方程式为CH3OH+HCl$→_{△}^{ZnCl_{2}}$CH3Cl+H2O.
②装置B的主要作用是除去氯化氢气体.
③收集到的CH3Cl气体在氧气中充分燃烧,产物用过量的V1mL、c1mol•L-1NaOH溶液充分吸收,以甲基橙作指示剂,用c2 mol•L-1盐酸标准液对吸收液进行返滴定(发生的反应为:
NaOH+HCl=NaCl+H2O,Na2CO3+2HCl=2NaCl+2CO2↑+2H2O),最终消耗V2mL盐酸.则所收集CH3Cl的物质的量为(c1V1-c2V2)×10-3 _ mol.(已知:2CH3Cl+3O2$\stackrel{点燃}{→}$2CO2+2H2O+2HCl)
(2)乙组同学选用甲组A、B装置和图2所示的部分装置检验CH3Cl中的氯元素.
(已知:一卤代烷一般要在加热条件下才能与氢氧化钠溶液反应)
①乙组同学的实验装置中,依次连接的合理顺序为A→B→F→D→G.
②通入一段时间的CH3Cl气体,打开装置D中分液漏斗的活塞,观察实验现象.分液漏斗中盛放的试剂是硝酸和硝酸银溶液.
③能证明CH3Cl中含有氯元素的实验现象是F中无白色沉淀生成,D中有白色沉淀生成.
(3)查阅资料可知:AgNO3的乙醇溶液可以检验CH3X中的卤素原子.相关数据如表:
①CH3X通入AgNO3的乙醇溶液中,除有沉淀生成外,还生成硝酸甲酯,请写出硝酸甲酯的结构简式:CH3ONO2.
③将CH3Cl和CH3Br的混合气体通入AgNO3的乙醇溶液中,先出现淡黄色沉淀.请依据表中数据解释原因C-Br键的键能小,更容易断裂,同时溴化银的溶度积常数更小,溴化银更容易形成沉淀.

①无水ZnCl2为催化剂,a瓶中发生反应的化学方程式为CH3OH+HCl$→_{△}^{ZnCl_{2}}$CH3Cl+H2O.
②装置B的主要作用是除去氯化氢气体.
③收集到的CH3Cl气体在氧气中充分燃烧,产物用过量的V1mL、c1mol•L-1NaOH溶液充分吸收,以甲基橙作指示剂,用c2 mol•L-1盐酸标准液对吸收液进行返滴定(发生的反应为:
NaOH+HCl=NaCl+H2O,Na2CO3+2HCl=2NaCl+2CO2↑+2H2O),最终消耗V2mL盐酸.则所收集CH3Cl的物质的量为(c1V1-c2V2)×10-3 _ mol.(已知:2CH3Cl+3O2$\stackrel{点燃}{→}$2CO2+2H2O+2HCl)
(2)乙组同学选用甲组A、B装置和图2所示的部分装置检验CH3Cl中的氯元素.
(已知:一卤代烷一般要在加热条件下才能与氢氧化钠溶液反应)
①乙组同学的实验装置中,依次连接的合理顺序为A→B→F→D→G.
②通入一段时间的CH3Cl气体,打开装置D中分液漏斗的活塞,观察实验现象.分液漏斗中盛放的试剂是硝酸和硝酸银溶液.
③能证明CH3Cl中含有氯元素的实验现象是F中无白色沉淀生成,D中有白色沉淀生成.
(3)查阅资料可知:AgNO3的乙醇溶液可以检验CH3X中的卤素原子.相关数据如表:
| 化学键 | C-Cl | C-Br |
| 键能(kJ•mol-1) | 330 | 276 |
| 化合物 | AgCl | AgBr |
| Ksp近似值 | 1.8×10-10 | 5×10-13 |
③将CH3Cl和CH3Br的混合气体通入AgNO3的乙醇溶液中,先出现淡黄色沉淀.请依据表中数据解释原因C-Br键的键能小,更容易断裂,同时溴化银的溶度积常数更小,溴化银更容易形成沉淀.
2.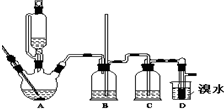 实验室制备1,2二溴乙烷的反应原理如下:
实验室制备1,2二溴乙烷的反应原理如下:
①CH3-CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2═CH2↑+H2O
②CH2═CH2+Br2→BrCH2CH2Br(1,2-二溴乙烷)
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:有关数据列表如下:
(1)在此实验中,要迅速地把反应温度提高到170℃左右,其最主要目的是d;
a.引发反应b.加快反应速度 c.防止乙醇挥发d.减少副产物乙醚生成
(2)在装置C中应加入c,其目的是吸收反应中可能生成的酸性气体;
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去.
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后产物应在下层(填“上”、“下”);
(5)若产物中有少量未反应的Br2,最好用b洗涤除去;
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚,可用蒸馏的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.
0 159717 159725 159731 159735 159741 159743 159747 159753 159755 159761 159767 159771 159773 159777 159783 159785 159791 159795 159797 159801 159803 159807 159809 159811 159812 159813 159815 159816 159817 159819 159821 159825 159827 159831 159833 159837 159843 159845 159851 159855 159857 159861 159867 159873 159875 159881 159885 159887 159893 159897 159903 159911 203614
 实验室制备1,2二溴乙烷的反应原理如下:
实验室制备1,2二溴乙烷的反应原理如下:①CH3-CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2═CH2↑+H2O
②CH2═CH2+Br2→BrCH2CH2Br(1,2-二溴乙烷)
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
a.引发反应b.加快反应速度 c.防止乙醇挥发d.减少副产物乙醚生成
(2)在装置C中应加入c,其目的是吸收反应中可能生成的酸性气体;
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去.
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后产物应在下层(填“上”、“下”);
(5)若产物中有少量未反应的Br2,最好用b洗涤除去;
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚,可用蒸馏的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.
 ;BA4的结构式
;BA4的结构式 .
. .
. 某学习小组探究溴乙烷的消去反应并验证产物.
某学习小组探究溴乙烷的消去反应并验证产物.