��Ŀ����
9�����淴ӦaA��g��+bB��g��?cC��g��+dD��g����H=Q��ͬʱ����������ͼ�и����ߵĹ����ǣ�������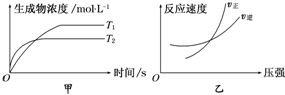
| A�� | a+b��c+d��T1��T2��H��0 | B�� | a+b��c+d��T1��T2 ��H��0 | ||
| C�� | a+b��c+d��T1��T2��H��0 | D�� | a+b��c+d��T1��T2��H��0 |
���� �ɼ�ͼ��֪��T2�ȴﵽƽ�⣬��T1��T2�����¶ȸ�ʱ������Ũ�ȵͣ���֪�����¶�ƽ�������ƶ���
����ͼ��֪���ڽ���������Ӧ���ʴ����淴Ӧ���ʣ���֪����ѹǿƽ�������ƶ����Դ������
��� �⣺�ɼ�ͼ��֪��T2�ȴﵽƽ�⣬��T1��T2�����¶ȸ�ʱ������Ũ�ȵͣ���֪�����¶�ƽ�������ƶ�����������ӦΪ���ȷ�Ӧ������H��0��
����ͼ��֪���ڽ���������Ӧ���ʴ����淴Ӧ���ʣ���֪����ѹǿƽ�������ƶ����÷�ӦΪ���������С�ķ�Ӧ����a+b��c+d��
��ѡB��
���� ���⿼�黯ѧƽ���Ӱ�����أ�Ϊ��Ƶ���㣬����ͼ���¶ȡ�ѹǿ��ƽ���ƶ���Ӱ��Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��ͼ��ķ�����ƽ���ƶ��Ľ�ϣ���Ŀ�ѶȲ���

��ϰ��ϵ�д�
 ��ѧʵ����ϵ�д�
��ѧʵ����ϵ�д�
�����Ŀ
20������2L�ܱ������ڣ�800��ʱ������Ӧ��2NO��g��+O2��g��?2NO2��g��������ϵ�У�n��NO����ʱ��ı仯�����
��1��������Ӧ�ڵ�5sʱ��NO��ת����Ϊ65%��
��2����O2��ʾ��0��2 s�ڸ÷�Ӧ��ƽ������v��O2��=0.00125mol/��L•s����
��3����˵���÷�Ӧ�Ѵﵽƽ��״̬����bc��
a��v��NO2��=2v��O2�� b��������ѹǿ���ֲ���
c��v����NO��=2v����O2�� d�������������ܶȱ��ֲ���
���±��е��������ƻ�1mol�����еĻ�ѧ�������ĵ�������
�����������ݻش��������⣺
��4���������ʱ������е�������͵���A��
A��H2 B��Cl2 C��Br2 D��I2
��5�������⻯�������ȶ�����A��
A��HCl B��HBr C��HI
��6��X2+H2=2HX��X����Cl��Br��I���ķ�Ӧ�����ȷ�Ӧ���Ƿ��ȷ�Ӧ�����ȷ�Ӧ��
| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| NO�����ʵ�����mol�� | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��2����O2��ʾ��0��2 s�ڸ÷�Ӧ��ƽ������v��O2��=0.00125mol/��L•s����
��3����˵���÷�Ӧ�Ѵﵽƽ��״̬����bc��
a��v��NO2��=2v��O2�� b��������ѹǿ���ֲ���
c��v����NO��=2v����O2�� d�������������ܶȱ��ֲ���
���±��е��������ƻ�1mol�����еĻ�ѧ�������ĵ�������
| ���� | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| ������kJ�� | 243 | 193 | 151 | 431 | 366 | 298 | 436 |
��4���������ʱ������е�������͵���A��
A��H2 B��Cl2 C��Br2 D��I2
��5�������⻯�������ȶ�����A��
A��HCl B��HBr C��HI
��6��X2+H2=2HX��X����Cl��Br��I���ķ�Ӧ�����ȷ�Ӧ���Ƿ��ȷ�Ӧ�����ȷ�Ӧ��
19��NaOH��һ����Ҫ�Ļ�ѧ�Լ�����Ħ������Ϊ��������
| A�� | 20g | B�� | 20g•mol-1 | C�� | 40mol•g-1 | D�� | 40g•mol-1 L |

 ijѧϰС��̽�����������ȥ��Ӧ����֤���
ijѧϰС��̽�����������ȥ��Ӧ����֤��� ��
��