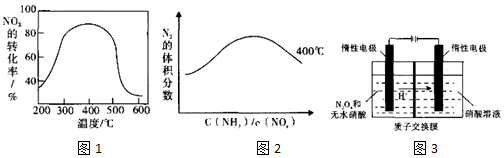
2.下列离子方式正确的是( )
| A. | 向100mL 0.1mol/L的FeSO4溶液中,加入0.01mol Na2O2固体2Fe2++2Na2O2+2H2O═4Na++2Fe(OH)2+O2↑ | |
| B. | 向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全2Al3++3 SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| C. | 苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-?2C6H5OH+CO32- | |
| D. | 向20mL0.5mol/LFeBr2溶液中通入448mLCl2(标准状况):2Fe2++4Br-+3Cl2═2Fe3++6Cl-+2Br2 |
1.在某无色透明的酸性溶液中,能大量共存的离子组是( )
| A. | NH4+、SO42-、Al3+、Cl- | B. | Na+、OH-、K+、Cl- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | K+、NO3-、I-、Na+ |
19.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 相同温度下,测定某物质的量浓度的H2SO4溶液,H3PO4溶液的pH | pH(H2SO4)溶液<pH(H3PO4)溶液 | 非金属性S>P |
| B | 将SO2通入紫色石蕊溶液中 | 溶液先变红后褪色 | SO2具有酸性、漂白性 |
| C | 向AgNO3溶液中滴加过量氨水 | 溶液澄清 | Ag+、NH3•H2O能大量共存 |
| D | 相同的铝片分别和同体积,同温度且c(H+)相等的盐酸,硫酸发生反应 | 为盐酸反应产生气体的速率快 | 酸性;盐酸>硫酸 |
| A. | A | B. | B | C. | C | D. | D |
18.下列关于仪器使用的说法不正确的是( )
| A. | 酸碱中和滴定实验中,锥形瓶用蒸馏水洗涤后,不需要干燥 | |
| B. | 在量取液体后,量筒中残留的液体要用蒸馏水洗涤并转入相应容器 | |
| C. | 在测量或监测温度时,温度计水银球不能碰到容器内璧或底部 | |
| D. | 分液漏斗使用前需要检漏,确认不漏水后方可使用 |
17.下列反应的离子方程式书写正确的是( )
| A. | 将钢片插入稀硝酸中:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O | |
| B. | 稀硫酸与Ba(OH)2溶液反应:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| C. | 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ | |
| D. | 向Na2SiO3溶液中滴加醋酸:SiO32-+2H+=H2SiO3↓ |
16.下列实验操作能达到实验目的是( )
| A. | 用湿润的KI-淀粉试纸鉴别Br2(g)和NO2(g) | |
| B. | 用新制Cu(OH)2悬浊液鉴别乙醛和丙醛 | |
| C. | 将CH4与CH2=CH2混合气体依次通过酸性KMnO4溶液、浓硫酸可得到纯净的CH4 | |
| D. | 用托盘天平、量筒、烧杯、玻璃捧配制10%的NaCl溶液 |
15.2016年入夏以来,我国多地出现暴雨等灾害天气,抢险救灾需要大量物资,下列相关说法正确的是( )
0 159470 159478 159484 159488 159494 159496 159500 159506 159508 159514 159520 159524 159526 159530 159536 159538 159544 159548 159550 159554 159556 159560 159562 159564 159565 159566 159568 159569 159570 159572 159574 159578 159580 159584 159586 159590 159596 159598 159604 159608 159610 159614 159620 159626 159628 159634 159638 159640 159646 159650 159656 159664 203614
| A. | 救灾用的葡萄糖溶液能产生丁达尔效应 | |
| B. | 福尔马林可用于洪水后环境消毒和鱼肉等食益的防腐保鲜 | |
| C. | 医用酒精可用于灾后饮用水消毒 | |
| D. | 淀粉、油脂、蛋白质可为灾民提供营养 |
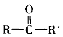 +2
+2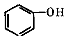 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$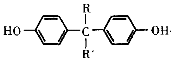 +H2O
+H2O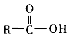 +SOCl2→
+SOCl2→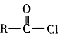 +SO2+HCl
+SO2+HCl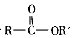 +HCl
+HCl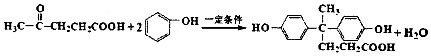 .
.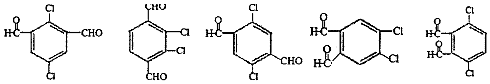 (其中两种).
(其中两种).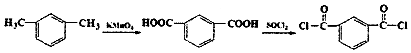 .
.