8.下列说法不正确的是( )
①某种元素的相对原子质量取整数,就是其质量数
②同位素的性质完全相同
③质子数相同,电子数也相同的两种粒子,不可能是一种分子和一种离子
④电子数相同的粒子不一定是同一种元素
⑤一种元素只能有一种质量数
⑥质子数相同的粒子一定是同种元素.
①某种元素的相对原子质量取整数,就是其质量数
②同位素的性质完全相同
③质子数相同,电子数也相同的两种粒子,不可能是一种分子和一种离子
④电子数相同的粒子不一定是同一种元素
⑤一种元素只能有一种质量数
⑥质子数相同的粒子一定是同种元素.
| A. | ②③⑤⑥ | B. | ①②④⑤ | C. | ③④⑤⑥ | D. | ①②⑤⑥ |
7.下列有机物分子中,在氢核磁共振谱中信号强度(个数比)是1:3的是( )
| A. | 邻二甲苯 | B. | 均三甲苯 | C. | 异丙醇 | D. | 丙酸乙酯 |
6.下列选项中符合如图关系的是( )
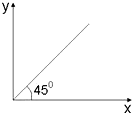

| A. | 第二周期的核电荷数和最高化合价之间的关系 | |
| B. | 烷烃中碳原子数(X)与氢原子数(Y)的关系 | |
| C. | 温度大于100℃时,CH4和C2H4的混合气体在氧气中充分燃烧,同温同压下燃烧前后参与反应的气体的体积之和(X)与生成物的气体体积之和(Y)的关系 | |
| D. | 燃烧一定质量C2H4与C3H6的混合气体,消耗O2的物质的量(Y)与C3H6的质量分数(X)的关系 |
5.下列有关化学用语正确的是( )
| A. | NaOH的电子式: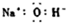 | B. | I4O9(碘酸碘)中碘的化合价为+3,+5 | ||
| C. | NH5的结构式为: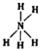 | D. | CO2的比例模型: |
4.对于A2+3B2=2C+D的反应来说,以下化学反应速率的表示中,反应速率最快的是( )
| A. | v(A2)=0.4 mol•L-1•s-1 | B. | v(B2)=0.8 mol•L-1•s-1 | ||
| C. | v(C)=0.6 mol•L-1•s-1 | D. | v(D)=0.6 mol•L-1•min-1 |
3.下列实验现象,是由于发生加成反应而引起的是( )
| A. | 乙烯使酸性高锰酸钾溶液褪色 | |
| B. | 苯与溴水混合,反复振荡后溴水层颜色变浅 | |
| C. | 油脂使溴的四氯化碳溶液褪色 | |
| D. | 甲烷与氯气混合,光照一段时间后黄绿色消失 |
2.同周期的两种主族元素A和B能够形成离子化合物AmBn,已知A的原子序数为a,则B的原子序数可能为( )
| A. | a+8+m-n | B. | a+16-m+n | C. | a+24-m-n | D. | a+18-m-n |
1.镁、锂在元素周期表中具有特殊“对角线”位置关系,它们的性质相似,例如它们的单质在过量氧气中燃烧时均只生成正常的氧化物,以下对锂的性质的叙述正确的是( )
| A. | Li2SO4难溶于水 | B. | Li遇浓硫酸产生“钝化”现象 | ||
| C. | LiOH的水溶液不能使酚酞变红 | D. | Li2CO3受热分解,生成Li2O和CO2 |
20.某烃不与溴水反应,能使酸性高锰酸钾溶液褪色,在Fe存在下与Cl2反应,能生成两种一氯代物,该烃是( )
| A. | 丙烯 | B. | 对二甲苯 | C. | 1-甲基-4-乙基苯 | D. | 1-甲基-2-乙基苯 |
19.含氮化合物是化学与工业中运用广泛的物质.
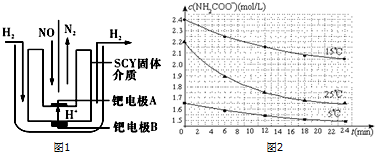
(1)该小组利用电解原理设计了如图1装置进行H2还原NO的实验(高质子导电性的SCY陶瓷(能传递H+)为介质,金属钯薄膜做电极).铂电极B是阳极,钯电极A的电极反应式为2NO+4H++4e-=N2+2H2O.
(2)若工业废水中的NO2-的浓度约为1.0×10-4 mol•L-1,取工业废水5mL 于试管中,滴加2滴0.1mol•L-1的硝酸银溶液,能否看到沉淀现象?试通过计算说明.(注:1mL溶液以20滴计;Ksp(AgNO2)=2×10-8)
(3)已知键能数据,H-H 436,S=S 255,H-S 339,单位kJ/mol.请计算热化学方程式2H2(g)+S2(g)=2H2S(g)的△H=-229KJ/mol
(4)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).
实验测得不同温度下的平衡数据列于下表:
?根据表中数据,列式计算25.0℃时的分解平衡常数:K=c(CO2)•c2(NH3)=[4.8×10-3×$\frac{2}{3}$]2×[4.8×10-3×$\frac{1}{3}$]=1.64×10-8.
?已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图2所示.根据图中信息,如何说明水解反应速率随温度升
高而增大:25.00C时反应物的起始浓度较小,但0-6min的平均反应速率(曲线的斜率)仍比15.00C的大.
0 155990 155998 156004 156008 156014 156016 156020 156026 156028 156034 156040 156044 156046 156050 156056 156058 156064 156068 156070 156074 156076 156080 156082 156084 156085 156086 156088 156089 156090 156092 156094 156098 156100 156104 156106 156110 156116 156118 156124 156128 156130 156134 156140 156146 156148 156154 156158 156160 156166 156170 156176 156184 203614

(1)该小组利用电解原理设计了如图1装置进行H2还原NO的实验(高质子导电性的SCY陶瓷(能传递H+)为介质,金属钯薄膜做电极).铂电极B是阳极,钯电极A的电极反应式为2NO+4H++4e-=N2+2H2O.
(2)若工业废水中的NO2-的浓度约为1.0×10-4 mol•L-1,取工业废水5mL 于试管中,滴加2滴0.1mol•L-1的硝酸银溶液,能否看到沉淀现象?试通过计算说明.(注:1mL溶液以20滴计;Ksp(AgNO2)=2×10-8)
(3)已知键能数据,H-H 436,S=S 255,H-S 339,单位kJ/mol.请计算热化学方程式2H2(g)+S2(g)=2H2S(g)的△H=-229KJ/mol
(4)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).
实验测得不同温度下的平衡数据列于下表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
?已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图2所示.根据图中信息,如何说明水解反应速率随温度升
高而增大:25.00C时反应物的起始浓度较小,但0-6min的平均反应速率(曲线的斜率)仍比15.00C的大.