6.用饱和的氯化铁溶液制取氢氧化铁胶体,正确的操作是( )
| A. | 将饱和氯化铁溶液滴入氢氧化钠溶液中即可 | |
| B. | 将饱和氯化铁溶液滴入热水中,生成棕黄色液体即可 | |
| C. | 将饱和氯化铁溶液滴入沸水中,并继续煮沸至生成红褐色液体即可 | |
| D. | 将饱和氯化铁溶液滴入沸水中,并继续煮沸至生成红褐色沉淀即可 |
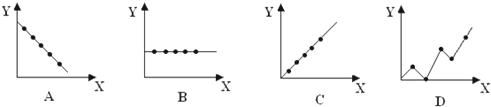
5.化学概念在逻辑上存在如下关系:

对下列概念的说法正确的是( )

对下列概念的说法正确的是( )
| A. | 化合物与纯净物属于重叠关系 | |
| B. | 化合物与氧化物属于交叉关系 | |
| C. | 分解反应与复分解反应属于并列关系 | |
| D. | 钠盐与碳酸盐属于并列关系 |
4.下列说法正确的是( )
| A. | c(H+)<c(OH-)的溶液一定显碱性 | B. | pH=6的溶液一定显酸性 | ||
| C. | pH=7的溶液一定显中性 | D. | Kw只适用于纯水 |
3.25°C时,水的电离达到平衡:H2O?H++OH-,下列叙述正确的是( )
| A. | 将纯水加热到950C时,Kw变大,pH不变,水仍呈中性 | |
| B. | 向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,Kw变小 | |
| C. | 向水中加入少量固体硫酸氢钠,c(H+)增大,平衡逆向移动,KW不变 | |
| D. | 向水中通入HCl气体,平衡逆向移动,溶液导电能力减弱 |
2..某溶液能够使石蕊试液变蓝,则下列离子中一定能大量共存于该溶液的是( )
| A. | HCO3-、Ag+、NO3-、Na+ | B. | Na+、Cl-、CO32-、NO3- | ||
| C. | Fe3+、Na+、Cl-、SO42- | D. | H+、Cl-、CO32-、NH4+ |
20.某同学欲在实验室中对Fe3+与I-的反应进行探究,实现Fe2+与Fe3+的相互转化.
(1)该同学最初的实验操作和现象如下:
①实验Ⅰ的现象是滴加KSCN后溶液无明显变化,加入氯水后溶液变成红色.
②FeCl2溶液与新制氯水反应的离子方程式为2Fe2++Cl2═2Fe3++2Cl-.
(2)该同学分析了导致实验Ⅱ现象的可能原因,并对实验方案进行了改进.改进后的实验操作和现象如下:
根据实验III,甲同学认为Fe3+有可能与I-发生氧化还原反应,请结合实验现象用简明的文字说明他得出上述结论的理由溶液变成黄色,推测生成了I2
(3)该同学认为需要进一步设计实验证明根据实验Ⅲ中现象得出的结论.请补全下表中的实验方案.
(4)上述实验结果表明,Fe3+能与I-发生氧化还原反应;进一步查阅资料知,参加反应的Fe3+与I-的物质的量相同.该同学结合上述实验结论,分析了实验Ⅲ中加入KSCN后溶液变红的原因,认为Fe3+与I-反应的离子方程式应为2Fe3++2I-?2Fe2++I2.
0 154369 154377 154383 154387 154393 154395 154399 154405 154407 154413 154419 154423 154425 154429 154435 154437 154443 154447 154449 154453 154455 154459 154461 154463 154464 154465 154467 154468 154469 154471 154473 154477 154479 154483 154485 154489 154495 154497 154503 154507 154509 154513 154519 154525 154527 154533 154537 154539 154545 154549 154555 154563 203614
(1)该同学最初的实验操作和现象如下:
| 编号 | 操作 | 现象 |
| Ⅰ | 向2 mL 0.1 mol/LFeCl2溶液中滴加KSCN溶液,再滴加氯水 | |
| Ⅱ | 向2 mL 0.1 mol/L FeCl3溶液中滴加KSCN溶液,再滴加0.1 mol/L KI溶液 | 滴加KSCN溶液后,溶液变成红色; 滴加KI溶液后,红色无明显变化 |
②FeCl2溶液与新制氯水反应的离子方程式为2Fe2++Cl2═2Fe3++2Cl-.
(2)该同学分析了导致实验Ⅱ现象的可能原因,并对实验方案进行了改进.改进后的实验操作和现象如下:
| 编号 | 操作 | 现象 |
| Ⅲ | 向2 mL 0.1 mol/L KI溶液中滴加1 mL 0.1 mol/L FeCl3溶液,再滴加KSCN溶液 | 滴加FeCl3溶液后,溶液变成黄色; 滴加KSCN溶液后,溶液变成红色 |
(3)该同学认为需要进一步设计实验证明根据实验Ⅲ中现象得出的结论.请补全下表中的实验方案.
| 编号 | 操作 | 预期现象及结论 |
| Ⅳ | 向2 mL 0.1 mol/L KI溶液中滴加 1 mL 0.1mol/L FeCl3溶液,或CCl4;或铁氰化钾溶液 | 溶液变蓝(或溶液分层,下层溶液为紫色;或生成蓝色沉淀),结论:Fe3+能与I-发生氧化还原反应,生成I2(或Fe2+) |
 某化学学习小组发现在碱性溶液中,NO2会发生如下反应:
某化学学习小组发现在碱性溶液中,NO2会发生如下反应: .
.