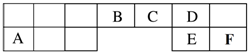
2.下列实验操作正确的是( )
| A. | 可用托盘天平称取10.20g氢氧化钠 | |
| B. | 某实验需要900mL的0.1mol/L的硫酸铜溶液,则配得该溶液需称取22.5g胆矾晶体 | |
| C. | 用10mL量筒量取5.2mL硫酸,仰视时实际量得液体提及大于5.2mL | |
| D. | 焰色反应实验中,连续做两个样品时,应将铂丝用硫酸洗净并灼烧到无特殊焰色 |
18.区分下列各组物质,所加试剂或操作方法完全正确的是( )
| 需鉴别物质 | 方法1 | 方法2 | |
| A | 硫酸铵和磷矿粉 | 加水溶解 | 加熟石灰 |
| B | 一氧化碳和二氧化碳 | 闻气味 | 通过灼热的氧化铜 |
| C | 食盐水和蒸馏水 | 测pH | 蒸发结晶 |
| D | 真黄金和假黄金 (铜铝合金) | 看颜色 | 灼烧 |
| A. | A | B. | B | C. | C | D. | D |
17.下列有关说法中正确的是( )
| A. | 硅单质既不能与酸反应又不能与碱反应 | |
| B. | 晶体硅中每个硅原子与另外四个硅原子形成4个共价键 | |
| C. | 硅与NaOH溶液的反应中NaOH作氧化剂 | |
| D. | 硅元素在地壳中的含量居第一位 |
15.室温条件下,现有四种溶液:①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液.下列有关说法正确的是( )
| A. | 由水电离出的c(H+):①=②=③=④ | |
| B. | 将②、③溶液混合后,pH=7,消耗溶液的体积:③=② | |
| C. | 等体积的①、②、④溶液分别与足量铝粉反应,②生成的H2的物质的量最大 | |
| D. | 向溶液中加入100mL水后,溶液的pH:③>④>①>② |
14.下列事实,其中不能用平衡移动原理解释的是( )
0 154051 154059 154065 154069 154075 154077 154081 154087 154089 154095 154101 154105 154107 154111 154117 154119 154125 154129 154131 154135 154137 154141 154143 154145 154146 154147 154149 154150 154151 154153 154155 154159 154161 154165 154167 154171 154177 154179 154185 154189 154191 154195 154201 154207 154209 154215 154219 154221 154227 154231 154237 154245 203614
| A. | 500℃左右的温度比室温更有利于合成氨反应N2(g)+3H2(g)?2NH3(g)△H<0 | |
| B. | 在恒容密闭容器中充入一定量NO2建立2NO2(g)═N2O4(g)△H<0 平衡后,升高温度,体系颜色加深 | |
| C. | 向水中投入金属Na,最终溶液呈碱性 | |
| D. | FeCl3和KSCN的混合溶液中加入FeCl3固体,溶液颜色加深 |
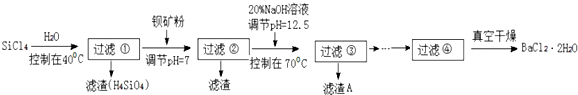
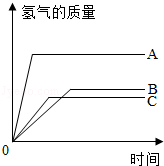
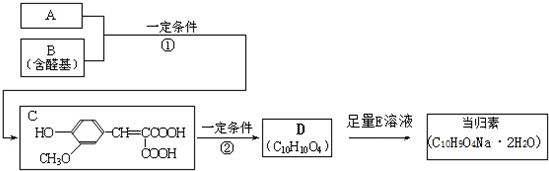
 .
. .
.