4. 空气质量日报中有一项重要检测指标是SO2的含量,结合所学知识回答下列问题.工业制硫酸的过程中,SO2催化氧化的原理为:
空气质量日报中有一项重要检测指标是SO2的含量,结合所学知识回答下列问题.工业制硫酸的过程中,SO2催化氧化的原理为:
2SO2(g)+O2(g)?△催化剂 2SO3(g)+Q
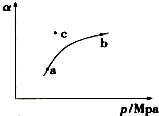
某温度下,测得SO2(g)的平衡转化率(a)与体系总压强( p )的关系如图所示.
(1)a、b两点对应的平衡常数K(a)= K(b) (填“>”、“<”或“=”,下同),SO3浓度c(a)<c(b).c点时,反应速率υ(正)<υ(逆).将一定量的SO2(g)和O2(g)分别通入到体积为2L的恒容密闭容器中,在不同温度下进行反应得到如表中的两组数据:
(2)实验1从开始到反应达到化学平衡时,用去时间t 分钟,则υ(SO2)表示的反应速率为$\frac{1.2}{t}$mol•L-1•min-1,温度T1大于T2的理由是反应放热,温度升高,平衡向左移动,反应物转化率低.
(3)制取SO2的尾气用NaOH溶液吸收,可得到Na2SO3和NaHSO3两种盐.
①0.1mol/L的NaHSO3溶液中c(H+)>c(OH-),用水解和电离理论的角度解释其原因HSO3-的电离程度大于水解程度,若往溶液中加入氨水至中性,则c(Na+)=c(HSO3-)+c(SO32-)+c(H2SO3) (填“>”、“<”或“=”).
②往0.1mol/L 的Na2SO3溶液加入少量NaOH固体,完全溶解后溶液中c(Na+):c(SO32-)的比值变大(填“变大”、“变小”或“保持不变”).
 空气质量日报中有一项重要检测指标是SO2的含量,结合所学知识回答下列问题.工业制硫酸的过程中,SO2催化氧化的原理为:
空气质量日报中有一项重要检测指标是SO2的含量,结合所学知识回答下列问题.工业制硫酸的过程中,SO2催化氧化的原理为:2SO2(g)+O2(g)?△催化剂 2SO3(g)+Q
某温度下,测得SO2(g)的平衡转化率(a)与体系总压强( p )的关系如图所示.
(1)a、b两点对应的平衡常数K(a)= K(b) (填“>”、“<”或“=”,下同),SO3浓度c(a)<c(b).c点时,反应速率υ(正)<υ(逆).将一定量的SO2(g)和O2(g)分别通入到体积为2L的恒容密闭容器中,在不同温度下进行反应得到如表中的两组数据:
| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | ||
| SO2 | O2 | SO2 | O2 | ||
| 1 | T1 | 4 | 2 | x | 0.8 |
| 2 | T2 | 4 | 2 | 0.4 | y |
(3)制取SO2的尾气用NaOH溶液吸收,可得到Na2SO3和NaHSO3两种盐.
①0.1mol/L的NaHSO3溶液中c(H+)>c(OH-),用水解和电离理论的角度解释其原因HSO3-的电离程度大于水解程度,若往溶液中加入氨水至中性,则c(Na+)=c(HSO3-)+c(SO32-)+c(H2SO3) (填“>”、“<”或“=”).
②往0.1mol/L 的Na2SO3溶液加入少量NaOH固体,完全溶解后溶液中c(Na+):c(SO32-)的比值变大(填“变大”、“变小”或“保持不变”).
3.某温度下,反应2A(g)?B(g)-Q 在密闭容器中达到平衡,平衡后c(A):c(B)=a,若改变某一条件,足够时间后反应达到平衡状态,此时c(A):c(B)=b,下列叙述正确的是( )
| A. | 若保持温度,保持容器容积固定不变,向容器内补充B气体,则有a<b | |
| B. | 若保持温度、压强不变,充入惰性气体,则有a>b | |
| C. | 若其他条件不变,升高温度,则有a<b | |
| D. | 若a=b,则可能是在该温度下,保持容器容积固定不变情况下充入了惰性气体 |
1.工业制硝酸的主要反应是:4NH3(g)+5O2(g)?4NO(g)+6H2O (g)+1025kJ
(1)该反应的平衡常数表达式为$\frac{{c}^{4}(NO){c}^{6}({H}_{2}O)}{{c}^{4}(N{H}_{3}){c}^{5}({O}_{2})}$;升高温度K值减小 (填“增大”、“减小”或“不变”).
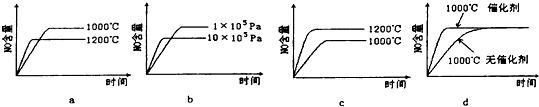
(2)若反应物起始的物质的量相同,下列关系图错误的是c (填字母序号).
(3)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
①起始时物料比c (O2):c (NH3)>1.25,其原因是增大氨气的转化率.
②反应在第2min到第4min时O2的平均反应速率为0.1875;
③反应在第8min改变的反应条件可能是增大反应物的浓度.
(1)该反应的平衡常数表达式为$\frac{{c}^{4}(NO){c}^{6}({H}_{2}O)}{{c}^{4}(N{H}_{3}){c}^{5}({O}_{2})}$;升高温度K值减小 (填“增大”、“减小”或“不变”).
(2)若反应物起始的物质的量相同,下列关系图错误的是c (填字母序号).

(3)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
| 时间/浓度 | c(NH3)(mol/L) | C(O2)(mol/L) | C(NO)(mol/L) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.8 | 0.975 | 0.5 |
②反应在第2min到第4min时O2的平均反应速率为0.1875;
③反应在第8min改变的反应条件可能是增大反应物的浓度.
20.某有机物M的分子式为C5H12O,它能和钠反应产生氢气,且它是烯烃在一定条件下与水发生加成反应的产物,M的结构有( )
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
19.下列各有机物的命名正确的是( )
| A. | 2,2-甲基-3-乙基丁烷 | B. | 2-甲基-3-乙基戊烷 | ||
| C. | 3-甲基-2-乙基戊烷 | D. | 2,3,4-3甲基丁烷 |
18.下列叙述中,正确的是( )
| A. | 在多电子的原子里,能量高的电子通常在离核近的区域活动 | |
| B. | 核外电子总是先排在能量低的电子层上 | |
| C. | 两种微粒,若核外电子排布完全相同,则其化学性质一定相同 | |
| D. | 微粒的最外层只能是8个或2个电子才稳定 |
17.下列说法不正确的是( )
①质子数相同的粒子一定属于同一种元素②同位素的性质完全相同③质子数相同,电子数也相同的两种粒子,不可能是一种分子和一种离子④电子数相同的粒子不一定是同一种元素⑤一种元素只能有一种质量数.
①质子数相同的粒子一定属于同一种元素②同位素的性质完全相同③质子数相同,电子数也相同的两种粒子,不可能是一种分子和一种离子④电子数相同的粒子不一定是同一种元素⑤一种元素只能有一种质量数.
| A. | ②③⑤ | B. | ①②④⑤ | C. | ①②⑤ | D. | ③④⑤ |
16.将铁粉和铜粉的均匀混合物,平均分成三等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成NO的体积和剩余金属的质量如下表(设硝酸的还原产物只有NO)
由上述数据推测:
(1)硝酸的物质的量浓度;
(2)③中溶解金属的成分是什么?其相应的质量为多少克?
| 编号 | ① | ② | ③ |
| 稀硝酸体积/mL | 100 | 200 | 300 |
| 剩余金属/g | 30.4 | 22 | 12.8 |
| NO体积/mL | 2240 | 4480 | 6720 |
(1)硝酸的物质的量浓度;
(2)③中溶解金属的成分是什么?其相应的质量为多少克?
15.下列说法正确的是( )
0 153488 153496 153502 153506 153512 153514 153518 153524 153526 153532 153538 153542 153544 153548 153554 153556 153562 153566 153568 153572 153574 153578 153580 153582 153583 153584 153586 153587 153588 153590 153592 153596 153598 153602 153604 153608 153614 153616 153622 153626 153628 153632 153638 153644 153646 153652 153656 153658 153664 153668 153674 153682 203614
| A. | 一个反应能否自发进行,由焓变、熵变、反应温度共同决定 | |
| B. | 在同一条件下,不同物质有不同的熵变,其体系混乱度越大,熵值越小 | |
| C. | 自发进行的反应一定能迅速发生 | |
| D. | 低温时,吸热且熵减的反应可能会自发发生 |
