11.合成氨的反应为:3H2+N2?2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3)(单位为mol•L-1•s-1),则下列关系正确的是( )
| A. | v(H2)=v(N2)=v(NH3) | B. | v(H2)=3 v(N2) | C. | v(N2)=2 v(NH3) | D. | 2v(NH3)=3v(H2) |
9.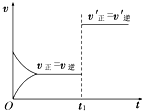 对可逆反应:2A(g)+B(s)?3C(s)+2D(g);△H>0.如图所示为正逆反应速率(v)与时间(t)关系的示意图,如果在t1时刻改变以下条件:
对可逆反应:2A(g)+B(s)?3C(s)+2D(g);△H>0.如图所示为正逆反应速率(v)与时间(t)关系的示意图,如果在t1时刻改变以下条件:
①加入A;
②加入催化剂;
③加压;
④升温;
⑤减少C
符合图示的条件是( )
 对可逆反应:2A(g)+B(s)?3C(s)+2D(g);△H>0.如图所示为正逆反应速率(v)与时间(t)关系的示意图,如果在t1时刻改变以下条件:
对可逆反应:2A(g)+B(s)?3C(s)+2D(g);△H>0.如图所示为正逆反应速率(v)与时间(t)关系的示意图,如果在t1时刻改变以下条件:①加入A;
②加入催化剂;
③加压;
④升温;
⑤减少C
符合图示的条件是( )
| A. | ②③ | B. | ①② | C. | ③④ | D. | ④⑤ |
8.已知:4NH3(g)+5O2(g)?4NO(g)+6H2O(g),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列关系不正确的是( )
| A. | 4v(NH3)=5v(O2) | B. | 6v(O2)=5v(H2O) | C. | 3v(NH3)=2v(H2O) | D. | 4v(O2)=5v(NO) |
7.有100mL氯化镁和氯化铝的混合溶液,其中c (Mg2+)为0.1mol•L-1,c(Cl-)为0.65mol•L-1.要使Mg2+全部转化为沉淀分离出来,至少需加2mol•L-1NaOH溶液的体积为( )
| A. | 40 mL | B. | 72 mL | C. | 128 mL | D. | 20 mL |
6.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 2L 1mol/L Na2SO4溶液中离子总数为3NA | |
| B. | 25℃、101.3kPa时,11.2L H2中含有的原子数为NA | |
| C. | 4℃、101.3kPa时,54mL H2O中含有的原子数为3NA | |
| D. | 78g Na2O2与足量水充分反应时电子转移数为NA |
5.某无色溶液中一定能大量共存的离子组是( )
| A. | Cu2+、Na+、NO3-、SO42- | B. | Ba2+、NH4+、Cl-、SO42- | ||
| C. | Na+、K+、ClO-、SO42- | D. | H+、Na+、I-、NO3- |
4.常温时,下列块状金属中能全部溶于足量浓硝酸的是( )
| A. | Al | B. | Ag | C. | Fe | D. | Pt |
3.下列说法正确的是( )
| A. | 硫粉在过量的纯氧中燃烧可以生成大量的SO3 | |
| B. | SO2能使品红溶液、酸性KMnO4溶液褪色,褪色原理相同 | |
| C. | 可以用品红溶液鉴别SO2和CO2 | |
| D. | 少量SO2通过CaCl2的溶液能生成白色沉淀 |
2.下列有关实验现象或结论的描述不正确的是( )
0 153172 153180 153186 153190 153196 153198 153202 153208 153210 153216 153222 153226 153228 153232 153238 153240 153246 153250 153252 153256 153258 153262 153264 153266 153267 153268 153270 153271 153272 153274 153276 153280 153282 153286 153288 153292 153298 153300 153306 153310 153312 153316 153322 153328 153330 153336 153340 153342 153348 153352 153358 153366 203614
| A. | 铅蓄电池充电时,阳极的反应为:PbSO4+2H2O+2e-═PbO2+SO42-+4H+ | |
| B. | FeCl2溶液与K3[Fe(CN)6]溶液混合后得到特征蓝色沉淀,利用此反应可检验Fe2+ | |
| C. | 常温下将5mL 0.1 mol/LNa2S2O3溶液、5mL 0.01 mol/LNa2S2O3溶液分别与5mL 0.1 mol/LH2SO4溶液混合并搅拌,通过记录溶液中出现浑浊的时间,可确定浓度对化学反应速率的影响 | |
| D. | 处理含有Hg2+离子的废水可加入硫化钠,使Hg2+离子转化为HgS沉淀 |