20.下列热化学方程式中,△H的绝对值能表示可燃物的燃烧热的是( )
| A. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-110.5 kJ•mol-1 | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-802.3 kJ•mol-1 | |
| C. | 2CO(g)+1O2(g)═2CO2(g)△H=-566 kJ•mol-1 | |
| D. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1 |
19.室温下等体积混合0.12mol•L-1的盐酸和0.05mol•L-1的Ba(OH)2溶液后,溶液的pH等于( )
| A. | 2.0 | B. | 12.3 | C. | 1.7 | D. | 12.0 |
18.一定条件下反应H2(g)+I2(g)═2HI(g)达到平衡状态的标志是( )
| A. | υ(正、H2)=υ(逆、HI) | |
| B. | 容器内的总压强不随时间而变化 | |
| C. | 单位时间内生成2n mol HI的同时,生成n mol的I2 | |
| D. | H2、I2、HI的反应速率比为2:2:1的状态 |
17.胶体区别于其它分散系最本质的特征是( )
| A. | 外观澄清、稳定 | B. | 分散质粒子直径为1---100nm | ||
| C. | 分散至粒子能透过半透膜 | D. | 丁达尔现象 |
15.下列说法正确的是( )
| A. | CaCl2是中性干燥剂可以干燥NH3、SO2 | |
| B. | 检查病人胃病所用的钡餐,既可以用BaSO4,也可以用BaCO3 | |
| C. | 氮氧化物的大量排放是造成光化学烟雾的主要原因 | |
| D. | 雨水样品放置一段时间后,酸性增强的原因是因为溶解了空气中的CO2 |
14.中国科学家利用干冰和金属钠在不锈钢反应釜中反应合成出微米级金刚石,其反应为CO2(s)+Na$\stackrel{440℃}{→}$金刚石+石墨+Na2CO3.下列说法不正确的是( )
| A. | 金刚石与石墨互为同素异形体 | |
| B. | 11.5 g金属钠的物质的量为0.5 mol | |
| C. | 44 g CO2在标准状况下的体积为22.4 L | |
| D. | 该反应中碳元素发生了氧化反应 |
13.常温下,在下列溶液中一定能大量共存的离子组是( )
| A. | 酸性溶液:Na+、NH4+、SO32-、NO3- | |
| B. | 滴加石蕊试剂呈红色的溶液:Na+、Al3+、SO42-、Cl- | |
| C. | 无色透明溶液:MnO4-、SO42-、K+、NO3- | |
| D. | 强碱性的溶液:Al3+、NH4+、Cl-、NO3- |
12.现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)写出BA3的电子式: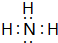 .
.
(2)B元素基态原子中能量最高的电子,其电子云在空间有3个取向,原子轨道呈哑铃形.
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为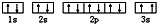 ,该同学所画的电子排布图违背了泡利原理.
,该同学所画的电子排布图违背了泡利原理.
(4)比较B和D的电负性N>P(填元素符号)
(5)G位于ⅦB族d区,该元素的核外电子排布式为1s22s22p63s23p63d54s2.
(6)检验F元素的方法是焰色反应,请用原子结构的知识解释产生此现象的原因:当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子.电子从较高能量的激发态跃迁到较低能量的激发态或基态时,将以光的形式释放能量.
0 153106 153114 153120 153124 153130 153132 153136 153142 153144 153150 153156 153160 153162 153166 153172 153174 153180 153184 153186 153190 153192 153196 153198 153200 153201 153202 153204 153205 153206 153208 153210 153214 153216 153220 153222 153226 153232 153234 153240 153244 153246 153250 153256 153262 153264 153270 153274 153276 153282 153286 153292 153300 203614
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下: I1=738kJ•mol-1 I2=1451kJ•mol-1 I3=7733kJ•mol-1 I4=10540kJ•mol-1 |
| D原子价电子层的p轨道半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
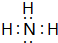 .
.(2)B元素基态原子中能量最高的电子,其电子云在空间有3个取向,原子轨道呈哑铃形.
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为
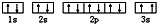 ,该同学所画的电子排布图违背了泡利原理.
,该同学所画的电子排布图违背了泡利原理.(4)比较B和D的电负性N>P(填元素符号)
(5)G位于ⅦB族d区,该元素的核外电子排布式为1s22s22p63s23p63d54s2.
(6)检验F元素的方法是焰色反应,请用原子结构的知识解释产生此现象的原因:当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子.电子从较高能量的激发态跃迁到较低能量的激发态或基态时,将以光的形式释放能量.
 回答下列问题:
回答下列问题: