11.下列物质①NaOH、②氯水、③空气、④氢硫酸、⑤Na2SO3、⑥Na2CO3,其中能与SO2在一定条件下发生反应的是( )
| A. | ①②④⑤ | B. | ②④⑤⑥ | C. | ②③④⑤ | D. | 全部 |
9.一化学研究性学习小组对某Na2CO3和NaHC:O3的混合溶液(以下简称“样品溶液”)的组成进行探究.取20.0mL样品溶液不断滴入1.0mol•L-1的稀盐酸,加入盐酸的体积和产生的现象见表.
回答下列有关问题:
(1)配制1.0mol•L-1的稀盐酸250mL,需要36.5%的浓盐酸20.8mL(36.5%的浓盐酸的密度约为1.2g•cm-3);实验配制过程中所用的玻璃仪器除烧杯、玻璃棒和量筒外,还有250mL容量瓶、胶头滴管.
(2)第Ⅱ阶段溶液中反应的离子方程式为:HCO3-+H+=H2O+CO2↑.样品溶液中c(CO32-)=0.500mol•L-1mol•L-1.
| 反应阶段 | I | II | III |
| 盐酸体积x/mL | 0<x≤10.0 | 10.0<x≤40.0 | x>40.0 |
| 现 象 | 无气体 | 产生气体 | 无气体 |
| 解释 | CO32-+H+=HCO3- |
(1)配制1.0mol•L-1的稀盐酸250mL,需要36.5%的浓盐酸20.8mL(36.5%的浓盐酸的密度约为1.2g•cm-3);实验配制过程中所用的玻璃仪器除烧杯、玻璃棒和量筒外,还有250mL容量瓶、胶头滴管.
(2)第Ⅱ阶段溶液中反应的离子方程式为:HCO3-+H+=H2O+CO2↑.样品溶液中c(CO32-)=0.500mol•L-1mol•L-1.
8.下列各组离子在水溶液中能大量共存的是( )
| A. | NH4+、Na+、Cl-、OH- | B. | Fe3+、H+、Cl-、CH3COO- | ||
| C. | Fe3+、SCN-、K+、Cl- | D. | H+、Fe2+、SO42-、Cl- |
7.氢能是一种洁净的可再生能源,制备和储存氢气是氢能开发的两个关键环节.
Ⅰ氢气的制取
(1)水是制取氢气的常见原料,下列说法正确的是AB(填序号).
A.H3O+的空间构型为三角锥形
B.水的沸点比硫化氢高
C.冰晶体中,1mol水分子可形成4mol氢键
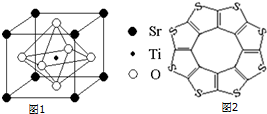
(2)科研人员研究出以钛酸锶为电极的光化学电池,用紫外线照射钛酸锶电极,使水分解产生氢气.已知钛酸锶晶胞结构如图1,则其化学式为SrTiO3.
Ⅱ氢气的存储
(3)Ti(BH4)2是一种储氢材料.
①Ti原子在基态时的核外电子排布式是1s22s22p63s23p63d24s2或[Ar]3d24s2.
②Ti(BH4)2可由TiCl4和LiBH4反应制得,TiCl4 熔点-25.0℃,沸点136.94℃,常温下是无色液体,则TiCl4晶体类型为分子晶体.
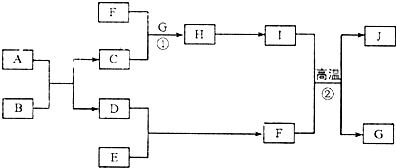
(4)最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如图2所示),每个平面上下两侧最多可储存10个H2分子.
①元素电负性大小关系是:C<S(填“>”、“=”或“<”).
②分子中C原子的杂化轨道类型为sp2.
③有关键长数据如下:
从表中数据可以看出,C16S8中碳硫键键长介于C-S与C═S之间,原因可能是:分子中的C与S原子之间有π键或分子中的碳硫键具有一定程度的双键性质.
④C16S8与H2微粒间的作用力是范德华力.
Ⅰ氢气的制取
(1)水是制取氢气的常见原料,下列说法正确的是AB(填序号).
A.H3O+的空间构型为三角锥形
B.水的沸点比硫化氢高
C.冰晶体中,1mol水分子可形成4mol氢键
(2)科研人员研究出以钛酸锶为电极的光化学电池,用紫外线照射钛酸锶电极,使水分解产生氢气.已知钛酸锶晶胞结构如图1,则其化学式为SrTiO3.

Ⅱ氢气的存储
(3)Ti(BH4)2是一种储氢材料.
①Ti原子在基态时的核外电子排布式是1s22s22p63s23p63d24s2或[Ar]3d24s2.
②Ti(BH4)2可由TiCl4和LiBH4反应制得,TiCl4 熔点-25.0℃,沸点136.94℃,常温下是无色液体,则TiCl4晶体类型为分子晶体.
(4)最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如图2所示),每个平面上下两侧最多可储存10个H2分子.
①元素电负性大小关系是:C<S(填“>”、“=”或“<”).
②分子中C原子的杂化轨道类型为sp2.
③有关键长数据如下:
| C-S | C═S | C16S8中碳硫键 | |
| 键长/pm | 181 | 155 | 176 |
④C16S8与H2微粒间的作用力是范德华力.
4.下列叙述正确的是( )
| A. | 镁铝合金的抗腐蚀能力强,不与稀硫酸反应 | |
| B. | Na的金属活动性比Mg的强,故可用Na与MgCl2溶液反应制Mg | |
| C. | 钠可与冷水剧烈反应,而镁与热水才能反应,说明钠比镁活泼 | |
| D. | Fe在Cl2中燃烧生成FeCl3,故在与其他非金属反应的产物中,Fe也显+3价 |
3. 下列各组物质中,能一步实现如图所示①~⑤转化关系的是( )
下列各组物质中,能一步实现如图所示①~⑤转化关系的是( )
 下列各组物质中,能一步实现如图所示①~⑤转化关系的是( )
下列各组物质中,能一步实现如图所示①~⑤转化关系的是( )| X | Y | Z | W | |
| A | C | CO | CO2 | Na2CO3 |
| B | Fe3O4 | Fe | FeCl2 | FeCl3 |
| C | H2SO4 | SO2 | S | SO3 |
| D | Al | Al2O3 | NaAlO2 | Al(OH)3 |
| A. | A | B. | B | C. | C | D. | D |
2.下列说法中,正确的是( )
0 152968 152976 152982 152986 152992 152994 152998 153004 153006 153012 153018 153022 153024 153028 153034 153036 153042 153046 153048 153052 153054 153058 153060 153062 153063 153064 153066 153067 153068 153070 153072 153076 153078 153082 153084 153088 153094 153096 153102 153106 153108 153112 153118 153124 153126 153132 153136 153138 153144 153148 153154 153162 203614
| A. | 向NaAlO2溶液中滴入NaHCO3溶液有白色沉淀,原因是二者可以发生双水解反应 | |
| B. | 电解精炼铜时,若阴极得到1.204×1024个电子,则阳极质量减少6.4g | |
| C. | 使甲基橙变红色溶液:Mg2+、K+、SO42-、NO3-能大量共存 | |
| D. | Na2S在空气中长期放置变浑浊的离子方程式为:2S2-+O2+4H+=2S+2H2O |
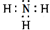 ,含有的化学键类型是极性共价键
,含有的化学键类型是极性共价键