题目内容
2.下列说法中,正确的是( )| A. | 向NaAlO2溶液中滴入NaHCO3溶液有白色沉淀,原因是二者可以发生双水解反应 | |
| B. | 电解精炼铜时,若阴极得到1.204×1024个电子,则阳极质量减少6.4g | |
| C. | 使甲基橙变红色溶液:Mg2+、K+、SO42-、NO3-能大量共存 | |
| D. | Na2S在空气中长期放置变浑浊的离子方程式为:2S2-+O2+4H+=2S+2H2O |
分析 A.碳酸氢根离子的酸性大于氢氧化铝,二者反应生成氢氧化铝沉淀和碳酸根离子,不是发生双水解反应;
B.粗铜中含有比金属铜活泼的金属铁、锌等,电解时,阳极放电的先是铁和锌,最后是铜;
C.使甲基橙变红色溶液中存在大量氢离子,四种离子之间不反应,都不与氢离子反应,能够共存;
D.硫化钠溶液在空气中能够被氧气氧化成硫单质,反应物中的水不能拆开.
解答 解:A.由于碳酸氢根离子的酸性大于氢氧化铝,则向NaAlO2溶液中滴入NaHCO3溶液生成氢氧化铝沉淀和碳酸钠,没有发生双水解反应,故A错误;
B.粗铜中含有比金属铜活泼的金属铁、锌等,电解时,阳极放电的先是铁和锌,最后是铜,所以当转移的电子数为1.204×1024个时,则阳极溶解的铜的质量小于64g,故B错误;
C.使甲基橙变红色溶液为酸性溶液,溶液中存在大量氢离子,Mg2+、K+、SO42-、NO3-之间不发生反应,都不与氢离子反应,在溶液中能够大量共存,故C正确;
D.Na2S在空气中长期放置变浑浊,是硫离子的还原性被空气中的氧气氧化生成硫单质,反应物中水不能写出氢离子,正确的离子方程式为:2S2-+02+2H20=2S+40H-,故D错误;
故选C.
点评 本题考查较为综合,涉及离子共存、离子方程式书写、电解原理等知识,明确离子反应发生条件为解答关键,注意掌握离子方程式书写原则,A为易错点,注意偏铝酸根离子与碳酸氢根离子的反应不属于双水解反应.

练习册系列答案
相关题目
5.NA为阿伏加罗常数的值,下列有关计算正确的是( )
| A. | 标准状况下,22.4LCHCl3中含有的氯原子数目为3NA | |
| B. | 46g二氧化氮含有的原子总数一定为3NA | |
| C. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2NHO3+4N2↑+9H2O该反应生成28gN2时,转移的电子数目为4NA | |
| D. | 在密闭容器中加入1,5molH2和0.5molN2,充分反应后可得到NH3分子数为NA |
7.氢能是一种洁净的可再生能源,制备和储存氢气是氢能开发的两个关键环节.
Ⅰ氢气的制取
(1)水是制取氢气的常见原料,下列说法正确的是AB(填序号).
A.H3O+的空间构型为三角锥形
B.水的沸点比硫化氢高
C.冰晶体中,1mol水分子可形成4mol氢键
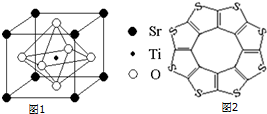
(2)科研人员研究出以钛酸锶为电极的光化学电池,用紫外线照射钛酸锶电极,使水分解产生氢气.已知钛酸锶晶胞结构如图1,则其化学式为SrTiO3.
Ⅱ氢气的存储
(3)Ti(BH4)2是一种储氢材料.
①Ti原子在基态时的核外电子排布式是1s22s22p63s23p63d24s2或[Ar]3d24s2.
②Ti(BH4)2可由TiCl4和LiBH4反应制得,TiCl4 熔点-25.0℃,沸点136.94℃,常温下是无色液体,则TiCl4晶体类型为分子晶体.
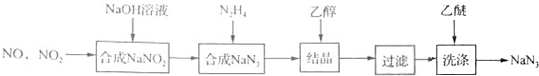
(4)最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如图2所示),每个平面上下两侧最多可储存10个H2分子.
①元素电负性大小关系是:C<S(填“>”、“=”或“<”).
②分子中C原子的杂化轨道类型为sp2.
③有关键长数据如下:
从表中数据可以看出,C16S8中碳硫键键长介于C-S与C═S之间,原因可能是:分子中的C与S原子之间有π键或分子中的碳硫键具有一定程度的双键性质.
④C16S8与H2微粒间的作用力是范德华力.
Ⅰ氢气的制取
(1)水是制取氢气的常见原料,下列说法正确的是AB(填序号).
A.H3O+的空间构型为三角锥形
B.水的沸点比硫化氢高
C.冰晶体中,1mol水分子可形成4mol氢键
(2)科研人员研究出以钛酸锶为电极的光化学电池,用紫外线照射钛酸锶电极,使水分解产生氢气.已知钛酸锶晶胞结构如图1,则其化学式为SrTiO3.

Ⅱ氢气的存储
(3)Ti(BH4)2是一种储氢材料.
①Ti原子在基态时的核外电子排布式是1s22s22p63s23p63d24s2或[Ar]3d24s2.
②Ti(BH4)2可由TiCl4和LiBH4反应制得,TiCl4 熔点-25.0℃,沸点136.94℃,常温下是无色液体,则TiCl4晶体类型为分子晶体.
(4)最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如图2所示),每个平面上下两侧最多可储存10个H2分子.
①元素电负性大小关系是:C<S(填“>”、“=”或“<”).
②分子中C原子的杂化轨道类型为sp2.
③有关键长数据如下:
| C-S | C═S | C16S8中碳硫键 | |
| 键长/pm | 181 | 155 | 176 |
④C16S8与H2微粒间的作用力是范德华力.
11.下列实验能达到目的是( )
| A. | 加入盐酸以除去硫酸钠中少量的碳酸钠杂质 | |
| B. | 用玻璃棒搅拌漏斗中的液体以加快反应速率 | |
| C. | 用稀硫酸和锌反应制氢气时加入少许硫酸铜以加快反应速率 | |
| D. | 在容量瓶中加入一定体积的水,再加入浓硫酸配制准确浓度的稀硫酸 |
12.下列关于电解质的说法正确的是( )
| A. | 液态HCl不导电,所以HCl不是电解质 | |
| B. | NH3溶于水形成的溶液能导电,所以NH3是电解质 | |
| C. | Cl2溶于水能导电,所以Cl2是电解质 | |
| D. | BaSO4在水溶液中难导电,但熔融下能导电所以BaSO4是电解质 |
 .
.