12.向NaBr、NaI、Na2SO3混合溶液中通入过量的氯气后,将溶液蒸干并充分灼烧,得到的固体物质为( )
| A. | NaCl Na2SO4 | B. | NaCl NaBr Na2SO4 | ||
| C. | NaCl Na2SO4 I2 | D. | NaCl NaI Na2SO4 |
9.下列叙述错误的是( )
| A. | 检验NH4+时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验逸出的气体 | |
| B. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| C. | 实验室用NH4Cl和Ca(OH)2制备NH3涉及氧化还原反应 | |
| D. | 将分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 |
8.由丙烷、乙烯和乙炔组成的混合气体,完全燃烧生成CO2和H2O的物质的量相等,则原混合气体中三种组分的体积比为( )
| A. | 1:2:4 | B. | 1:2:3 | C. | 3:2:1 | D. | 2:5:2 |
7.炼铝厂的废料中主要含Al、Al2O3及少量SiO2和FeO•xFe2O3,可用于制备明矾[KAl(SO4)2•12H2O].工艺流程如下:

(1)“酸浸”过程中的应选择H2SO4(写酸的化学式).为提高浸出速率,除适当增大酸的浓度外,还可采取的措施有提高反应温度、粉碎等.(写出两条)
(2)操作Ⅰ是过滤,操作Ⅱ是蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(3)在溶液A中加入高锰酸钾发生反应的离子方程式为(该条件下MnO4-转化为Mn2+)5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O.
已知:生成氢氧化物沉淀的pH如下表所示
调节pH=3的目的是使Fe3+转化成Fe(OH)3沉淀,防止Al3+沉淀.此步骤中,可以用H2O2代替KMnO4,写出H2O2的电子式 .
.
(4)只用一种试剂检验溶液A中是否存在Fe2+,该试剂是高锰酸钾酸性溶液或铁氰化钾溶液(写名称).
(5)己知在pH=3、加热条件下,加入MnSO4发生反应的离子方程式为3Mn2++2MnO4-+2H2O═5MnO2+4H+.

(1)“酸浸”过程中的应选择H2SO4(写酸的化学式).为提高浸出速率,除适当增大酸的浓度外,还可采取的措施有提高反应温度、粉碎等.(写出两条)
(2)操作Ⅰ是过滤,操作Ⅱ是蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(3)在溶液A中加入高锰酸钾发生反应的离子方程式为(该条件下MnO4-转化为Mn2+)5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O.
已知:生成氢氧化物沉淀的pH如下表所示
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
 .
.(4)只用一种试剂检验溶液A中是否存在Fe2+,该试剂是高锰酸钾酸性溶液或铁氰化钾溶液(写名称).
(5)己知在pH=3、加热条件下,加入MnSO4发生反应的离子方程式为3Mn2++2MnO4-+2H2O═5MnO2+4H+.
5.下表中评价合理的是( )
0 152938 152946 152952 152956 152962 152964 152968 152974 152976 152982 152988 152992 152994 152998 153004 153006 153012 153016 153018 153022 153024 153028 153030 153032 153033 153034 153036 153037 153038 153040 153042 153046 153048 153052 153054 153058 153064 153066 153072 153076 153078 153082 153088 153094 153096 153102 153106 153108 153114 153118 153124 153132 203614
| A. | 石灰乳与Na2CO3溶液混合:Ca2++CO32-═CaCO3↓正确 | |
| B. | 向碳酸镁中加入稀盐酸:CO32-+2H+═CO2↑+H2O 错误,碳酸镁不应该写成离子形式 | |
| C. | 向硫酸铵溶液中加入氢氧化钡溶液:Ba2++SO42-═BaSO4↓正确 | |
| D. | 氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++2OH-+2H++SO42-═CaSO4↓+2H2O 错误,反应物和产物的配比不正确 |
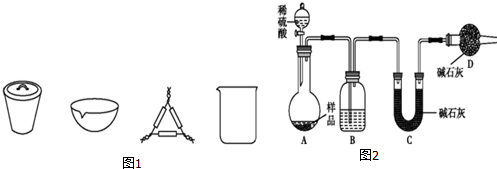
 浓硝酸是一种常见的酸,加热或见光易分解生成NO2.某实验小组欲探究碳与浓硝酸的反应情况.实验装置如图.回答下列问题:
浓硝酸是一种常见的酸,加热或见光易分解生成NO2.某实验小组欲探究碳与浓硝酸的反应情况.实验装置如图.回答下列问题: